有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E正一价阳离子M能层电子已排满。D与B可形成离子化合物其晶胞结构如图所示。请回答下列问题:

(1)E元素原子基态时的价电子排布图为___________ ;
(2)A2F分子中F原子的杂化类型是_______ ,F的氧化物FO3分子空间构型为______ ;
(3)CA3极易溶于水,其原因主要是________ ,试判断CA3溶于水后形成CA3·H2O的合理结构________ (填字母代号),从氢键的形成角度回答推理依据是:___________ 。
(a) (b)
(b)
(4)E的晶胞常采取________ 堆积方式。
(5)从图中可以看出,D跟B形成的离子化合物的化学式为_________ ;该离子化合物晶体的密度为ag/cm3,则晶胞的体积是_______ cm3(写出表达式即可,NA表示阿伏加德罗常数的值)。

(1)E元素原子基态时的价电子排布图为
(2)A2F分子中F原子的杂化类型是
(3)CA3极易溶于水,其原因主要是
(a)
 (b)
(b)
(4)E的晶胞常采取
(5)从图中可以看出,D跟B形成的离子化合物的化学式为
更新时间:2017-05-10 16:49:01
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】已知a—f是元素周期表中前四周期常见的元素,其结构或者性质信息如表所示:
(1)元素a有___________ 种不同能级的电子
(2)b、c的第一电离能的大小顺序为___________ (填元素符号),请从原子结构的角度解释原因:___________ 。
(3)a、c的气态氢化物中,沸点更低的是___________ (填化学式),更稳定的是___________ (填化学式)。
(4)d元素在元素周期表中的位置是___________ ,基态原子的价电子轨道表示式是___________ 。
(5)在f元素的同主族元素中,最高价氧化物对应水化物的酸性最强的是___________ (填化学式)
(6)e元素的块状单质在与极稀的b元素最高价氧化物对应水化物的反应过程中,单质溶解但未观测到气泡的生成,b元素以一种常见离子的形式存在,请写出该反应的离子方程式___________ 。检验产物中b元素存在形式的方法是:___________ 。
| 元素 | 结构或者性质信息 |
| a | 原子的L层上s能级电子数等于p能级电子数 |
| b | 非金属元素,其单质为气态,有多种氧化物且都是大气污染物 |
| c | 原子的最外层电子数是内层电子数的3倍 |
| d | 元素的正三价离子的3d能级为半充满 |
| e | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
| f | 单质常温、常压下是易挥发的液体,基态原子的N层上有1个未成对的p电子 |
(2)b、c的第一电离能的大小顺序为
(3)a、c的气态氢化物中,沸点更低的是
(4)d元素在元素周期表中的位置是
(5)在f元素的同主族元素中,最高价氧化物对应水化物的酸性最强的是
(6)e元素的块状单质在与极稀的b元素最高价氧化物对应水化物的反应过程中,单质溶解但未观测到气泡的生成,b元素以一种常见离子的形式存在,请写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】氧化锌广泛应用于有机高分子材料、医药、食品等领域。以氧化锌烟灰(含 及少量
及少量 、
、 、
、 等)为原料制备氧化锌的工艺流程如下:
等)为原料制备氧化锌的工艺流程如下:

已知:用有机溶剂 从水溶液中萃取A时,
从水溶液中萃取A时,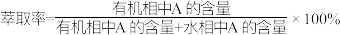
(1)为了提高酸浸效果,可采取的措施有______________________ (任写一点)。
(2)“滤渣1”的主要成分除了 还有
还有_________________________________ 。
(3)“沉铁”操作时不能用 代替
代替 ,原因是
,原因是_________________________________ 。
(4)若 、
、 时,用
时,用 萃取
萃取 溶液,
溶液, (水相)
(水相)
 (有机相)的平衡常数
(有机相)的平衡常数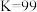 ,则用等体积的
,则用等体积的 一次性萃取
一次性萃取 溶液,
溶液, 萃取率为
萃取率为___________ (答案保留3位有效数字)
(5)“沉锌”时,可生成碱式碳酸锌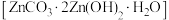 固体,请写出该反应的离子方程式
固体,请写出该反应的离子方程式_________________________________ 。
(6)锌可形成多种配合物。某种含锌配合物一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图1所示。请画出基态 的价电子排布图
的价电子排布图______________________ , 的配位数为
的配位数为___________ ;甘氨酸(如图2)易溶于水,原因是______________________ 。

 及少量
及少量 、
、 、
、 等)为原料制备氧化锌的工艺流程如下:
等)为原料制备氧化锌的工艺流程如下:
已知:用有机溶剂
 从水溶液中萃取A时,
从水溶液中萃取A时,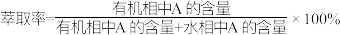
(1)为了提高酸浸效果,可采取的措施有
(2)“滤渣1”的主要成分除了
 还有
还有(3)“沉铁”操作时不能用
 代替
代替 ,原因是
,原因是(4)若
 、
、 时,用
时,用 萃取
萃取 溶液,
溶液, (水相)
(水相)
 (有机相)的平衡常数
(有机相)的平衡常数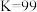 ,则用等体积的
,则用等体积的 一次性萃取
一次性萃取 溶液,
溶液, 萃取率为
萃取率为(5)“沉锌”时,可生成碱式碳酸锌
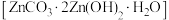 固体,请写出该反应的离子方程式
固体,请写出该反应的离子方程式(6)锌可形成多种配合物。某种含锌配合物一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图1所示。请画出基态
 的价电子排布图
的价电子排布图 的配位数为
的配位数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】用软锰矿(主要成分MnO2,含有SiO2、Fe2O3、Al2O3、MgCO3等杂质)制备MnSO4·H2O的流程如下:
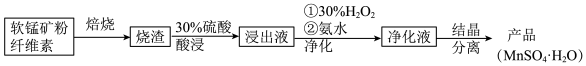
已知:MnO2不溶于酸
回答下列问题:
(1)Mn基态原子价态电子的电子排布图___________ ;周期表位置___________
(2)焙烧时,MnO2和Fe2O3在纤维素作用下分别转化为MnO、Fe3O4,则纤维素的作用是___________ 。酸浸时,浸出液的pH与锰的浸出率关系如下图所示:实际生产中,酸浸时控制硫酸的量不宜过多,使pH在2左右。请结合图示和制备硫酸锰的流程,说明硫酸的量不宜过多的原因:___________ 。
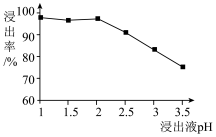
(3)净化时,加入30%H2O2的目的是(用离子方程式表示)___________ ;加氨水,调pH范围为是___________ 。
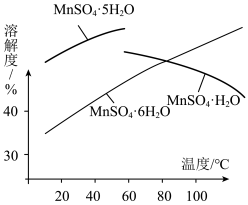
(4)结合MgSO4与MnSO4溶解度曲线,简述“结晶分离”的具体实验操作:___________ 。
(5)产品MnSO4·H2O(相对分子质量为169)纯度测定:称取a g产品,在适宜的条件下用适量NH4NO3将Mn2+氧化为Mn3+,再用0.1000 mol·L-1(NH4)2Fe(SO4)2溶液b mL刚好把Mn3+转化为Mn2+。通过计算可知产品纯度为___________ ,若滴定管洗涤时只用蒸馏水洗涤后直接使用,则所测产品纯度___________ 。(填偏大、偏小或无影响)

已知:MnO2不溶于酸
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.0 | 7.5 | 8.8 | 10.4 |
| 沉淀完全时的pH | 4.1 | 5.2 | 9.7 | 10.4 | 12.4 |
(1)Mn基态原子价态电子的电子排布图
(2)焙烧时,MnO2和Fe2O3在纤维素作用下分别转化为MnO、Fe3O4,则纤维素的作用是

(3)净化时,加入30%H2O2的目的是(用离子方程式表示)
(4)结合MgSO4与MnSO4溶解度曲线,简述“结晶分离”的具体实验操作:

(5)产品MnSO4·H2O(相对分子质量为169)纯度测定:称取a g产品,在适宜的条件下用适量NH4NO3将Mn2+氧化为Mn3+,再用0.1000 mol·L-1(NH4)2Fe(SO4)2溶液b mL刚好把Mn3+转化为Mn2+。通过计算可知产品纯度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】碳元素是形成单质及其化合物种类最多的元素。回答下列问题:
(1)碳元素是组成有机物必不可少的元素。1828年,化学家维勒首次用加热的方法将无机物氰酸铵 转化为有机物尿素,开启了人造有机物的大门。氰酸铵中阳离子的立体构型是
转化为有机物尿素,开启了人造有机物的大门。氰酸铵中阳离子的立体构型是_______ ,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式_______ (写出一种物质即可)
(2)石墨烯(图a)是一种由单层碳原子构成的平面结构新型导电材料,具有大π共轭体系。石墨烯中部分碳原子被氧化后,其平面结构发生改变,转化为氧化石量烯(图b)。

图a中,1号C的杂化方式为_______ ,图b中键角α_______ 键角β (填“>”、“<”或“=”);若将图b所示的氧化石墨烯分散在 中,则氧化石墨烯中可与
中,则氧化石墨烯中可与 形成氢键的原子有
形成氢键的原子有_______ (填元素符号)。
(3)丁二酮肟与 生成鲜红色丁二酮肟镍沉淀(如图①),该反应可用于检验
生成鲜红色丁二酮肟镍沉淀(如图①),该反应可用于检验 。丁二酮肟镍中存在的化学键有
。丁二酮肟镍中存在的化学键有_______ (标号)。
A.配位键 B.氢键 C.金属键 D.范德华力 E.共价键

(4)碳的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图②所示,则其化学式可表示为_______ 。
(5)碳和钨(W)组成一种晶体,其熔点为2870℃,硬度接近金刚石,其晶胞结构如图所示,则其化学式为_______ 。

(1)碳元素是组成有机物必不可少的元素。1828年,化学家维勒首次用加热的方法将无机物氰酸铵
 转化为有机物尿素,开启了人造有机物的大门。氰酸铵中阳离子的立体构型是
转化为有机物尿素,开启了人造有机物的大门。氰酸铵中阳离子的立体构型是 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式(2)石墨烯(图a)是一种由单层碳原子构成的平面结构新型导电材料,具有大π共轭体系。石墨烯中部分碳原子被氧化后,其平面结构发生改变,转化为氧化石量烯(图b)。

图a中,1号C的杂化方式为
 中,则氧化石墨烯中可与
中,则氧化石墨烯中可与 形成氢键的原子有
形成氢键的原子有(3)丁二酮肟与
 生成鲜红色丁二酮肟镍沉淀(如图①),该反应可用于检验
生成鲜红色丁二酮肟镍沉淀(如图①),该反应可用于检验 。丁二酮肟镍中存在的化学键有
。丁二酮肟镍中存在的化学键有A.配位键 B.氢键 C.金属键 D.范德华力 E.共价键

(4)碳的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图②所示,则其化学式可表示为
(5)碳和钨(W)组成一种晶体,其熔点为2870℃,硬度接近金刚石,其晶胞结构如图所示,则其化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】(1)基态Co原子的电子排布式为_______ 。
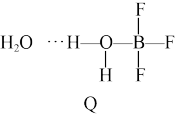
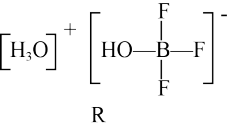
(2)BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:
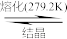
晶体Q中各种微粒间的作用力不涉及_______ (填序号)。
a.离子键 b.共价键 c. 配位键 d.金属键
(3)NaF和NaCl属于同一主族的钠盐,但NaF的硬度比NaCl大,原因是_______ 。
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为_______ 。
(5)第一电离能介于B、N之间的第二周期元素有_______ 种。S单质的常见形式为S8,其环状结构如图所示,该分子中S原子采用的轨道杂化方式是_______ 。
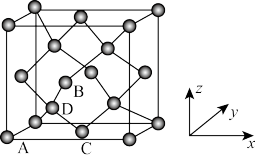
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,图为金刚石的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子坐标参数为
,0)。则D原子坐标参数为_______ 。②晶胞参数,描述晶胞的大小和形状,已知金刚石的晶胞参数a=356.89pm,其密度为_______ g•cm-3。(列出计算式即可,不必计算出结果)
(2)BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:


晶体Q中各种微粒间的作用力不涉及
a.离子键 b.共价键 c. 配位键 d.金属键
(3)NaF和NaCl属于同一主族的钠盐,但NaF的硬度比NaCl大,原因是
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
(5)第一电离能介于B、N之间的第二周期元素有

(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,图为金刚石的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子坐标参数为
,0)。则D原子坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】根据元素周期表中完整周期元素的性质,填写下列空白。
(1)在第三周期中,第一电离能最小的元素符号是________________ ,第一电离能最大的元素符号是________________ 。
(2)在元素周期表中,元素的电负性
________________ (填“大于”或“小于”,下同) ,第一电离能B
,第一电离能B________________  。
。
(3)第四周期元素中未成对电子数最多的元素符号是________________ ,其基态原子的简化电子排布式为________________ ,原子中所有电子占有________________ 个轨道,核外共有________________ 个不同运动状态的电子。
(4)杀虫剂 中阴离子的空间构型为
中阴离子的空间构型为________________ , 原子采取
原子采取________________ 杂化。
(5)某元素的正三价离子的 能级为半充满,其硫酸盐水溶液显
能级为半充满,其硫酸盐水溶液显________________ 性(填“酸”、“碱”或“中”),用离子方程式解释其原因________________ 。
(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为________________ 。电解一段时间后,阴极区
________________ (填“增大”、“减小”或“不变”)。
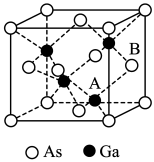
(7)原子晶体 的晶胞参数
的晶胞参数 ,它的晶胞结构如图所示。该晶胞内部存在的共价键数为
,它的晶胞结构如图所示。该晶胞内部存在的共价键数为________________ ;该晶胞的密度为________________  。(阿伏加德罗常数用
。(阿伏加德罗常数用 表示,已知Ga:70 As:75)。
表示,已知Ga:70 As:75)。
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,元素的电负性

 ,第一电离能B
,第一电离能B 。
。(3)第四周期元素中未成对电子数最多的元素符号是
(4)杀虫剂
 中阴离子的空间构型为
中阴离子的空间构型为 原子采取
原子采取(5)某元素的正三价离子的
 能级为半充满,其硫酸盐水溶液显
能级为半充满,其硫酸盐水溶液显(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为

(7)原子晶体
 的晶胞参数
的晶胞参数 ,它的晶胞结构如图所示。该晶胞内部存在的共价键数为
,它的晶胞结构如图所示。该晶胞内部存在的共价键数为 。(阿伏加德罗常数用
。(阿伏加德罗常数用 表示,已知Ga:70 As:75)。
表示,已知Ga:70 As:75)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】工业中可利用生产钛白的副产物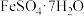 和硫铁矿
和硫铁矿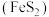 联合制备铁精粉
联合制备铁精粉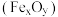 和硫酸,实现能源及资源的有效利用。
和硫酸,实现能源及资源的有效利用。
(1) 结构示意图如图1。
结构示意图如图1。

① 的价层电子排布式为
的价层电子排布式为___________ 。
② 中O和
中O和 中S均为
中S均为 杂化,比较
杂化,比较 中
中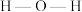 键角和
键角和 中
中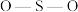 键角的大小并解释原因
键角的大小并解释原因___________ 。
③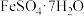 中
中 与
与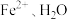 与
与 的作用力类型分别是
的作用力类型分别是___________ 。
(2) 晶体的晶胞形状为立方体,边长为
晶体的晶胞形状为立方体,边长为 ,结构如图2。
,结构如图2。

①距离 最近的阴离子有
最近的阴离子有___________ 个。
② 的摩尔质量为
的摩尔质量为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 。
。
该晶体的密度为___________  。
。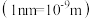
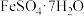 和硫铁矿
和硫铁矿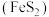 联合制备铁精粉
联合制备铁精粉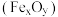 和硫酸,实现能源及资源的有效利用。
和硫酸,实现能源及资源的有效利用。(1)
 结构示意图如图1。
结构示意图如图1。
①
 的价层电子排布式为
的价层电子排布式为②
 中O和
中O和 中S均为
中S均为 杂化,比较
杂化,比较 中
中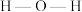 键角和
键角和 中
中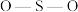 键角的大小并解释原因
键角的大小并解释原因③
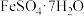 中
中 与
与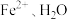 与
与 的作用力类型分别是
的作用力类型分别是(2)
 晶体的晶胞形状为立方体,边长为
晶体的晶胞形状为立方体,边长为 ,结构如图2。
,结构如图2。
①距离
 最近的阴离子有
最近的阴离子有②
 的摩尔质量为
的摩尔质量为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 。
。该晶体的密度为
 。
。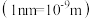
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】回答下列问题
(1)硼的研究在无机化学发展中占有独特的位置。硼元素有 和
和 两种天然稳定的同位素,在基态
两种天然稳定的同位素,在基态 原子中,核外存在
原子中,核外存在___________ 对自旋相反的电子,有___________ 种不同空间运动状态的电子,根据对角线规则硼元素许多性质与___________ 元素相似。
(2) 能与硼元素的某种氢化物作用得到化合物
能与硼元素的某种氢化物作用得到化合物 ,
, 是一种新的储氢材料,加热
是一种新的储氢材料,加热 会缓慢释放出
会缓慢释放出 ,并转化为化合物
,并转化为化合物 ,
, 、
、 分别与乙烷、乙烯的结构相似
分别与乙烷、乙烯的结构相似 的结构式为
的结构式为___________ , 分子中的
分子中的 键和
键和 键数目之比为
键数目之比为___________ 。
(3) 和
和 两种元素是自然界最常见的两种元素。均能与
两种元素是自然界最常见的两种元素。均能与 形成
形成 和
和 ,结构如图甲所示。请说明
,结构如图甲所示。请说明 略大于
略大于 的原因:
的原因:___________ 。
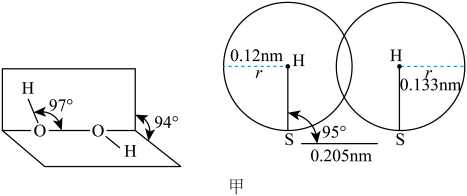
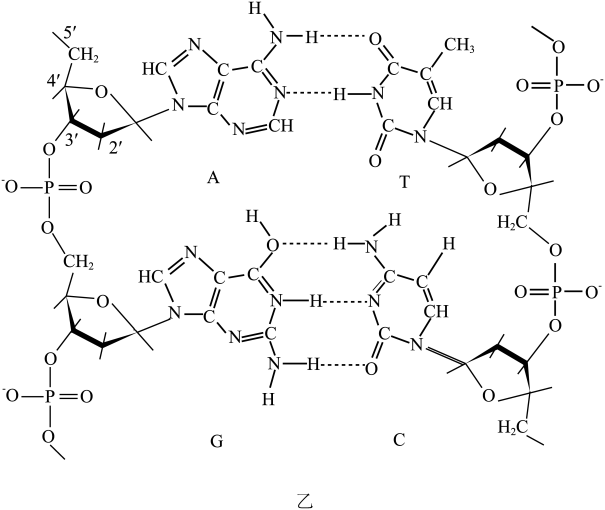
(4)图乙为DNA结构局部图。双链通过氢键使它们的碱基(A…T和C…G)相互配对形成双螺旋结构,请写出图中存在的两种氢键的表示式:___________ ;___________ 。
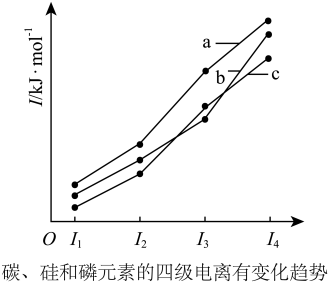
(5)如图表示碳、硅和磷元素的四级电离能变化趋势,其中表示碳的曲线是___________ (填标号)。
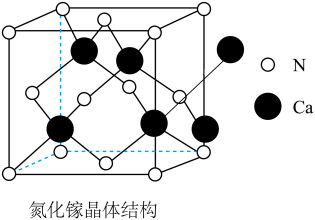
(6)氮化嫁(GaN)的晶体结构如图所示。晶体中N、Ga原子的轨道杂化类型分别为___________ 、___________ ,判断该晶体结构中存在配位键的依据是___________ 。
(1)硼的研究在无机化学发展中占有独特的位置。硼元素有
 和
和 两种天然稳定的同位素,在基态
两种天然稳定的同位素,在基态 原子中,核外存在
原子中,核外存在(2)
 能与硼元素的某种氢化物作用得到化合物
能与硼元素的某种氢化物作用得到化合物 ,
, 是一种新的储氢材料,加热
是一种新的储氢材料,加热 会缓慢释放出
会缓慢释放出 ,并转化为化合物
,并转化为化合物 ,
, 、
、 分别与乙烷、乙烯的结构相似
分别与乙烷、乙烯的结构相似 的结构式为
的结构式为 分子中的
分子中的 键和
键和 键数目之比为
键数目之比为(3)
 和
和 两种元素是自然界最常见的两种元素。均能与
两种元素是自然界最常见的两种元素。均能与 形成
形成 和
和 ,结构如图甲所示。请说明
,结构如图甲所示。请说明 略大于
略大于 的原因:
的原因:
(4)图乙为DNA结构局部图。双链通过氢键使它们的碱基(A…T和C…G)相互配对形成双螺旋结构,请写出图中存在的两种氢键的表示式:

(5)如图表示碳、硅和磷元素的四级电离能变化趋势,其中表示碳的曲线是

(6)氮化嫁(GaN)的晶体结构如图所示。晶体中N、Ga原子的轨道杂化类型分别为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】工业上制备纯碱的原理为:NaCl+CO2+NH3+H2O=NH4Cl+NaHCO3,请回答下列问题:
(1) 上述反应体系中出现的几种短周期元素中,第二周期元素原子半径由大到小的顺序是___________ 。
(2) 反应体系中出现的非金属元素,可形成多种化合物,其中和铵根离子空间构型相同,且属于有机物的电子式是___________ ,该分子为___________ (填“极性”或“非极性”)分子。
(3) 有人设想冰的晶胞也应该类似于金刚石,但实际较为复杂,可能是因为氢键较弱而导致饱和性和方向性,很难被严格执行,有文献报道,氨晶体中每个氢原子都形成氢键,则每个氨分子与周围___________ 个氨分子通过氢键相结合。
(4) 化合物FeF3熔点高于1000℃而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的原因可能是___________ 。
(5) 氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。
①FeO立方晶胞结构如图甲所示,则Fe2+的配位数为___________ ,与O2-紧邻的所有Fe2+构成的几何构型为___________ 。

②Cu2O立方晶胞结构如图乙所示,若O2-与Cu之间最近距离为a pm,则该晶体的密度为___________ g·cm-3.(用含a、NA的代数式表示,NA代表阿伏加德罗常数的值)
(1) 上述反应体系中出现的几种短周期元素中,第二周期元素原子半径由大到小的顺序是
(2) 反应体系中出现的非金属元素,可形成多种化合物,其中和铵根离子空间构型相同,且属于有机物的电子式是
(3) 有人设想冰的晶胞也应该类似于金刚石,但实际较为复杂,可能是因为氢键较弱而导致饱和性和方向性,很难被严格执行,有文献报道,氨晶体中每个氢原子都形成氢键,则每个氨分子与周围
(4) 化合物FeF3熔点高于1000℃而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的原因可能是
(5) 氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。
①FeO立方晶胞结构如图甲所示,则Fe2+的配位数为

②Cu2O立方晶胞结构如图乙所示,若O2-与Cu之间最近距离为a pm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】I.氟化镁钾(KMgF3)是一种具有优良光学性能的材料,其晶胞结构如图。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。

(1)KMgF3晶体中,每个Mg2+位于( )个距离最近的F-构成的( )空隙中。填选项字母______ 。
a.3 三角形 b.4 正四面体 c.6 正八面体 d.8 立方体
(2)Fe3+半径与Mg2+接近,将Mg2+部分由Fe3+取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
①基态Fe3+价电子的轨道表示式为______ 。
②某实验室合成新型催化剂材料KMg0.8Fe0.2F3O0.1(O2-是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为anm。若要合成厚度为0.3mm、面积为1m2的催化剂材料,理论上需要掺杂的Fe3+约为______ mol。(1nm=10-9m,1mm=10-3m,阿伏加德罗常数取6×1023mol-1)。
(3)AthMn(N3)3晶体结构与KMgF3类似。已知Ath+与N 的结构简式如图:
的结构简式如图:
Ath+: N
N :
: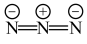
①Ath+中N原子的杂化方式为_______ ,N 中心N原子的杂化方式为
中心N原子的杂化方式为_______ 。
②Ath+的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的Mn2+与N 还存在着
还存在着______ ,上述相互作用不会随Ath+的转动改变。
Ⅱ.钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图及Co的晶胞俯视投影图如图。晶体中O围绕Co形成八面体,八面体共棱形成层状空间结构,与Li+层交替排列。在充放电过程中,Li+在层间脱出或嵌入。
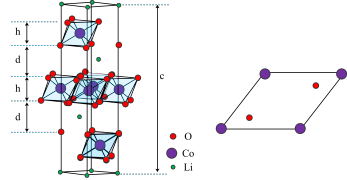
(4)基态Co原子中未成对的电子数为______ 。
(5)该晶胞中O的个数为______ 。
(6)Li+在______ (填“充电”或“放电”)过程中会从八面体层间脱出。该过程会导致晶胞高度c变大,解释原因:_______ 。

(1)KMgF3晶体中,每个Mg2+位于( )个距离最近的F-构成的( )空隙中。填选项字母
a.3 三角形 b.4 正四面体 c.6 正八面体 d.8 立方体
(2)Fe3+半径与Mg2+接近,将Mg2+部分由Fe3+取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
①基态Fe3+价电子的轨道表示式为
②某实验室合成新型催化剂材料KMg0.8Fe0.2F3O0.1(O2-是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为anm。若要合成厚度为0.3mm、面积为1m2的催化剂材料,理论上需要掺杂的Fe3+约为
(3)AthMn(N3)3晶体结构与KMgF3类似。已知Ath+与N
 的结构简式如图:
的结构简式如图:Ath+:
 N
N :
: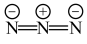
①Ath+中N原子的杂化方式为
 中心N原子的杂化方式为
中心N原子的杂化方式为②Ath+的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的Mn2+与N
 还存在着
还存在着Ⅱ.钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图及Co的晶胞俯视投影图如图。晶体中O围绕Co形成八面体,八面体共棱形成层状空间结构,与Li+层交替排列。在充放电过程中,Li+在层间脱出或嵌入。

(4)基态Co原子中未成对的电子数为
(5)该晶胞中O的个数为
(6)Li+在
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】A、B、C、D、E、F、G是原子序数依次增大的前四周期元素,A的某种原子无中子,B的最外层有3个成单电子,C与A可形成1:1和1:2的化合物且常温下呈液体,D的原子半径是短周期中最大的,F的最高价氧化物对应水化物是最强的含氧酸,C和E形成的氧化物有两性,G的最高能层符号为N, 且其内层的d轨道电子数与最外层电子数相等。
(1)G原子的价电子排布式为_____________ 。
(2)BA3的VSEPR模型为_____________ 。
(3)离子半径C2->D+,原因是_____________ 。
(4)E与F形成的化合物EF3 在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为_____________ (标明配位键),其中该蒸气分子中E原子的杂化方式为_________ 。
(5)A、B、C三种元素可形成盐,则在形成的盐中存在的作用力有_____________ 。
(6)图甲是G单质的堆积方式,该堆积方式为__________ 堆积;GC2·H2O可通过CF4水解来制备,则该制备过程的化学方程式为_____________ 。
(7)A、D、E可形成化合物DEA4 ,在DEA4晶体中,与D+紧邻且等距的EA4-有_____ 个;DEA4晶体的密度为_____________ g/cm3(用含a的代数式表示)。若DEA4晶胞上下底心处的D+被Li+取代,得到的晶体为__________ (填化学式)。

(1)G原子的价电子排布式为
(2)BA3的VSEPR模型为
(3)离子半径C2->D+,原因是
(4)E与F形成的化合物EF3 在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为
(5)A、B、C三种元素可形成盐,则在形成的盐中存在的作用力有
(6)图甲是G单质的堆积方式,该堆积方式为
(7)A、D、E可形成化合物DEA4 ,在DEA4晶体中,与D+紧邻且等距的EA4-有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】金属钨是重要的战略资源,由黑钨矿(主要成分为 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:

已知:常温下钨酸( )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。
回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第_____ 族。
(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先_____ ,“碱熔”过程 发生反应的化学方程式为
发生反应的化学方程式为_____ 。
(3)上述流程中加盐酸中和至 时,溶液中的杂质阴离子有
时,溶液中的杂质阴离子有 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为_____ 。
(4)沉钨过程中,判断 是否沉淀完全的方法是
是否沉淀完全的方法是_____ 。
(5)钨酸钙( ))和氢氧化钙都是微溶电解质。某温度下
))和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中,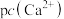 与pc(阴离子)的关系如图所示,已知:pc(离子)
与pc(阴离子)的关系如图所示,已知:pc(离子) (离子)。该温度下将
(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数
_____ 。

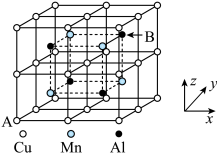
(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。该合金的化学式为_____ 。若A原子的坐标参数为 ,则B原子的坐标参数为
,则B原子的坐标参数为_____ 。
 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:
已知:常温下钨酸(
 )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第
(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先
 发生反应的化学方程式为
发生反应的化学方程式为(3)上述流程中加盐酸中和至
 时,溶液中的杂质阴离子有
时,溶液中的杂质阴离子有 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为(4)沉钨过程中,判断
 是否沉淀完全的方法是
是否沉淀完全的方法是(5)钨酸钙(
 ))和氢氧化钙都是微溶电解质。某温度下
))和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中,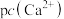 与pc(阴离子)的关系如图所示,已知:pc(离子)
与pc(阴离子)的关系如图所示,已知:pc(离子) (离子)。该温度下将
(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数

(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。该合金的化学式为
 ,则B原子的坐标参数为
,则B原子的坐标参数为
您最近一年使用:0次



