物质的组成与结构决定了物质的性质与变化。请回答下列问题:
(1)C、H、N、O四种元素中电负性最大的是____ (填元素符号),写出Fe2+的最外层电子排布式____ 。
(2)根据等电子原理,写出CN-的电子式___ ,CNO-中心原子的杂化方式为 ________ 。
(3)MgO、CaO两种晶体的结构与NaCl晶体结构相似,则两种离子晶体的熔点由高到低顺序是___ (用化学式表示),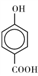 的沸点比
的沸点比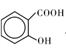
____ (填“高”或“低”);原因是______________________ .
(4)铁有δ、γ、α三种同素异形体,如下图所示。
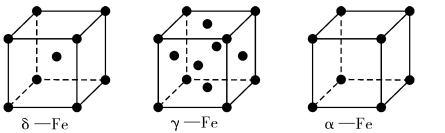
γ -Fe晶体的一个晶胞中所含有的铁原子数为____ ,δ一Fe、α- Fe两种晶胞中铁原子的配位数之比为____ 。已知δ-Fe晶体的密度为dg/cm3,NA表示阿伏伽德罗常数的数值,则Fe原子半径为____ pm(列表达式)。
(1)C、H、N、O四种元素中电负性最大的是
(2)根据等电子原理,写出CN-的电子式
(3)MgO、CaO两种晶体的结构与NaCl晶体结构相似,则两种离子晶体的熔点由高到低顺序是
 的沸点比
的沸点比
(4)铁有δ、γ、α三种同素异形体,如下图所示。

γ -Fe晶体的一个晶胞中所含有的铁原子数为
更新时间:2017-06-05 01:55:28
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】硼的化合物有重要应用。
(1)写出基态B的电子排布式___________ 。
(2)硼酸 的结构如图所示。在水溶液中硼酸的电离方程式:
的结构如图所示。在水溶液中硼酸的电离方程式: ,25℃时
,25℃时 。
。
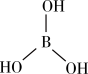
①将“ ”视为一个原子,硼酸分子的空间结构名称为
”视为一个原子,硼酸分子的空间结构名称为___________ 。
② 中,
中, 原子的杂化轨道类型为
原子的杂化轨道类型为___________ ;其中一条 键是配位键,电子对由
键是配位键,电子对由___________ 原子提供。
(3)硼砂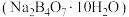 在水溶液中可以解离出等物质的量浓度的
在水溶液中可以解离出等物质的量浓度的 和
和 ,该溶液在一定温度下具有固定的pH,可作为校准pH计的标准溶液。计算常温下
,该溶液在一定温度下具有固定的pH,可作为校准pH计的标准溶液。计算常温下 硼砂溶液的
硼砂溶液的
___________ 。
(4)氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储攽材料。
含氢量高、热稳定性好,是一种具有潜力的固体储攽材料。
①氨硼烷中N为-3价,B为+3价。H、B、N的电负性由大到小依次为___________ 。
②氨硼烷在催化剂作用下水解释放氢气,用单线桥表示该反应的电子转移。

___________
③氨硼烷分子间存在“双氢键”使氨硼烷的熔点明显升高。“双氢键”能形成的原因是___________ 。
(1)写出基态B的电子排布式
(2)硼酸
 的结构如图所示。在水溶液中硼酸的电离方程式:
的结构如图所示。在水溶液中硼酸的电离方程式: ,25℃时
,25℃时 。
。
①将“
 ”视为一个原子,硼酸分子的空间结构名称为
”视为一个原子,硼酸分子的空间结构名称为②
 中,
中, 原子的杂化轨道类型为
原子的杂化轨道类型为 键是配位键,电子对由
键是配位键,电子对由(3)硼砂
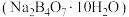 在水溶液中可以解离出等物质的量浓度的
在水溶液中可以解离出等物质的量浓度的 和
和 ,该溶液在一定温度下具有固定的pH,可作为校准pH计的标准溶液。计算常温下
,该溶液在一定温度下具有固定的pH,可作为校准pH计的标准溶液。计算常温下 硼砂溶液的
硼砂溶液的
(4)氨硼烷
 含氢量高、热稳定性好,是一种具有潜力的固体储攽材料。
含氢量高、热稳定性好,是一种具有潜力的固体储攽材料。①氨硼烷中N为-3价,B为+3价。H、B、N的电负性由大到小依次为
②氨硼烷在催化剂作用下水解释放氢气,用单线桥表示该反应的电子转移。

③氨硼烷分子间存在“双氢键”使氨硼烷的熔点明显升高。“双氢键”能形成的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表所列是A、B、C、D、E五种短周期元素的相关数据:
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是________ 。
A.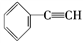 B.CH4
B.CH4
C.CH2==CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键:____________ 。
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是______ (化学式),理由是____ 。
(4)B、D形成的氢化物沸点:________ 更高,热稳定性________ 更强。(写化学式)
| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
A.
 B.CH4
B.CH4 C.CH2==CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键:
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是
(4)B、D形成的氢化物沸点:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.国产C919大型客机的正式下线,标志着我国航空工业进入了新的发展阶段,我国成为世界上少数几个具有自行研制大型飞机的国家之一。
(1)飞机的外壳通常采用镁一铝合金材料,铝的价电子排布图为_______________ ,第一电离能:铝________ (填“大于”或“小于”)镁。
(2)为了减轻质量而不减轻外壳承压能力,现代飞机通常采用复合材料一玻璃纤维增强塑料,其成分之一为环氧树脂,常见的E51型环氧树脂中部分结构如图甲所示,其中碳原子的杂化方式为___________ ,该材料此部分中所含元素的电负性从小到大的顺序为_______________ 。

II.大型飞机的发动机在制造过程中通常采用碳化钨做关键部位的材料。
(1)钨元素位于周期表的第六周期第VIB族,请写出其位于同一族的元素铬的原子的价电子排布式__________________ ,
(2)图乙为碳化钨晶体的一部分结构,碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有_______ 个,1个钨原子周围距离钨原子最近的碳原子有_______ 个,下列金属元素的堆积方式与碳化钨晶胞中碳原子和钨原子所处位置类似的是___________ (填序号)。
A.Fe Cu B.Ti Au C.Mg Zn D.Cu Ag
(4)设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g/mol,密度为b g/cm3,则阿伏伽德罗常数NA用上述数据可以表示为____________________ 。
(1)飞机的外壳通常采用镁一铝合金材料,铝的价电子排布图为
(2)为了减轻质量而不减轻外壳承压能力,现代飞机通常采用复合材料一玻璃纤维增强塑料,其成分之一为环氧树脂,常见的E51型环氧树脂中部分结构如图甲所示,其中碳原子的杂化方式为

II.大型飞机的发动机在制造过程中通常采用碳化钨做关键部位的材料。
(1)钨元素位于周期表的第六周期第VIB族,请写出其位于同一族的元素铬的原子的价电子排布式
(2)图乙为碳化钨晶体的一部分结构,碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有
A.Fe Cu B.Ti Au C.Mg Zn D.Cu Ag
(4)设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g/mol,密度为b g/cm3,则阿伏伽德罗常数NA用上述数据可以表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态Fe2+与Fe3+离子中未成对的电子数之比为______ 。
(2)钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,基态Ti原子的核外电子排布式为____________ 。
(3)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。Fe基态核外电子排布式为___________ ;
(4)钙和铜合金可用作电解制钙的阴极电极材料,基态铜原子的价电子排布式为________ 。
(5)基态Sn原子价层电子的空间运动状态有___ 种,基态氧原子的价层电子排布式不能表示为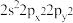 ,因为这违背了
,因为这违背了____ 原理(规则)。
(2)钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,基态Ti原子的核外电子排布式为
(3)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。Fe基态核外电子排布式为
(4)钙和铜合金可用作电解制钙的阴极电极材料,基态铜原子的价电子排布式为
(5)基态Sn原子价层电子的空间运动状态有
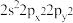 ,因为这违背了
,因为这违背了
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为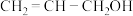 。请回答下列问题:
。请回答下列问题:
①基态镍原子的价电子排布式为___________ 。
② 中含
中含___________  键,烯丙醇分子中碳原子的杂化类型是
键,烯丙醇分子中碳原子的杂化类型是___________ 。
(2)乙炔是有机合成的一种重要原料。实验室可用 与水反应得到乙炔。
与水反应得到乙炔。
①将乙炔通入 溶液中生成
溶液中生成 红棕色沉淀。基态
红棕色沉淀。基态 的核外电子排布式为
的核外电子排布式为___________ 。
②乙炔与 反应可得丙烯腈
反应可得丙烯腈 ,丙烯腈分子中碳原子的杂化轨道类型是
,丙烯腈分子中碳原子的杂化轨道类型是___________ ,分子中含有 键的数目为
键的数目为___________ 。
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为
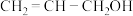 。请回答下列问题:
。请回答下列问题:①基态镍原子的价电子排布式为
②
 中含
中含 键,烯丙醇分子中碳原子的杂化类型是
键,烯丙醇分子中碳原子的杂化类型是(2)乙炔是有机合成的一种重要原料。实验室可用
 与水反应得到乙炔。
与水反应得到乙炔。①将乙炔通入
 溶液中生成
溶液中生成 红棕色沉淀。基态
红棕色沉淀。基态 的核外电子排布式为
的核外电子排布式为②乙炔与
 反应可得丙烯腈
反应可得丙烯腈 ,丙烯腈分子中碳原子的杂化轨道类型是
,丙烯腈分子中碳原子的杂化轨道类型是 键的数目为
键的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铝及其化合物广泛应用于金属冶炼、有机合成等领域。
⑴铝热反应可以冶炼金属铬,Cr基态核外电子排布式为_______ 。
⑵已知反应:
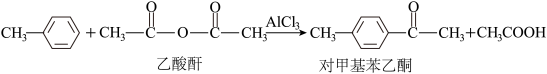
①乙酸酐分子中碳原子轨道的杂化类型为______ 。
②1 mol对甲基苯乙酮分子中含有的σ键的数目为_____ 。
③甲苯分子难溶于水的原因是______ 。
④单个AlCl3气态分子的空间构型为______ ,AlCl3可与Cl-形成AlCl ,与AlCl
,与AlCl 互为等电子体的分子为
互为等电子体的分子为______ 。
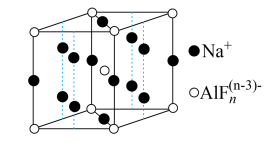
(3)某遮光剂的晶胞如右图所示,则n=______ 。
⑴铝热反应可以冶炼金属铬,Cr基态核外电子排布式为
⑵已知反应:

①乙酸酐分子中碳原子轨道的杂化类型为
②1 mol对甲基苯乙酮分子中含有的σ键的数目为
③甲苯分子难溶于水的原因是
④单个AlCl3气态分子的空间构型为
 ,与AlCl
,与AlCl 互为等电子体的分子为
互为等电子体的分子为(3)某遮光剂的晶胞如右图所示,则n=

您最近一年使用:0次
【推荐1】物质结构揭示物质构成的奥秘,请回答以下问题:
(1)元素A含有8个质子,10个中子的核素,用核素符号表示为______ 。元素B被科学家称“防癌之王”,与元素A同主族位于第四周期,元素B的名称为______ ,A和B的氢化物,沸点较高的是_____ (填化学式)。
(2)CH4中共用电子对偏向C,SiH4中硅元素为+4价,则C、Si、H的电负性由大到小的顺序为______ 。
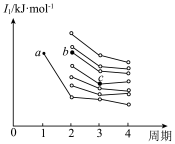
(3)如图是前四周期主族元素第一电离能梯度图,图中a点对应的元素为氢,则b点对应元素的未成对电子数为______ ,c点对应元素基态原子价电子排布式为_______ 。
(4)FeC13晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因是____ 。
(5)水果中含有不同的果酸,其中柠檬、柑橘等水果中含有柠檬酸,柠檬酸的结构如下图。柠檬酸的晶体类型为_____ ,碳原子的杂化轨道类型为_____ ;柠檬酸晶体中含有的作用力有___________ 。

(1)元素A含有8个质子,10个中子的核素,用核素符号表示为
(2)CH4中共用电子对偏向C,SiH4中硅元素为+4价,则C、Si、H的电负性由大到小的顺序为
(3)如图是前四周期主族元素第一电离能梯度图,图中a点对应的元素为氢,则b点对应元素的未成对电子数为

(4)FeC13晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因是
(5)水果中含有不同的果酸,其中柠檬、柑橘等水果中含有柠檬酸,柠檬酸的结构如下图。柠檬酸的晶体类型为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】应用:判断金属性、非金属性强弱
判断依据:
(1)一般大于1.8:元素为非金属元素,且电负性越大,非金属性越___________ 。
(2)一般小于1.8:元素为金属元素,且电负性越小,金属性越___________ 。
(3)1.8左右:一般位于金属元素和非金属元素的交界线处,它们既有___________ 性,又有___________ 性。
判断依据:
(1)一般大于1.8:元素为非金属元素,且电负性越大,非金属性越
(2)一般小于1.8:元素为金属元素,且电负性越小,金属性越
(3)1.8左右:一般位于金属元素和非金属元素的交界线处,它们既有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】材料是人类文明进步的阶梯,主族非金属元素是组成特殊材料的重要元素。请回答下列问题:
(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是_____ ,第一电离能从大到小的顺序是_____ 。
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是______ (填化学式);已知等电子体具有相同的空间构型,结合价电子对互斥理论可知N2O分子为______ 形。
(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是_____ (填符号);配合物T与[M(NH3)5(H2O)]Cl3组成所含微粒种类和数目相同,中心离子的配位数相同且T中也只有两种配体,若1molT溶于水,加入足量AgNO3溶液只生成2molAgCl,则T的配合物可表示为_____ 。
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为_____ 。

(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO
 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1) CH3COO[Cu(NH3)2]中C原子轨道的杂化类型是____ 。与NH3分子互为等电子体的阴离子为____ 。
(2) 乳酸分子(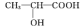 )中C原子的杂化类型为
)中C原子的杂化类型为____ 。与 互为等电子体的一种分子化学式为
互为等电子体的一种分子化学式为_____ 。
(3) 的空间构型为
的空间构型为________ (用文字描述);NaNT可由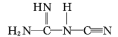 (双聚氰胺)为原料制备。双聚氰胺中碳原子杂化轨道类型为
(双聚氰胺)为原料制备。双聚氰胺中碳原子杂化轨道类型为________ 。
(4)草酸(HOOCCOOH)分子中碳原子轨道的杂化类型是____ ;与SiF4互为等电子体的阴离子的化学式为_______ 。
(5) 中N原子轨道的杂化类型是
中N原子轨道的杂化类型是___ 。与 互为等电子体的一种分子为
互为等电子体的一种分子为__ (填化学式)。
(6)苯甲醇(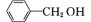 )中碳原子的杂化轨道类型为
)中碳原子的杂化轨道类型为______ 。与 互为等电子体的阳离子为
互为等电子体的阳离子为______ (填化学式), 离子的空间构型为(用文字描述)
离子的空间构型为(用文字描述)________ 。
(2) 乳酸分子(
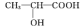 )中C原子的杂化类型为
)中C原子的杂化类型为 互为等电子体的一种分子化学式为
互为等电子体的一种分子化学式为(3)
 的空间构型为
的空间构型为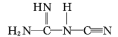 (双聚氰胺)为原料制备。双聚氰胺中碳原子杂化轨道类型为
(双聚氰胺)为原料制备。双聚氰胺中碳原子杂化轨道类型为(4)草酸(HOOCCOOH)分子中碳原子轨道的杂化类型是
(5)
 中N原子轨道的杂化类型是
中N原子轨道的杂化类型是 互为等电子体的一种分子为
互为等电子体的一种分子为(6)苯甲醇(
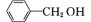 )中碳原子的杂化轨道类型为
)中碳原子的杂化轨道类型为 互为等电子体的阳离子为
互为等电子体的阳离子为 离子的空间构型为(用文字描述)
离子的空间构型为(用文字描述)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空。
(1)已知NaN3中的 阴离子与CO2结构相似,写出NaN3的电子式
阴离子与CO2结构相似,写出NaN3的电子式_______ 。
(2)甲酸能发生双分子缔合,导致其沸点(101℃)比相对分子质量相等的乙醇(78.4℃)更高,写出八元环状的甲酸二缔合体的结构式_______ 。
(3)四种晶体的熔点数据如下表:
其中, 与另外三种晶体的熔点相差较大,原因是
与另外三种晶体的熔点相差较大,原因是_______ 。
(1)已知NaN3中的
 阴离子与CO2结构相似,写出NaN3的电子式
阴离子与CO2结构相似,写出NaN3的电子式(2)甲酸能发生双分子缔合,导致其沸点(101℃)比相对分子质量相等的乙醇(78.4℃)更高,写出八元环状的甲酸二缔合体的结构式
(3)四种晶体的熔点数据如下表:
| 物质 | SiC |  |  |  |
| 熔点/℃ | 2730 | 1900 | 1723 | -90 |
其中,
 与另外三种晶体的熔点相差较大,原因是
与另外三种晶体的熔点相差较大,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的排列顺序为_______________ 。
(2)根据等电子体原理,NO2+中氮原子的轨道杂化类型是__________ ;1molO22+中含有的π键数目为__________________ 个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。基态Cr3+核外电子排布式为______________ 。
(4)下列物质的分子与O3分子的结构最相似的是_____________ (填选项字母)
A. H2O B. CO2
C. SO2 D. BeCl2
(5)固体二氧化碳外形似冰,受热气化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:干冰中1个分子周围有____________ 个紧邻分子。
(6)BF3与一定量的水形成(H2O)2 • BF3晶体Q,Q在一定条件下可转化为R:
① 晶体Q中各种微粒间的作用力有___________________ (填选项字母)。
a.范德华力 b.非极性共价键 c.配位键 d.极性共价键 e.氢键
② R中阳离子的空间构型为___________ ,阴离子的中心原子轨道采用___________ 杂化。
(1)氮、氧、氟元素的第一电离能从大到小的排列顺序为
(2)根据等电子体原理,NO2+中氮原子的轨道杂化类型是
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。基态Cr3+核外电子排布式为
(4)下列物质的分子与O3分子的结构最相似的是
A. H2O B. CO2
C. SO2 D. BeCl2
(5)固体二氧化碳外形似冰,受热气化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:干冰中1个分子周围有
(6)BF3与一定量的水形成(H2O)2 • BF3晶体Q,Q在一定条件下可转化为R:

① 晶体Q中各种微粒间的作用力有
a.范德华力 b.非极性共价键 c.配位键 d.极性共价键 e.氢键
② R中阳离子的空间构型为
您最近一年使用:0次



