下表是元素周期表前四周期的一部分,X、Y、Z、R、Q、W、J是7种元素的代号。回答下列问题时,涉及元素书写的请用相应的元素符号。

(1)J基态原子的核外电子排布式为________ 。基态Q2+中未成对电子数为________ ;R和Y的简单离子与Na+半径大小顺序为________ 。
(2)X、Y、Z三种元素电负性由大到小的排序是________ ;X与Y的第一电离能:X________ (填“>”“<”或“=”)Y,其理由是________ 。
(3)检验某溶液中是否含有Q3+的方法是_____________________________ 。
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为________________ 。

(1)J基态原子的核外电子排布式为
(2)X、Y、Z三种元素电负性由大到小的排序是
(3)检验某溶液中是否含有Q3+的方法是
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为
更新时间:2018-02-11 21:57:55
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】W、X、Y、Z是短周期元素,其部分性质如表:
(1)X的简单氢化物的结构式_____ ,Y和W形成的化合物YW2的电子式_____ 。
(2)元素Z在周期表中的位置_____ 。
(3)比较X、Y最高价氧化物对应的水化物的酸性:_____ >_____ (填化学式)。
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的 |
| Z | 第三周期简单离子半径最小 |
(2)元素Z在周期表中的位置
(3)比较X、Y最高价氧化物对应的水化物的酸性:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
I.乳酸(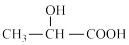 )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。
(1)在生活中,常选择上述物质中_______________ (填结构简式)清洗水壶里的水垢。
(2)生活中常选择_______________ 酒精 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水” 皮肤消毒。
皮肤消毒。
(3)上述物质中,属于天然高分子化合物的是_________________  填名称
填名称 。
。
(4)乳酸中发生如下变化: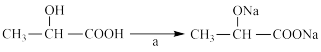 ,则所用的试剂a为
,则所用的试剂a为________ (写化学式)。
II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
(5)X在元素周期表中的位置为___________ ;Y元素的名称为________________ 。
(6)元素W的离子结构示意图是_______________ ;Z、Y形成的化合物为____________ (用化学式表示)。
I.乳酸(
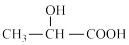 )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。(1)在生活中,常选择上述物质中
(2)生活中常选择
 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水” 皮肤消毒。
皮肤消毒。(3)上述物质中,属于天然高分子化合物的是
 填名称
填名称 。
。(4)乳酸中发生如下变化:
 ,则所用的试剂a为
,则所用的试剂a为II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最外层电子数是次外层的2倍 |
| Y | M层上的电子数是K层的3倍 |
| Z | Z的一种核素的质量数为53,中子数为34 |
| W | W2+与氖原子具有相同核外电子排布 |
(5)X在元素周期表中的位置为
(6)元素W的离子结构示意图是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.物质的分类、氧化还原反应原理可以帮助我们推测物质的性质以及反应的产物。已知:元素铬(Cr)的几种化合物存在如图转化关系,回答相关问题:

(1)写出反应①中发生的化学反应方程式___________ 。
(2)反应②中H2O2做___________ 剂。
(3)已知K2Cr2O7的氧化性大于MnO2,K2Cr2O7溶液___________ (填“能”或“不能”)与浓盐酸反应制取Cl2。
Ⅱ.物质的量是联系宏观和微观的桥梁。
(4)标准状况下,与9.6gCH4所含氢原子数相同的NH3的体积约为___________ L。
(5)6.8g某二价金属氯化物(MCl2)含3.55gCl-。则该金属原子的摩尔质量为___________ 。
(6)8gFe2O3和CuO组成的混合物全部溶于300mL物质的量浓度为0.1mol·L-1的硫酸中,反应后向所得溶液中加入20mLNaOH溶液,恰好使Fe3+和Cu2+完全沉淀,则氢氧化钠溶液的物质的量浓度为___________ mol·L-1。
Ⅲ.人类对原子结构的认识是研究物质微观结构的重要方面。
(7)已知X、Y、Z、W四种元素中,X元素的某种粒子只有一个质子;Y元素原子最外电子数是内层电子数的3倍;Z元素原子K层和M层电子总数等于其L层电子数;W元素原子最外层有1个电子,其阳离子与Y的阴离子具有相同电子层结构。
①含X、Y、Z、W四种元素的化合物的化学式为___________ 。
②ZY2与足量WYX溶液反应的化学方程式为___________ 。

(1)写出反应①中发生的化学反应方程式
(2)反应②中H2O2做
(3)已知K2Cr2O7的氧化性大于MnO2,K2Cr2O7溶液
Ⅱ.物质的量是联系宏观和微观的桥梁。
(4)标准状况下,与9.6gCH4所含氢原子数相同的NH3的体积约为
(5)6.8g某二价金属氯化物(MCl2)含3.55gCl-。则该金属原子的摩尔质量为
(6)8gFe2O3和CuO组成的混合物全部溶于300mL物质的量浓度为0.1mol·L-1的硫酸中,反应后向所得溶液中加入20mLNaOH溶液,恰好使Fe3+和Cu2+完全沉淀,则氢氧化钠溶液的物质的量浓度为
Ⅲ.人类对原子结构的认识是研究物质微观结构的重要方面。
(7)已知X、Y、Z、W四种元素中,X元素的某种粒子只有一个质子;Y元素原子最外电子数是内层电子数的3倍;Z元素原子K层和M层电子总数等于其L层电子数;W元素原子最外层有1个电子,其阳离子与Y的阴离子具有相同电子层结构。
①含X、Y、Z、W四种元素的化合物的化学式为
②ZY2与足量WYX溶液反应的化学方程式为
您最近一年使用:0次
【推荐1】已知X、Y、Z、W、Q、R六种元素中,原子序数依次增大,其结构或性质信息如表。
请根据信息回答有关问题:
(1)元素X原子核外共有____________ 种不同运动状态的电子。
(2)元素X、Y的第一电离能较大的是___________ (填元素符号)。
(3)元素X、Y、Z的电负性最小的是___________ (填元素名称)。
(4)元素W的基态原子核外电子排布式为___________
(5)元素Q在周期表中位置为___________ ,元素R基态原子的价电子排布式为___________ 。
| 元素 | 结构或性质信息 |
| X | 基态原子的最外层电子排布式为nsnnpn+1 |
| Y | 基态原子的L层上有2个未成对的p电子 |
| Z | 基态原子的M层上s、p电子个数相等 |
| W | 位于第4周期ⅥB族 |
| Q | 元素的正三价离子的3d能级半充满 |
| R | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
请根据信息回答有关问题:
(1)元素X原子核外共有
(2)元素X、Y的第一电离能较大的是
(3)元素X、Y、Z的电负性最小的是
(4)元素W的基态原子核外电子排布式为
(5)元素Q在周期表中位置为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)如图是某同学画出CO分子中氧原子的核外电子排布图,请判断该排布图:___ (填“正确”或“错误”),理由是___ (若判断正确,该空不用回答)。

(2)基态Fe2+的价电子排布式为___ ;Ti原子核外共有___ 种运动状态不同的电子。
(3)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)___ 。
(4)元素X与铁同周期,X元素原子核外未成对电子数最多,X为___ (填元素符号)X的基态原子的电子排布式为___ 。
(5)乙醇的沸点明显高于乙醛,其主要原因为____ 。
(6)Fe(CO)x的核外电子数之和为96,则x=___ 。
(1)如图是某同学画出CO分子中氧原子的核外电子排布图,请判断该排布图:

(2)基态Fe2+的价电子排布式为
(3)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)
(4)元素X与铁同周期,X元素原子核外未成对电子数最多,X为
(5)乙醇的沸点明显高于乙醛,其主要原因为
(6)Fe(CO)x的核外电子数之和为96,则x=
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)下列各组多电子原子的能级能量比较不正确的是_______
①2p=3p ②4s>2s ③4p>4f ④4d>3d
(2)Fe3+与Fe2+的离子半径大小关系为Fe3+_______ Fe2+(填“大于”或“小于”)
(3)C、N、O三种元素的第一电离能有大到小的排序为_______
(4)[Ni(NH3)6]SO4中配位数为_______ ,配位原子为_______ 。
(5)1molCH3COOH分子中含有σ键的为_______ mol。
(1)下列各组多电子原子的能级能量比较不正确的是_______
①2p=3p ②4s>2s ③4p>4f ④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
(3)C、N、O三种元素的第一电离能有大到小的排序为
(4)[Ni(NH3)6]SO4中配位数为
(5)1molCH3COOH分子中含有σ键的为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】氧族元素的单质及其化合物是一类重要物质,请回答下列问题。
⑴基态硒(Se)原子的价层电子排布式为____________ 。
⑵OCN-中所含三种元素的电负性从大到小的顺序为________ (用元素符号表示,下同);第一电离能从大到小的顺序为________ 。已知等电子体具有相同的空间构型,则OCN-的空间构型为_______ 。
⑶H2O2分子中氧原子的轨道杂化类型是__________ ;H2O的沸点明显高于H2Se的沸点( 42℃),其主要原因是
42℃),其主要原因是_______________ 。
⑷硒化锌的晶胞结构如图所示,则硒化锌的化学式为_________ ,其中Zn(黑球)的配位数为______ 。

⑴基态硒(Se)原子的价层电子排布式为
⑵OCN-中所含三种元素的电负性从大到小的顺序为
⑶H2O2分子中氧原子的轨道杂化类型是
 42℃),其主要原因是
42℃),其主要原因是⑷硒化锌的晶胞结构如图所示,则硒化锌的化学式为

您最近一年使用:0次
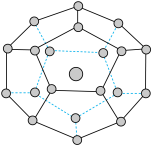
【推荐2】2017年5月海底天然气水合物(俗称可燃冰)试采成功,这是我国能源开发的一次历史性突破。一定条件下,CH4和CO2都能与H2O形成如图所示的笼状结构(表面的小球是水分子,内部的大球是CH4分子或CO2分子;“可燃冰”是CH4与H2O形成的水合物),其相关参数见下表。
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子的空间结构为___________ 。
(3)为开采海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为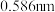 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(4)“可燃冰”中分子间存在的作用力是氢键和___________ ,上图中最小的环中连接的原子总数是___________ 。
| 参数分子 | 分子直径/nm | 分子与H2O的结合能E(kJ·mol-1) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为
(2)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为(3)为开采海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为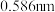 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是(4)“可燃冰”中分子间存在的作用力是氢键和
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】卤族元素能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
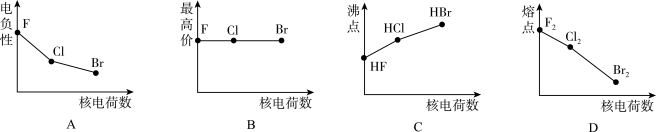
(1)下面曲线(图1)表示卤族元素某种性质随核电荷数的变化趋势。正确的是___ 。
(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子的电子式为___ 。
(3)F2与其他卤素单质反应可以生成ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2C1F3(g)△H=−313kJ/mol;F−F键的键能为159kJ/mol;Cl−C1键的键能为242kJ/mol;则ClF3中C1−F键的平均键能为___ kJ/mol。ClF3的熔、沸点比BrF3的___ (填“高”或“低”)。
(4)根据第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___ 。
(5)(CN)2与Cl2的化学性质相似,(CN)2与NaOH溶液反应的化学方程式为___ 。
(6)上述反应涉及到的元素中,氯原子核外电子能量最高能级符号是___ ;H、Cl、N、O、Na的电负性从小到大的顺序为___ 。
(7)氯有多种含氧酸,其酸性:HClO4>HClO3>HClO2>HClO,从物质结构的角度解释以上含氧酸酸性依次减小的原因___ 。
(1)下面曲线(图1)表示卤族元素某种性质随核电荷数的变化趋势。正确的是

(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子的电子式为
(3)F2与其他卤素单质反应可以生成ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2C1F3(g)△H=−313kJ/mol;F−F键的键能为159kJ/mol;Cl−C1键的键能为242kJ/mol;则ClF3中C1−F键的平均键能为
(4)根据第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(5)(CN)2与Cl2的化学性质相似,(CN)2与NaOH溶液反应的化学方程式为
(6)上述反应涉及到的元素中,氯原子核外电子能量最高能级符号是
(7)氯有多种含氧酸,其酸性:HClO4>HClO3>HClO2>HClO,从物质结构的角度解释以上含氧酸酸性依次减小的原因
您最近一年使用:0次



