CrSi、Ge-GaAs、ZnGeAs2、聚吡咯、碳化硅和氧化亚铜都是重要的半导体化合物。回答下列问题:
(1)基态铬原子的核外电子排布式为___________ ,其中未成对电子数为____________ 。
(2) Ge-GaAs中元素Ge、Ga、As的第一电离能从大到小的顺序为_______________ 。ZnGeAs2中 Zn、Ge、As 的电负性从大到小的顺序为________________ 。
(3) 聚吡咯的单体为吡咯( ),该分子中氮原子的杂化轨道类型为
),该分子中氮原子的杂化轨道类型为__________ ;分子中σ键与π键的数目之比为________________ 。
(4)碳化硅、晶体硅及金刚石的熔点如下表:
分析熔点变化规律及其差异的原因:__________________________________________________ 。
(5)氧化亚铜的熔点为1235℃,其固态时的单晶胞如下图所示。
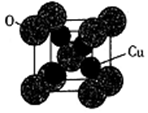
①氧化亚铜属于__________ 晶体。
②已知Cu2O的晶胞参数a=425.8pm,则其密度为__________ g·cm-3 (列出计算式即可)。
(1)基态铬原子的核外电子排布式为
(2) Ge-GaAs中元素Ge、Ga、As的第一电离能从大到小的顺序为
(3) 聚吡咯的单体为吡咯(
 ),该分子中氮原子的杂化轨道类型为
),该分子中氮原子的杂化轨道类型为(4)碳化硅、晶体硅及金刚石的熔点如下表:
| 立方碳化硅 | 晶体硅 | 金刚石 | |
| 熔点/℃ | 2973 | 1410 | 3550~4000 |
分析熔点变化规律及其差异的原因:
(5)氧化亚铜的熔点为1235℃,其固态时的单晶胞如下图所示。

①氧化亚铜属于
②已知Cu2O的晶胞参数a=425.8pm,则其密度为
更新时间:2018-03-20 17:13:48
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】钼精矿中含有 ,还含有
,还含有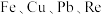 的硫化物。铼、钼的回收价值较高,科研人员可从如下图所示的工艺流程中提取铼、钼等金属。
的硫化物。铼、钼的回收价值较高,科研人员可从如下图所示的工艺流程中提取铼、钼等金属。 为一种有机萃取剂(用
为一种有机萃取剂(用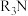 表示),萃取过程可表示:
表示),萃取过程可表示:
②高铼酸铵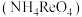 是白色片状晶体,微溶于冷水,溶于热水。
是白色片状晶体,微溶于冷水,溶于热水。
③铼是一种类锰元素,价电子与锰类似。
回答下列问题:
(1)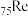 的价电子排布式为
的价电子排布式为___________ 。
(2)Re2O7所属的类型为___________ (填“酸性”“碱性”或“两性”)氧化物。
(3)钼精矿焙烧除了常见的氧化焙烧之外,还有石灰焙烧法, 、
、 焙烧转化为
焙烧转化为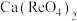 的化学方程式为
的化学方程式为___________ ,氧化焙烧法比较与石灰焙烧法的缺点是___________ 。
(4)试剂A适宜用___________ 。
(5)操作X为___________ 、过滤、洗涤、干燥。
(6)在 还原
还原 的过程中,实际
的过程中,实际 的用量大于理论值,原因是
的用量大于理论值,原因是___________ 。
 ,还含有
,还含有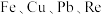 的硫化物。铼、钼的回收价值较高,科研人员可从如下图所示的工艺流程中提取铼、钼等金属。
的硫化物。铼、钼的回收价值较高,科研人员可从如下图所示的工艺流程中提取铼、钼等金属。
 为一种有机萃取剂(用
为一种有机萃取剂(用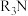 表示),萃取过程可表示:
表示),萃取过程可表示:
②高铼酸铵
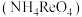 是白色片状晶体,微溶于冷水,溶于热水。
是白色片状晶体,微溶于冷水,溶于热水。③铼是一种类锰元素,价电子与锰类似。
回答下列问题:
(1)
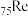 的价电子排布式为
的价电子排布式为(2)Re2O7所属的类型为
(3)钼精矿焙烧除了常见的氧化焙烧之外,还有石灰焙烧法,
 、
、 焙烧转化为
焙烧转化为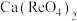 的化学方程式为
的化学方程式为(4)试剂A适宜用
(5)操作X为
(6)在
 还原
还原 的过程中,实际
的过程中,实际 的用量大于理论值,原因是
的用量大于理论值,原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Cu+在基态时的价电子排布式为__________________ 。
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释___________________________ 。
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为_____________ 。
(4)AsF3的空间构型是:______________ 。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为________ 。
②[B(OH)4]-的结构式为____________________ 。
(6)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是_______________________ (用化学式表示)。
②立方氮化硼(BN)晶体的结构与金刚石相似,硬度与金刚石相当,立方氮化硼的密度是ρ g·㎝-3,,则晶胞边长为___________ 。(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(1)Cu+在基态时的价电子排布式为
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为
(4)AsF3的空间构型是:
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为
②[B(OH)4]-的结构式为
(6)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是
②立方氮化硼(BN)晶体的结构与金刚石相似,硬度与金刚石相当,立方氮化硼的密度是ρ g·㎝-3,,则晶胞边长为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】 是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺如下。
水合物的工艺如下。 时各物质溶度积见下表:
时各物质溶度积见下表:
回答下列问题:
(1) 中
中 元素的化合价是
元素的化合价是 和
和_______ 。 的核外电子排布式为
的核外电子排布式为_______ 。
(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是_______ 。
(3)反应釜2中,加入 和分散剂的同时通入空气。
和分散剂的同时通入空气。
①反应的离子方程式为_______ 。
②为加快反应速率,可采取的措施有_______ 。(写出两项即可)。
(4)①反应釜3中, 时,
时, 浓度为
浓度为 ,理论上
,理论上 不超过
不超过_______ 。
②称取 水合物
水合物 ,加水溶解,加入过量
,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用
,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用 标准溶液滴定,消耗
标准溶液滴定,消耗 。滴定达到终点的现象为
。滴定达到终点的现象为_______ ,该副产物中 的质量分数为
的质量分数为_______ 。
 是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺如下。
水合物的工艺如下。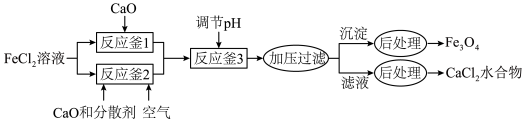
 时各物质溶度积见下表:
时各物质溶度积见下表:| 物质 |  |  |  |
溶度积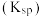 |  |  |  |
(1)
 中
中 元素的化合价是
元素的化合价是 和
和 的核外电子排布式为
的核外电子排布式为(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是
(3)反应釜2中,加入
 和分散剂的同时通入空气。
和分散剂的同时通入空气。①反应的离子方程式为
②为加快反应速率,可采取的措施有
(4)①反应釜3中,
 时,
时, 浓度为
浓度为 ,理论上
,理论上 不超过
不超过②称取
 水合物
水合物 ,加水溶解,加入过量
,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用
,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用 标准溶液滴定,消耗
标准溶液滴定,消耗 。滴定达到终点的现象为
。滴定达到终点的现象为 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】图1是元素周期表的一部分,已知A、B、C、D、E、F、G都是周期表中的前四周期元素,它们在周期表中的位置如图1所示。
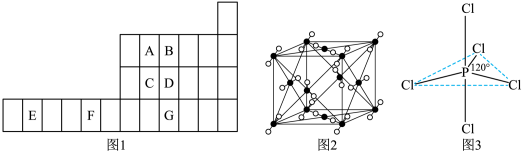
试回答下列问题:
(1)F元素基态原子的核外电子排布式为_________________ 。
(2)ABC的第一电离能由大到小的顺序______________ (用元素符号表示)。
(3)B元素单质分子中的_______ 个π键,与其互为等电子体的阴离子为____________________ 。
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用________ 杂化,每个分子周围有_____ 个分子与之距离相等且最近。若晶胞棱长为a pm,则该晶体密度的表达式为________ g·cm-3。
(5)G元素的氢化物分子的空间构型为________ ,其沸点与B元素的氢化物相比________ (填高或低),其原因是________ 。
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式________ 。
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同__________ ?(填“相同”或“不同”)。

试回答下列问题:
(1)F元素基态原子的核外电子排布式为
(2)ABC的第一电离能由大到小的顺序
(3)B元素单质分子中的
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用
(5)G元素的氢化物分子的空间构型为
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)①铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是___ (填字母)。
A. 电子从基态跃迁到较高的激发态 B. 电子从较高的激发态跃迁到基态
C. 焰色反应的光谱属于吸收光谱 D. 焰色反应的光谱属于发射光谱
②碘、铜两种元素的电负性如表:
CuI属于_______ (填“共价”或“离子”)化合物。
(2)氯化铁溶液用于检验食用香精乙酰乙酯时,会生成紫色配合物,其配离子结构如图所示。
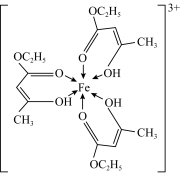
①此配合物中,基态铁离子的价电子排布图为________________ 。
②此配合物中碳原子的杂化轨道类型有________________ 。
③此配离子中含有的化学键有____________ (填字母)。
A.σ键 B.π键 C.极性键 D.非极性键 E. 配位键 F. 氢键 G.离子键
(3)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_____________ 。
(4)治疗铅中毒可滴注依地酸(别名EDTA,结构如下面左图)钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是_________ (填标号)

A.形成依地酸铅离子所需n(Pb2+):n(EDTA)=1:4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
(5)AlCl3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,一个分子中的氯原子与另外一个铝原子形成配位键,因此以二聚体Al2Cl6的形式存在,写出Al2Cl6的结构式_______ (用→标出配位键)。
(1)①铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是
A. 电子从基态跃迁到较高的激发态 B. 电子从较高的激发态跃迁到基态
C. 焰色反应的光谱属于吸收光谱 D. 焰色反应的光谱属于发射光谱
②碘、铜两种元素的电负性如表:
| 元素 | I | Cu |
| 电负性 | 2.5 | 1.9 |
(2)氯化铁溶液用于检验食用香精乙酰乙酯时,会生成紫色配合物,其配离子结构如图所示。

①此配合物中,基态铁离子的价电子排布图为
②此配合物中碳原子的杂化轨道类型有
③此配离子中含有的化学键有
A.σ键 B.π键 C.极性键 D.非极性键 E. 配位键 F. 氢键 G.离子键
(3)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是
(4)治疗铅中毒可滴注依地酸(别名EDTA,结构如下面左图)钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是

A.形成依地酸铅离子所需n(Pb2+):n(EDTA)=1:4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
(5)AlCl3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,一个分子中的氯原子与另外一个铝原子形成配位键,因此以二聚体Al2Cl6的形式存在,写出Al2Cl6的结构式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】钕铁硼永磁合金因其具有优异的磁性能而被称为“磁王”,钕铁硼永磁合金中含有铁、硼及大量的稀土元素钕。
(1)基态铁原子的价层电子排布图为___________________ ,铁元素所在周期第一电离能最大的主族元素是________ (填元素符号);已知基态钕(Nd)原子的价层电子排布式为4f46s2,则基态钕原子核外共有__________ 种类型的能级分布。
(2)硼与氢能形成类似于烃的一系列分子,如B2H6、B3H9、B4H10等。
①B2H6、B3H9、B4H10三种物质的沸点由低到高的顺序为__________________________ ;
②乙硼烷的结构式可表示为( )已知反应B2H6+3O2
)已知反应B2H6+3O2 B2O3+2H2O中被氧化的元素是氢元系,则H、B、O三种元素电负性由大到小的顺序为
B2O3+2H2O中被氧化的元素是氢元系,则H、B、O三种元素电负性由大到小的顺序为___________________ ;B2H6分子中有4个σ键、2个相同的大π键(多原子间共用多个电子形成的一种共价键),则构成一个大π键的原子、电子数目分别为__________________________ 。
(3)硼酸分子中含有三个“-OH”,易溶于水,其易溶于水的主要原因是_________________ 。
(4)图1是三氧化二硼的一种球根模型图, 则硼原子、氧原子的杂化轨道类型分别为_____________ 。

(5)铁元素与氮元素也能形成种磁性材料,其晶胞如图2所示,该磁性材料的化学式为__________ ;若该晶体的密度为p,铁原子、氮原子的半径分别为r(Fe)pm,r(N)pm,则该晶胞的空间利用率为_______ (设阿伏伽德罗常数的值为NA)。
(1)基态铁原子的价层电子排布图为
(2)硼与氢能形成类似于烃的一系列分子,如B2H6、B3H9、B4H10等。
①B2H6、B3H9、B4H10三种物质的沸点由低到高的顺序为
②乙硼烷的结构式可表示为(
 )已知反应B2H6+3O2
)已知反应B2H6+3O2 B2O3+2H2O中被氧化的元素是氢元系,则H、B、O三种元素电负性由大到小的顺序为
B2O3+2H2O中被氧化的元素是氢元系,则H、B、O三种元素电负性由大到小的顺序为(3)硼酸分子中含有三个“-OH”,易溶于水,其易溶于水的主要原因是
(4)图1是三氧化二硼的一种球根模型图, 则硼原子、氧原子的杂化轨道类型分别为

(5)铁元素与氮元素也能形成种磁性材料,其晶胞如图2所示,该磁性材料的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】钠离子电池被认为在基于电网的储能系统中最具发展前景,双金属硫化物Sb2S3@FeS2空心纳米棒将有助于提高钠离子电池性能。回答下列问题:
(1)Sb位于第五周期,与N同主族,基态Sb的价电子排布图(轨道表达式)为_______ , (氟锑酸)是一种超强酸,
(氟锑酸)是一种超强酸,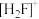 的空间构型为
的空间构型为_______ ,与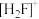 具有相同空间构型和键合形式的阴离子为
具有相同空间构型和键合形式的阴离子为_______ 。
(2)Si、P与S是同周期中相邻的元素,Si、P、S的第一电离能由大到小的顺序是_______ 。
(3)与S同主族的元素有O、Se、Te等,它们氢化物的沸点大小为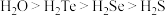 ,其原因是
,其原因是_______ 。
(4)已知: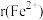 为61pm,
为61pm, 为65pm。在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3的分解温度低于CoCO3,原因是
为65pm。在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3的分解温度低于CoCO3,原因是_______ 。
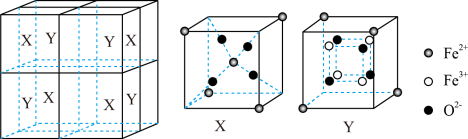
(5)其离子型铁的氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为_______ ;已知该晶体的密度为 ,阿伏加德罗常数的值为NA,则该晶体的晶胞参数
,阿伏加德罗常数的值为NA,则该晶体的晶胞参数
_______ pm(用含d和NA的代数式表示)。
(1)Sb位于第五周期,与N同主族,基态Sb的价电子排布图(轨道表达式)为
 (氟锑酸)是一种超强酸,
(氟锑酸)是一种超强酸,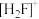 的空间构型为
的空间构型为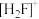 具有相同空间构型和键合形式的阴离子为
具有相同空间构型和键合形式的阴离子为(2)Si、P与S是同周期中相邻的元素,Si、P、S的第一电离能由大到小的顺序是
(3)与S同主族的元素有O、Se、Te等,它们氢化物的沸点大小为
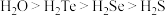 ,其原因是
,其原因是(4)已知:
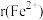 为61pm,
为61pm, 为65pm。在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3的分解温度低于CoCO3,原因是
为65pm。在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3的分解温度低于CoCO3,原因是(5)其离子型铁的氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为
 ,阿伏加德罗常数的值为NA,则该晶体的晶胞参数
,阿伏加德罗常数的值为NA,则该晶体的晶胞参数

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】钛硅分子筛是一种新型固体催化剂,可催化合成重要有机合成活性试剂甲乙酮肟(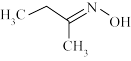 )。回答下列问题:
)。回答下列问题:
(1)基态硅原子的核外电子空间运动状态有____ 种。
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为____ ,氮原子的杂化方式为____ ,C=N与C—C键夹角____ (填“<”“>”或“=”)C=N与N—O键夹角。
(3)TiO2和TiCl4均是制备钛硅分子筛的重要中间体。
①TiO2与光气COCl2反应可用于制取四氯化钛。COCl2中σ键和π键的数目比为____ ,其空间构型为____ 。
②TiCl4与金属Ti在高温条件下可反应生成TiCl3,TiCl3中Ti3+极易被氧化,还原性很强。试解释Ti3+还原性强的原因____ 。
(4)研究表明,在TiO2通过氮掺杂反应生成TiO2-mNn,能使TiO2对可见光具有活性,反应如图所示。

若TiO2晶体密度为ρg·cm-3,则阿伏加德罗常数的值NA=____ ,TiO2-mNn晶体中m=____ 。
 )。回答下列问题:
)。回答下列问题:(1)基态硅原子的核外电子空间运动状态有
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为
(3)TiO2和TiCl4均是制备钛硅分子筛的重要中间体。
①TiO2与光气COCl2反应可用于制取四氯化钛。COCl2中σ键和π键的数目比为
②TiCl4与金属Ti在高温条件下可反应生成TiCl3,TiCl3中Ti3+极易被氧化,还原性很强。试解释Ti3+还原性强的原因
(4)研究表明,在TiO2通过氮掺杂反应生成TiO2-mNn,能使TiO2对可见光具有活性,反应如图所示。

若TiO2晶体密度为ρg·cm-3,则阿伏加德罗常数的值NA=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】VA族元素及其化合物在材料等方面有重要用途。根据所学知识回答下列问题:
(1)基态砷原子处于最高能级的电子云轮廓图为_______ 形。
(2)NH3、PH3、AsH3是同主族元素的氢化物,其中键角最小的是________ 。
(3)叠氮化钠(NaN3)用于汽车的安气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(HN3),叠氮酸中3个氮原子的杂化类型分别为___________ (不分先后)。
(4)N原子之间可以形成π键,而As原子之间较难形成π键。从原子结构角度分析,其原因为________ 。
(5)往硫酸铜溶液中加入过量氨水,可生成配离子[Cu(NH3)4]2+。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是______ 。
(6)磷的含氧酸有很多种,其中有磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸(H3PO2)等。
①已知NaH2PO2是次磷酸的正盐,则1molH3PO2中含有的σ键的物质的量为___ mol。
②磷酸通过分子间脱水缩合形成多磷酸,如:
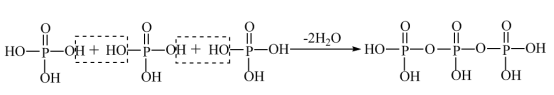
如果有n个磷酸分子间脱水形成链状的多磷酸,则相应的酸根可写为_______ 。
(7)HgCl2和不同浓度NH3–NH4Cl反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个Hg原子均处于小立方体的面心)

写出该含汞化合物的化学式:______ 。则该晶体的密度ρ=_____ g·cm-3(设阿伏加德罗常数的值为NA,用含a、NA的代数式表示)。
(1)基态砷原子处于最高能级的电子云轮廓图为
(2)NH3、PH3、AsH3是同主族元素的氢化物,其中键角最小的是
(3)叠氮化钠(NaN3)用于汽车的安气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(HN3),叠氮酸中3个氮原子的杂化类型分别为
(4)N原子之间可以形成π键,而As原子之间较难形成π键。从原子结构角度分析,其原因为
(5)往硫酸铜溶液中加入过量氨水,可生成配离子[Cu(NH3)4]2+。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(6)磷的含氧酸有很多种,其中有磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸(H3PO2)等。
①已知NaH2PO2是次磷酸的正盐,则1molH3PO2中含有的σ键的物质的量为
②磷酸通过分子间脱水缩合形成多磷酸,如:

如果有n个磷酸分子间脱水形成链状的多磷酸,则相应的酸根可写为
(7)HgCl2和不同浓度NH3–NH4Cl反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个Hg原子均处于小立方体的面心)

写出该含汞化合物的化学式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】元素及其化合物在化工、医药、材料等领域有着广泛的应用,回答下列问题:
(1)参照下图 B、F 元素的位置,依据第二周期元素第一电离能的变化规律,用小黑点标出 C、N、O 三 种元素的相对位置。

(2)碳的一种单质的结构如图(a)所示,则碳原子的杂化轨道类型为_________________ 。
(3)二卤化铅 PbX2 的熔点如图(b)所示,可推断:依 F、Cl、Br、I 次序,PbX2 中的化学键 的离子性_____ ( 填“增 强”、“ 不变”或“减弱”, 下 同 ), 共价性_____ 。

(4)NH3 和 F2 在 Cu 催化下可发生反应 4NH3+3F2 NF3+3NH4F,化学方程式中的 5 种物质所属的晶体 类型有
NF3+3NH4F,化学方程式中的 5 种物质所属的晶体 类型有_____ (填序号)。写出基态铜原子的价电子排布式_____ 。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
(5)BF3 与一定量水形成(H2O)2·BF3 晶体 Q,Q 在一定条件下可转化为 R: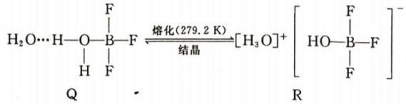 晶体 R 中含有的化学键包 括
晶体 R 中含有的化学键包 括_____ 。
(6)水杨酸第一级电离形成离子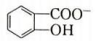 ,相同温度下,水杨酸的 Ka2
,相同温度下,水杨酸的 Ka2____________________________ 苯酚
(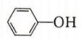 )的 Ka(填“>”“ =”或“<”),其原因是
)的 Ka(填“>”“ =”或“<”),其原因是______________ 。
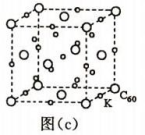
(7)碳的另一种单质 C60 可以与钾形成低温超导化合物,晶体结构如图(c)所示,K 位于立方体的棱上和 立方体的内部,此化合物的化学式为____________ ;其晶胞参数为 1.4 nm,阿伏伽德罗常数用 NA 表 示,则晶体的密度为________________ g·cm-3。(只需列出式子)
(1)参照下图 B、F 元素的位置,依据第二周期元素第一电离能的变化规律,用小黑点标出 C、N、O 三 种元素的相对位置。

(2)碳的一种单质的结构如图(a)所示,则碳原子的杂化轨道类型为
(3)二卤化铅 PbX2 的熔点如图(b)所示,可推断:依 F、Cl、Br、I 次序,PbX2 中的化学键 的离子性

(4)NH3 和 F2 在 Cu 催化下可发生反应 4NH3+3F2
 NF3+3NH4F,化学方程式中的 5 种物质所属的晶体 类型有
NF3+3NH4F,化学方程式中的 5 种物质所属的晶体 类型有a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
(5)BF3 与一定量水形成(H2O)2·BF3 晶体 Q,Q 在一定条件下可转化为 R:
 晶体 R 中含有的化学键包 括
晶体 R 中含有的化学键包 括(6)水杨酸第一级电离形成离子
 ,相同温度下,水杨酸的 Ka2
,相同温度下,水杨酸的 Ka2(
 )的 Ka(填“>”“ =”或“<”),其原因是
)的 Ka(填“>”“ =”或“<”),其原因是(7)碳的另一种单质 C60 可以与钾形成低温超导化合物,晶体结构如图(c)所示,K 位于立方体的棱上和 立方体的内部,此化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期,A基态原子的2p轨道上有2个未成对电子,C的最外层电子数是次外层电子数的3倍,C与D同主族相邻,E位于周期表的ds区,最外层只有一对成对电子。请回答下列问题:
(1)写出各元素符号:A________ ,B________ ,C________ ,D________ ,E________ 。
(2)D元素在元素周期表中的位置是_______________ ,基态E原子的电子占有_____ 种能量不同的原子轨道。
(3)A元素可形成多种单质,其中分子晶体的分子式为________ ;原子晶体的名称是_______ ,其每个晶胞(如图甲)实际含有______ 个A原子;A有一种单质为层状结构的晶体,晶体中存在的作用力有____________ ,晶体中每个最小环含有_____ 个原子。

(4)①写出B的单质的电子式___________ ,化合物AC2的结构式___________ 。
②用KMnO4酸性溶液吸收DC2气体时,MnO4﹣被还原为Mn2+,该反应的离子方程式为________________________________________________ 。
(5)D与E能形成化合物X,X的一种晶体晶胞结构如图乙所示,X的化学式为______ ,D离子的配位数为______ ;若晶胞边长为a cm,则晶体X的密度计算式为ρ=______________ g•cm-3(用a和NA的代数式表示)。

(1)写出各元素符号:A
(2)D元素在元素周期表中的位置是
(3)A元素可形成多种单质,其中分子晶体的分子式为

(4)①写出B的单质的电子式
②用KMnO4酸性溶液吸收DC2气体时,MnO4﹣被还原为Mn2+,该反应的离子方程式为
(5)D与E能形成化合物X,X的一种晶体晶胞结构如图乙所示,X的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】已知A、B、C为三种常见的单质,能发生如图1所示的转化关系,B的一种同素异形体的晶胞如图2所示。
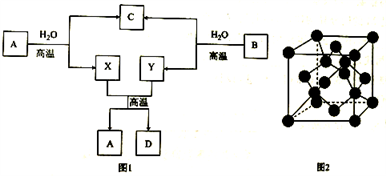
回答下列问题:
(1)形成A的元素在周期表中的位置是__________________________________ ,A对应的基态原子的价电子排布为_____________________ 。
(2)在B单质对应的基态原子中,核外存在___________ 对自旋方向相反的电子。
(3)写出Y的一种常见等电子体分子的结构式__________________________ ;两者相比较沸点较高的是__________ (填化学式);Y分子中B对应原子的杂化方式为_________________ 。
(4)配合物A(Y)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断A(Y)x晶体属于________________ (填晶体类型)。A(Y)x的中心原子价电子数与配体提供的电子数之和为18,则x=__________ 。A(Y)x在一定条件下发生反应A(Y)x (s)  A (s) + x Y (g),已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型是
A (s) + x Y (g),已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型是_____________ 。
(5)在图2晶胞中,每个晶胞平均占有__________ 个原子,若距离最近的两个原子的距离为L cm,晶胞边长为a cm,根据硬球接触模型,则L=_________ a,晶胞的密度ρ=___________ g·cm-3(用含a、NA代数式表示)。

回答下列问题:
(1)形成A的元素在周期表中的位置是
(2)在B单质对应的基态原子中,核外存在
(3)写出Y的一种常见等电子体分子的结构式
(4)配合物A(Y)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断A(Y)x晶体属于
 A (s) + x Y (g),已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型是
A (s) + x Y (g),已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型是(5)在图2晶胞中,每个晶胞平均占有
您最近一年使用:0次



