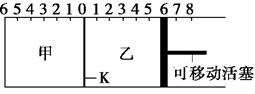
如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2 mol A和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g) 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
| A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡 |
| B.达到平衡后,隔板K最终停留在左侧刻度0~2之间 |
| C.达到平衡时,甲容器中C的物质的量大于乙容器中C的物质的量 |
| D.若平衡时K停留在左侧1处,则活塞仍停留在右侧6处 |
10-11高二下·浙江杭州·期中 查看更多[2]
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】已知图一表示的是可逆反应O2(g)+2SO2(g)⇌2SO3(g) ∆H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)⇌N2O4(g) ∆H<0的浓度(c)随时间t 的变化情况。下列说法中正确的是


| A.若图一t2时改变的条件是增大压强,则反应∆H的增大 |
| B.图一t2时改变的条件可能是升高了温度或增大了压强 |
| C.图二t1时改变的条件可能是增大了压强 |
| D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】—定条件下,在容积为10L的密闭容器中,将2molX和1molY进行如下反应:2X(g)+Y(g) Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
 Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是| A.1min内,用Z表示平均反应速率为0.03mol·L-1·min-1 |
| B.将容器容积变为20L,Z的新平衡浓度将等于原平衡浓度的一半 |
| C.当X的体积分数不变时,则说明该反应达到平衡状态 |
| D.若温度和体积不变,往容器内增加1molX,Y的转化率将增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】卤族元素单质及其化合物应用广泛。 具有与卤素单质相似的化学性质。
具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37.
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37. 通入
通入 酸性溶液中可制得黄绿色气体
酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用
,该气体常用作自来水消毒剂。工业用 制备
制备 的热化学方程式为
的热化学方程式为

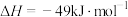 。下列关于反应
。下列关于反应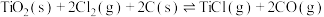 的说法
的说法不正确 的是
 具有与卤素单质相似的化学性质。
具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37.
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37. 通入
通入 酸性溶液中可制得黄绿色气体
酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用
,该气体常用作自来水消毒剂。工业用 制备
制备 的热化学方程式为
的热化学方程式为

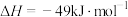 。下列关于反应
。下列关于反应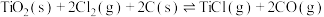 的说法
的说法A.保持其他条件不变,平衡时升高温度, |
B.保持其他条件不变,平衡时通入 ,达到新平衡时 ,达到新平衡时 变小 变小 |
C.反应生成1mol ,转移电子数目为 ,转移电子数目为 |
D.及时分离出CO,有利于 生成 生成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一定温度下将CaCO3放入密闭真空容器中,反应CaCO3(s) CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是
CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是
 CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是
CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是| A.平衡向左移动 | B.压强不变 |
| C.平衡常数不变 | D.固体总质量不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】恒温恒容,可逆反应N2O4(g) 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是| A.NO2的体积分数增大 | B.达新平衡后平衡体系压强比原平衡大 |
| C.平衡正向移动 | D.达新平衡后N2O4转化率降低 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知反应:2NO2(红棕色) N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小,且整个操作过程物质均为气态)。下列说法不正确的是
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小,且整个操作过程物质均为气态)。下列说法不正确的是
 N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小,且整个操作过程物质均为气态)。下列说法不正确的是
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小,且整个操作过程物质均为气态)。下列说法不正确的是
| A.b点到c点的实验现象是气体颜色先变深后变浅,最后气体颜色比a点还要深 |
| B.c点与a点相比,n(NO2)减小,混合气体密度增大 |
| C.d 点:v(正)<v(逆) |
D.若在注射器中对反应H2(g)+I2(g)  2HI(g)进行完全相同的操作,最后能得到相似的透光率变化趋势图象 2HI(g)进行完全相同的操作,最后能得到相似的透光率变化趋势图象 |
您最近一年使用:0次



