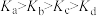一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
| A.v1< v2,c2< 2c1 | B.K1> K3,p2> 2p3 |
| C.v1< v3,α1(SO2 ) >α3(SO2 ) | D.c2> 2c3,α2(SO3 )+α3(SO2 )<1 |
2018·江苏·高考真题 查看更多[9]
2018年全国普通高等学校招生统一考试化学(江苏卷)(已下线)2018年高考题及模拟题汇编 专题09 反应速率、化学平衡(已下线)高考母题题源07 化学反应速率与化学平衡(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】(已下线)2019高考备考二轮复习精品资料-专题9 化学反应速率与化学平衡(教学案)(已下线)2019年高考总复习巅峰冲刺-专题06 化学反应速率、化学平衡问题应试策略山东省恒台第一中学2019-2020学年高二上学期期中考试化学试题(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训(已下线)2.3.3+化学平衡常数-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)
更新时间:2018-06-10 12:37:17
|
相似题推荐
多选题
|
较难
(0.4)
【推荐1】已知反应:CH2=CHCH3(g)+Cl2(g)⇌CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按w=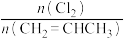 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是

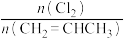 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆反应的平衡常数与温度的关系,则下列说法错误的是
| A.图甲中,w2>1 |
| B.图乙中,A线表示正反应的平衡常数 |
| C.温度为T1、w=2时,Cl2的平衡转化率为50% |
| D.若在恒容绝热装置中进行上述反应,达到平衡时,装置内的气体压强将增大 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)  2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是
2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是
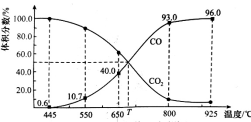
 2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是
2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是
| A.550℃时,若充入惰性气体,v正,v逆均减小,平衡不移动 |
| B.650℃时,反应达平衡后CO2的转化率为25.0% |
| C.T℃时,若充入等体积的CO2和CO,平衡不移动 |
| D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0p总 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐3】用CO还原 可减轻汽车尾气对空气的污染,该反应的热化学方程式为:
可减轻汽车尾气对空气的污染,该反应的热化学方程式为: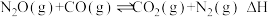 。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol
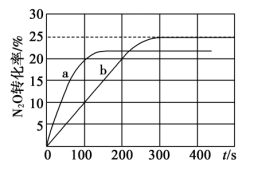
。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol 和0.4molCO,测得容器中
和0.4molCO,测得容器中 转化率随时间变化关系如图。下列说法正确的是
转化率随时间变化关系如图。下列说法正确的是
 可减轻汽车尾气对空气的污染,该反应的热化学方程式为:
可减轻汽车尾气对空气的污染,该反应的热化学方程式为: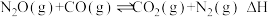 。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol
。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol 和0.4molCO,测得容器中
和0.4molCO,测得容器中 转化率随时间变化关系如图。下列说法正确的是
转化率随时间变化关系如图。下列说法正确的是
A.A容器中 的转化率随时间的变化关系是图中的曲线a 的转化率随时间的变化关系是图中的曲线a |
B.可通过缩小容器体积来缩短b曲线对应容器达到平衡的时间,同时不改变 的平衡转化率 的平衡转化率 |
C.500℃该反应的化学平衡常数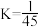 |
D.在平衡后向A容器中加入0.075mol 与0.025mol 与0.025mol ,则平衡正向移动 ,则平衡正向移动 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
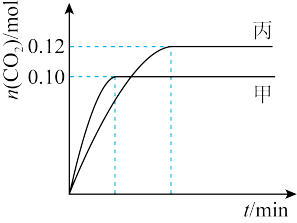
 N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
| 容器 | 温度/℃ | 起始物质的量/mol | |
| NO (g) | CO (g) | ||
| 甲 | T1 | 0.20 | 0.20 |
| 乙 | T1 | 0.30 | 0.30 |
| 丙 | T2 | 0.20 | 0.20 |
| A.该反应的正反应为吸热反应 |
| B.达到平衡时,乙中CO2的体积分数比甲中的大 |
| C.T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆) |
| D.T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40% |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】在某温度下,向三个初始体积均为1 L的密闭容器中按下表所示投料,发生反应:2SO2(g)+O2(g)  2SO3(g);ΔH<0。达到平衡时,下列说法不正确的是
2SO3(g);ΔH<0。达到平衡时,下列说法不正确的是
 2SO3(g);ΔH<0。达到平衡时,下列说法不正确的是
2SO3(g);ΔH<0。达到平衡时,下列说法不正确的是| 容器 编号 | 容器 类型 | 起始时,有关物质的物质的量/mol | 平衡时,SO3的物质的量/mol | ||
| SO2 | O2 | SO3 | |||
| Ⅰ | 恒温恒容 | 2 | 1 | 0 | 1.2 |
| Ⅱ | 绝热恒容 | 0 | 0 | 2 | a |
| Ⅲ | 恒温恒压 | 2 | 1 | 0 | b |
| A.平衡时SO3的物质的量:a>1.2,b <1.2 |
| B.容器Ⅱ、Ⅲ中的平衡常数相同 |
| C.容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1 |
| D.若起始时向容器Ⅰ中充入1 mol SO2(g)、0.4 mol O2(g)和1.4 mol SO3 (g),则此时v(正)>v(逆) |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】恒压下,将CO2和H2以体积比1∶4混合进行反应CO2(g)+4H2(g) CH4(g)+2H2O(g)(假定过程中无其他反应发生),用Ru/TiO2催化反应相同时间,测得CO2转化率随温度变化情况如图所示。下列说法正确的是( )
CH4(g)+2H2O(g)(假定过程中无其他反应发生),用Ru/TiO2催化反应相同时间,测得CO2转化率随温度变化情况如图所示。下列说法正确的是( )
 CH4(g)+2H2O(g)(假定过程中无其他反应发生),用Ru/TiO2催化反应相同时间,测得CO2转化率随温度变化情况如图所示。下列说法正确的是( )
CH4(g)+2H2O(g)(假定过程中无其他反应发生),用Ru/TiO2催化反应相同时间,测得CO2转化率随温度变化情况如图所示。下列说法正确的是( )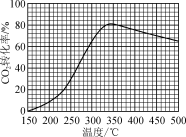
| A.反应CO2(g)+4H2(g)=CH4(g)+2H2O(g)的ΔH>0 |
| B.图中450 ℃时,延长反应时间无法提高CO2的转化率 |
| C.350 ℃时,c(H2)起始=0.4 mol·L-1,CO2平衡转化率为80%,则平衡常数K<2 500 |
| D.当温度从400 ℃升高至500 ℃,反应处于平衡状态时,v(400℃)逆>v(500℃)逆 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】工业上消除氮氧化物的污染可用如下反应:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的恒容密闭容器中,测得n(N2)随时间变化的数据如表.下列说法不正确的是
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(N2) | 0[ | 0.20 | 0.35 | 0.40 | 0.40 |
| T2 | n(N2) | 0 | 0.25 | … | 0.30 | 0.30 |
| A.T1温度下,CH4的平衡转化率为50% |
| B.T1<T2 |
| C.a<0 |
| D.T2时反应的平衡常数大于T1时反应的平衡常数 |
您最近一年使用:0次


 污染,反应原理如下:
污染,反应原理如下: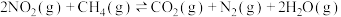 。T℃时,将2mol
。T℃时,将2mol  的混合气体置于绝热恒容密闭容器中发生反应,正反应速率随时间变化的趋势如图所示。
的混合气体置于绝热恒容密闭容器中发生反应,正反应速率随时间变化的趋势如图所示。
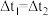 ,则产生
,则产生 的量:ab段<bc段
的量:ab段<bc段