铂(Pt)及其化合物用途广泛。
(1)在元素周期表中,Pt与Fe相隔一个纵行、一个横行,但与铁元素同处_____ 族。基态铂原子有2个未成对电子,且在能量不同的原子轨道上运动,其价电子排布式为____________ 。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
①吡啶分子是大体积平面配体,其结构简式如图所示。每个吡啶分子中含有的σ键数目为________ 。
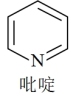
②二氯二吡啶合铂中存在的微粒间作用力有________ (填序号)。
a.离子键b.氢键c.范德华力d.金属键e.非极性键
③反式二氯二吡啶合铂分子是非极性分子,画出其结构式:_____ 。
(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
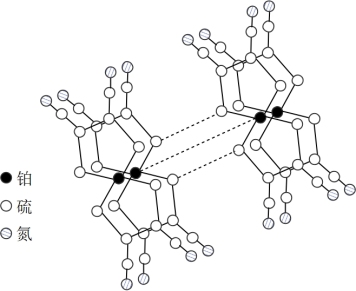
①硫和氮中,第一电离能较大的是______ 。
②“分子金属”可以导电,是因为______ 能沿着其中的金属原子链流动。
③“分子金属”中,铂原子是否以sp3的方式杂化?简述理由:______ 。
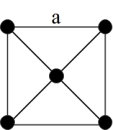
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为dg·cm-3,则晶胞参数a=_________________ nm(列计算式)。
(1)在元素周期表中,Pt与Fe相隔一个纵行、一个横行,但与铁元素同处
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
①吡啶分子是大体积平面配体,其结构简式如图所示。每个吡啶分子中含有的σ键数目为

②二氯二吡啶合铂中存在的微粒间作用力有
a.离子键b.氢键c.范德华力d.金属键e.非极性键
③反式二氯二吡啶合铂分子是非极性分子,画出其结构式:
(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。

①硫和氮中,第一电离能较大的是
②“分子金属”可以导电,是因为
③“分子金属”中,铂原子是否以sp3的方式杂化?简述理由:
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为dg·cm-3,则晶胞参数a=

更新时间:2018-06-03 18:52:37
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、元素周期表与元素周期律在化学学习研究中有很重要的作用。时至今年,已是元素周期表诞生的第154周年。下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试根据表格回答下列问题:
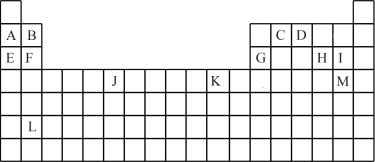
(1)写出基态J原子的简化电子排布式:_______ ,L的原子序数:_______ ,M的价层电子排布式:_______ 。
(2)下列关于元素在元素周期表中的位置的叙述正确的是_______(填选项字母)。
(3)下列有关说法正确的是_______(填选项字母)。
(4)如图是部分元素原子的第一电离能 随原子序数变化的曲线图。
随原子序数变化的曲线图。
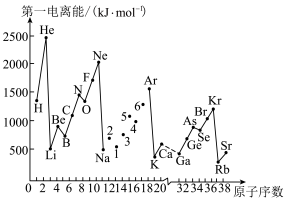
①认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间的元素用短线连接起来,构成完整的图像_______ 。
②从图像分析可知,同一主族元素原子的第一电离能 变化规律是
变化规律是_______ 。

(1)写出基态J原子的简化电子排布式:
(2)下列关于元素在元素周期表中的位置的叙述正确的是_______(填选项字母)。
| A.K位于元素周期表中第四周期第IIB族,属于ds区元素 |
| B.J位于元素周期表中第四周期第IVB族,属于d区元素 |
| C.F位于元素周期表中第三周期第IIA族,属于s区元素 |
| D.I位于元素周期表中第三周期第VIIA族,属于ds区元素 |
| A.第一电离能:G>F>E | B.电负性:D>C |
| C.原子半径:E>H | D.最高价氧化物对应水化物的酸性:I>H |
 随原子序数变化的曲线图。
随原子序数变化的曲线图。
①认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间的元素用短线连接起来,构成完整的图像
②从图像分析可知,同一主族元素原子的第一电离能
 变化规律是
变化规律是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为___________ 。
(2)在BF3分子中B原子的杂化轨道类型为___________ 。
(3)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(4)已知(CN)2是直线形分子,且有对称性,其中π键与σ键的个数比为___________ 。
(5)基态S原子价电子排布式___________ ;S原子的核外电子运动状态有___________ 种。
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为
(2)在BF3分子中B原子的杂化轨道类型为
(3)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(4)已知(CN)2是直线形分子,且有对称性,其中π键与σ键的个数比为
(5)基态S原子价电子排布式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W是元素周期表中前四周期的常见元素,其相关信息如下表;
(1)X位于元素周期表中的位置______ 。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于______ 晶体。
(2)XY2的电子式是______ ;分子空间构型为______ 。
(3)Z2Y2中含有的化学键类型有______ ;阴、阳离子的个数比为______ 。
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 原子最外层电子数是次外层的三倍 |
| Z | 单质及其化合物的焰色反应为黄色 |
| W | W为前四周期中未成对电子数最多的元素 |
(2)XY2的电子式是
(3)Z2Y2中含有的化学键类型有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】三草酸合铁酸钾{K3[Fe(C2O4)3]•3H2O}是制备铁触媒的主要原料,在光照下能分解:2K3[Fe(C2O4)3]•3H2O 3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:
3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:
(1)基态Fe原子的电子排布式为___ ,基态Fe2+与Fe3+中未成对电子的数目之比为___ 。
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是___ (填元素符号,下同),电负性最大的是____ 。
(3)CO2分子中σ键和π键的个数之比为___ ,H2O分子的立体构型为___ 。
(4)金刚石的晶胞结构如图1所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为(0,0,0),则原子2的坐标为___ 。若金刚石的晶胞边长为apm,则其中碳碳键的键长d=___ (用含a的代数式表示)pm。
(5)铁有δ、γ、α三种同素异形体(如图2),三种晶体在不同温度下能发生转化。

①δ、γ、α三种晶体晶胞中铁原子的配位数之比为___ 。
②若δ—Fe晶胞边长为acm,α—Fe晶胞边长为bcm,则两种晶胞空间利用率之比为___ (用含a、b的代数式表示)。
 3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:
3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:(1)基态Fe原子的电子排布式为
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是
(3)CO2分子中σ键和π键的个数之比为
(4)金刚石的晶胞结构如图1所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为(0,0,0),则原子2的坐标为
(5)铁有δ、γ、α三种同素异形体(如图2),三种晶体在不同温度下能发生转化。

①δ、γ、α三种晶体晶胞中铁原子的配位数之比为
②若δ—Fe晶胞边长为acm,α—Fe晶胞边长为bcm,则两种晶胞空间利用率之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】已知X、Y、Z三种元素均为短周期元素,原子序数依次递增,Q、W为前30号元素。5种元素的部分特点:
(1)XF3分子中X的杂化类型为______ ,该分子的空间构型为_______ 。
(2)基态Q原子的电子排布式为_____________________ ,第一电离能:X______ Y(填“>” “<”或“=”)。
(3)X、Y、Z电负性由大到小的顺序为____________ (用元素符号表示)。
(4)Na在Y2中燃烧产物的电子式为________________ 。
(5)Z和X形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于_______ 晶体。
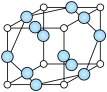
(6)W元素与X元素形成某种化合物的晶胞结构如图所示(黑球代表W原子),若该晶体的密度为ρ g·cm-3,则该晶胞的体积是__________ cm3。
| 元素 | 特点 |
| X | 其气态氢化物呈三角锥形,水溶液显碱性 |
| Y | 基态原子核外有三个能级,其中最外层电子数等于次外层电子数的3倍 |
| Z | 元素原子的外围电子层排布式为nsn-1npn-1 |
| Q | 被誉为“太空金属”、“生物金属”,其基态原子最高能级有3个空轨道 |
| W | 原子M能层为全充满状态且核外的未成对电子只有一个 |
(2)基态Q原子的电子排布式为
(3)X、Y、Z电负性由大到小的顺序为
(4)Na在Y2中燃烧产物的电子式为
(5)Z和X形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于
(6)W元素与X元素形成某种化合物的晶胞结构如图所示(黑球代表W原子),若该晶体的密度为ρ g·cm-3,则该晶胞的体积是

您最近一年使用:0次
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)某同学概括题目信息和掌握的知识分析h的轨道表示式为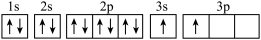 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(2)已知 为离子化合物,写出其电子式
为离子化合物,写出其电子式___________ 。
(3)元素As与___________ 同族(填写以上表中字母对应的元素符号),二者的简单氢化物的稳定性由大到小的顺序是___________ 。
(4)基态p原子成为阳离子时首先失去___________ 轨道电子,基态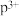 的最外层电子排布式为
的最外层电子排布式为___________ 。
(5)i的最高价氧化物与l的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(6)下列关于涉及元素的说法正确的是___________ (填序号)。
①未成对电子数最多的元素是o ②元素的电负性大小: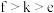
③元素的第一电离能: ④简单离子半径:
④简单离子半径: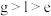
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p |
(1)某同学概括题目信息和掌握的知识分析h的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(2)已知
 为离子化合物,写出其电子式
为离子化合物,写出其电子式(3)元素As与
(4)基态p原子成为阳离子时首先失去
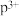 的最外层电子排布式为
的最外层电子排布式为(5)i的最高价氧化物与l的最高价氧化物对应的水化物反应的离子方程式为
(6)下列关于涉及元素的说法正确的是
①未成对电子数最多的元素是o ②元素的电负性大小:
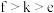
③元素的第一电离能:
 ④简单离子半径:
④简单离子半径: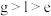
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】已知X、Y、Z、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X是空气中含量最高的元素,Z基态原子核外K、L、M三层电子数之比为1∶4∶2,R基态原子的3d原子轨道上的电子数是4s原子轨道上的4倍,Y基态原子的最外层电子数等于Z、R基态原子的最外层电子数之和。(答题时,X、Y、Z、R用所对应的元素符号表示)
(1)X、Y、Z的第一电离能由小到大的顺序为________ ,写出一种与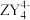 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:________ 。
(2)R3+基态核外电子排布式为________ 。
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是________ 。
(4)Y、Z形成的某晶体的晶胞结构如图所示,则该化合物的化学式为________ 。

(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1mol[R(NH3)6]2+中含有σ键的数目为________ 。
(1)X、Y、Z的第一电离能由小到大的顺序为
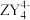 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(2)R3+基态核外电子排布式为
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是
(4)Y、Z形成的某晶体的晶胞结构如图所示,则该化合物的化学式为

(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1mol[R(NH3)6]2+中含有σ键的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、P、Ni、Fe等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.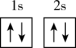 B.
B.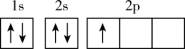
C.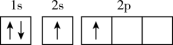 D.
D.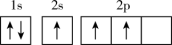
(2)镍能形成多种配合物,其中
 是无色挥发性液体,
是无色挥发性液体,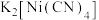 是红黄色单斜晶体。
是红黄色单斜晶体。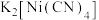 的熔点高于
的熔点高于 的原因是
的原因是
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。
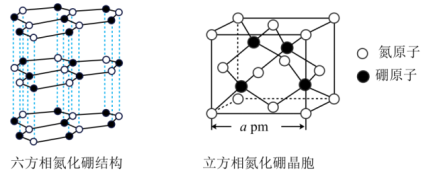
①石墨能导电,六方相氮化硼结构与石墨相似却不导电,原因是
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为
③立方相氮化硼晶胞边长为a pm, 代表阿伏加德罗常数的值,则该晶体的密度为
代表阿伏加德罗常数的值,则该晶体的密度为 。
。
(4)
 的结构如图所示,写出此配合物的内界阳离子
的结构如图所示,写出此配合物的内界阳离子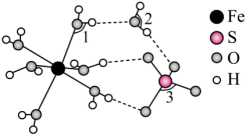
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W、R是原子序数依次增大的前四周期元素。Y原子核外p电子数比s电子数少1;Z原子最外层电子数是其电子层数的3倍,且质子数等于X与Y之和;W的价电子排布式为 ;R位于周期表第5列。
;R位于周期表第5列。
(1)基态W原子中不同运动状态的电子有________ 种;R的价电子轨道表示式为 ________ 。
(2)X2Z2的电子式为____________ 。
(3)Y2Z曾被用作麻醉剂,根据"等电子体原理"预测Y2Z的空间构型为____________ 。
(4)Y2X4常作火箭燃料,其沸点高于Z2的原因是____________ 。
(5)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18.
①下列R的配合物中,满足18电子规则的是____________ 。(填标号)
A. B.
B. 
C. D.
D. 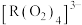
②CO作配体时,配位原子是C而不是O,其原因是____________ 。
 ;R位于周期表第5列。
;R位于周期表第5列。(1)基态W原子中不同运动状态的电子有
(2)X2Z2的电子式为
(3)Y2Z曾被用作麻醉剂,根据"等电子体原理"预测Y2Z的空间构型为
(4)Y2X4常作火箭燃料,其沸点高于Z2的原因是
(5)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18.
①下列R的配合物中,满足18电子规则的是
A.
 B.
B. 
C.
 D.
D. 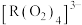
②CO作配体时,配位原子是C而不是O,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氮、磷、砷及其化合物在工农业生产等方面有着重要应用。请按要求回答下列问题。
(1)基态砷原子价电子排布图不能写为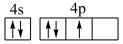 ,是因为该排布方式违背了
,是因为该排布方式违背了___________ 这一原理。
(2)元素第一电离能N___________ P(填“ ”或“
”或“ ”或“
”或“ ”,下同),电负性P
”,下同),电负性P___________ As。
(3)腓( )可用作火箭燃料等,它的沸点远高于乙烯的原因是
)可用作火箭燃料等,它的沸点远高于乙烯的原因是___________ 。
(4)尿素(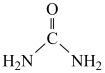 )和
)和 在酸性环境下生成
在酸性环境下生成 、
、 和
和 ,该反应的离子方程式为
,该反应的离子方程式为___________ ; 离子的立体构型(即空间构型)为
离子的立体构型(即空间构型)为___________ 。
(5)GaAs的熔点为1238℃可作半导体材料;而 的熔点为77.9℃。
的熔点为77.9℃。
①预测 的晶体类型为
的晶体类型为___________ 。
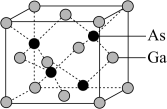
②GaAs晶胞结构如图所示,晶胞边长为a pm。则晶胞中每个Ga原子周围有____ 个紧邻等距的As原子;该晶体的密度为___________  (列出计算式)。
(列出计算式)。
(6)亚砷酸( )可以用于治疗白血病。其在溶液中存在多种微粒形态,将KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液的pH关系如图所示。
)可以用于治疗白血病。其在溶液中存在多种微粒形态,将KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液的pH关系如图所示。
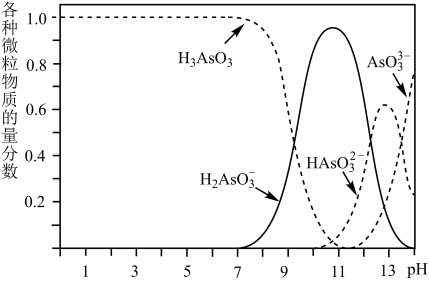
①人体血液的pH在7.35-7.45之间,患者用药后人体中含As元素的主要微粒是___________ 。
② 的第一电离常数
的第一电离常数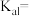
___________ 。
(1)基态砷原子价电子排布图不能写为
 ,是因为该排布方式违背了
,是因为该排布方式违背了(2)元素第一电离能N
 ”或“
”或“ ”或“
”或“ ”,下同),电负性P
”,下同),电负性P(3)腓(
 )可用作火箭燃料等,它的沸点远高于乙烯的原因是
)可用作火箭燃料等,它的沸点远高于乙烯的原因是(4)尿素(
 )和
)和 在酸性环境下生成
在酸性环境下生成 、
、 和
和 ,该反应的离子方程式为
,该反应的离子方程式为 离子的立体构型(即空间构型)为
离子的立体构型(即空间构型)为(5)GaAs的熔点为1238℃可作半导体材料;而
 的熔点为77.9℃。
的熔点为77.9℃。①预测
 的晶体类型为
的晶体类型为②GaAs晶胞结构如图所示,晶胞边长为a pm。则晶胞中每个Ga原子周围有
 (列出计算式)。
(列出计算式)。
(6)亚砷酸(
 )可以用于治疗白血病。其在溶液中存在多种微粒形态,将KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液的pH关系如图所示。
)可以用于治疗白血病。其在溶液中存在多种微粒形态,将KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液的pH关系如图所示。
①人体血液的pH在7.35-7.45之间,患者用药后人体中含As元素的主要微粒是
②
 的第一电离常数
的第一电离常数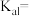
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】青蒿素(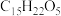 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。

(1)提取青蒿素
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚( )提取,效果更好。
)提取,效果更好。
①乙醚的沸点低于乙醇,原因是_______ 。
②用乙醚提取效果更好,原因是_______ 。
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中C、H、O的原子核附近电子云密度大小:_______ 。
②图中晶胞的棱长分别为a 、b
、b 、c
、c ,晶体的密度为
,晶体的密度为_______  。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)
③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是_______ 。
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
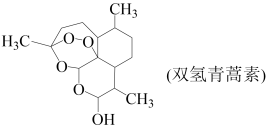
①双氢青蒿素分子中碳原子的杂化轨道类型为_______ 。
② 的空间结构为
的空间结构为_______ 。
双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
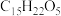 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
(1)提取青蒿素
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚(
 )提取,效果更好。
)提取,效果更好。①乙醚的沸点低于乙醇,原因是
②用乙醚提取效果更好,原因是
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中C、H、O的原子核附近电子云密度大小:
②图中晶胞的棱长分别为a
 、b
、b 、c
、c ,晶体的密度为
,晶体的密度为 。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用
 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
①双氢青蒿素分子中碳原子的杂化轨道类型为
②
 的空间结构为
的空间结构为双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】第一代半导体材料(Si、Ge等) 与第二代半导体材料(GaAs、 InSb等)一起,将人类推进了信息时代。近年来,以碳化硅(SiC)、氮化镓(GaN)为代表的第三代半导体材料的出现,开辟了人类资源和能源节约型社会的新发展,也成为了科学家研究的热点。
(1)N、P、AS位于同一主族,基态氮原子的核外共有___ 种不同运动状态的电子,N2O的空间构型为_______ 。
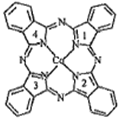
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。 酞菁钻中碳原子的杂化轨道类型为___ ;与钴离子通过配位键结合的氮原子的编号是_______ 。
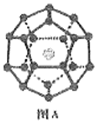
(3)C与N处于同周期相邻元素,C形成的一种重要物质可燃冰是天然气水合物,具有笼形结构如图A (表面的小球是水分子,内部的大球是甲烷分子)。图A 中最小的环中连接的原子总数是_______ 。 可燃冰晶体具有多种笼状结构,其中一种由1个图A所示笼分别用2 个面与另外两个相同的笼共面而成,则中间笼实际占有____ 个水分子。
(4)已知PH3分子的键角约为94%,而AsH3分子的键角约为91.8°,试用价层电子对互斥理论解释PH3的键角比AsH3的键角大的原因________________ 。
(5) 第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有____ 。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示;试从结构的角度分析它们熔点不同的原因__________________ 。
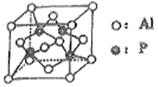
(7)磷化铝晶胞如图所示,若两个铝原子之间的最近距离为dpm,NA代表阿伏伽德罗常数的值,则磷化铝晶体的密度p=_____ g/cm3。
(1)N、P、AS位于同一主族,基态氮原子的核外共有
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。 酞菁钻中碳原子的杂化轨道类型为

(3)C与N处于同周期相邻元素,C形成的一种重要物质可燃冰是天然气水合物,具有笼形结构如图A (表面的小球是水分子,内部的大球是甲烷分子)。图A 中最小的环中连接的原子总数是

(4)已知PH3分子的键角约为94%,而AsH3分子的键角约为91.8°,试用价层电子对互斥理论解释PH3的键角比AsH3的键角大的原因
(5) 第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示;试从结构的角度分析它们熔点不同的原因
| 物质 | BN | AIN | GaN |
| 熔点/℃ | 3000 | 2200 | 1700 |
(7)磷化铝晶胞如图所示,若两个铝原子之间的最近距离为dpm,NA代表阿伏伽德罗常数的值,则磷化铝晶体的密度p=

您最近一年使用:0次



