(1)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的________________ 。
(2)氯化铝溶液具有净水的作用,原因是(用离子方程式表示):_______________ 。
(3)已知CO (g) + H2O (g) CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正
CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正________ v逆(填“>”“<”或“=”)。
(4)将25℃下pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a:b=_____________________ 。
(5)有物质的量浓度相同的盐酸、硫酸、醋酸三种溶液:若三种溶液c(H+)依次为C1、C2、C3,则它们的大小关系为______________
(6)常温下,已知Ksp[M(OH)3] =1.0×10-38,要使溶液中的M3+降至10-5mol/L,则应调节溶液pH=________ 。
(2)氯化铝溶液具有净水的作用,原因是(用离子方程式表示):
(3)已知CO (g) + H2O (g)
 CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正
CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正(4)将25℃下pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a:b=
(5)有物质的量浓度相同的盐酸、硫酸、醋酸三种溶液:若三种溶液c(H+)依次为C1、C2、C3,则它们的大小关系为
(6)常温下,已知Ksp[M(OH)3] =1.0×10-38,要使溶液中的M3+降至10-5mol/L,则应调节溶液pH=
更新时间:2018-07-25 20:56:02
|
相似题推荐
【推荐1】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ⇌CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
回答下列问题:
(1)该反应的平衡常数表达式:_______ 。该反应为_______ 反应(填“吸热”、“放热”)。
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是_______ 。
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3) 能判断该反应是否达到化学平衡状态的依据是_______ (多选不得分)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_______ ℃。
(5)若在(4)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,CO2的物质的量为_______ mol。
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的平衡常数表达式:
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3) 能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(5)若在(4)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,CO2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
①试比较K1、K2的大小,K1___ K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是___ (填序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,2NH3(g) N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=___ (填数值)。
④400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正___ v(N2)逆(填“>”、“<”“=”或“不能确定”)。
⑤若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡___ (填“向左”、“向右”或“不”)移动;使用催化剂__ (填“增大”、“减小”或“不改变”)反应的ΔH。
在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)
 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②下列各项能作为判断该反应达到化学平衡状态的依据是
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,2NH3(g)
 N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=④400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正
⑤若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】COCl2的分解反应为COCl2(g)  Cl2(g)+CO(g) ΔH=+108 kJ·mol-1.反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图乙所示(第10 min到14 min的COCl2浓度变化曲线未标出):
Cl2(g)+CO(g) ΔH=+108 kJ·mol-1.反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图乙所示(第10 min到14 min的COCl2浓度变化曲线未标出):

(1)比较第2 min时反应温度T(2)与第8 min时反应温度T(8)的高低:T(2)___________ (填“<”“>”或“=”)T(8)。
(2)若12 min时反应在温度T(8)下重新达到平衡,则此时c(COCl2)=___________ mol·L-1。
(3)比较产物CO在2~3 min、5~6 min和12~13 min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小:___________ 。
(4)比较反应物COCl2在5~6 min和15~16 min时平均反应速率的大小:v(5~6)___________ (填“<”“>”或“=”)v(15~16),原因是___________ 。
 Cl2(g)+CO(g) ΔH=+108 kJ·mol-1.反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图乙所示(第10 min到14 min的COCl2浓度变化曲线未标出):
Cl2(g)+CO(g) ΔH=+108 kJ·mol-1.反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图乙所示(第10 min到14 min的COCl2浓度变化曲线未标出):
(1)比较第2 min时反应温度T(2)与第8 min时反应温度T(8)的高低:T(2)
(2)若12 min时反应在温度T(8)下重新达到平衡,则此时c(COCl2)=
(3)比较产物CO在2~3 min、5~6 min和12~13 min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小:
(4)比较反应物COCl2在5~6 min和15~16 min时平均反应速率的大小:v(5~6)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】研究电解质在水溶液中的行为有重要的意义(以下均为25℃)。
I.有0.1 mol·L 的三种溶液:a.NaOH b.
的三种溶液:a.NaOH b. c.盐酸
c.盐酸
(1)溶液a的
_______ ;c中水电离出的
_______ 。
(2)溶液b的 ,用化学用语解释原因
,用化学用语解释原因_______ 。
(3) L溶液a与
L溶液a与 L溶液c混合后,若所得溶液的
L溶液c混合后,若所得溶液的 ,则
,则
_______ 。
(4)向20 mL溶液b中滴加溶液a的过程中,pH变化如图所示。
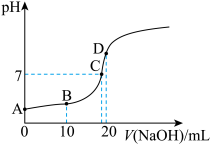
①滴加过程中发生反应的离子方程式是_______ 。
②B点溶液中,离子浓度由大到小的顺序为_______ 。
③D点溶液中,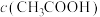
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
II. 、
、 、HClO和
、HClO和 的电离平衡常数如下:
的电离平衡常数如下:
(5)0.1 mol·L 的下列四种溶液,pH由小到大的顺序是_______(填字母)。
的下列四种溶液,pH由小到大的顺序是_______(填字母)。
(6)0.1 mol·L
 的溶液中
的溶液中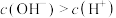 ,结合化学用语解释原因:
,结合化学用语解释原因:_______ 。
(7)向NaClO溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(8)向NaClO溶液中分别加入下列物质,能增大 的是
的是_______ (填字母)。
A. B.
B. C.
C.
I.有0.1 mol·L
 的三种溶液:a.NaOH b.
的三种溶液:a.NaOH b. c.盐酸
c.盐酸(1)溶液a的


(2)溶液b的
 ,用化学用语解释原因
,用化学用语解释原因(3)
 L溶液a与
L溶液a与 L溶液c混合后,若所得溶液的
L溶液c混合后,若所得溶液的 ,则
,则
(4)向20 mL溶液b中滴加溶液a的过程中,pH变化如图所示。

①滴加过程中发生反应的离子方程式是
②B点溶液中,离子浓度由大到小的顺序为
③D点溶液中,
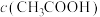
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。II.
 、
、 、HClO和
、HClO和 的电离平衡常数如下:
的电离平衡常数如下:| 化学式 |  |  | HClO |  |
电离平衡常数( ) ) |   | 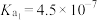  |  |  |
 的下列四种溶液,pH由小到大的顺序是_______(填字母)。
的下列四种溶液,pH由小到大的顺序是_______(填字母)。A. | B. | C.NaClO | D. |

 的溶液中
的溶液中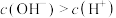 ,结合化学用语解释原因:
,结合化学用语解释原因:(7)向NaClO溶液中通入少量
 ,反应的离子方程式为
,反应的离子方程式为(8)向NaClO溶液中分别加入下列物质,能增大
 的是
的是A.
 B.
B. C.
C.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)1000℃时,硫酸钠与氢气发生下列反应:Na2SO4(s)+4H2(g)  Na2S(s) +4H2O(g)该反应的平衡常数表达式为
Na2S(s) +4H2O(g)该反应的平衡常数表达式为______________ ;已知K1000℃ < K1200℃, 若降低体系温度,混合气体的平均相对分子质量将___________ (填“增大”、“减小”或“不变”)。
(2)常温下,如果取0.1mol·L-1HA溶液与0.1mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化忽略不计),测得混合液的pH=8。混合液中由水电离出的c(OH-)与0.1mol·L-1NaOH溶液中由水电离出的c(OH-)之比为_________ 。
(3)25℃时,将 a mol NH3通入水中得到0.1 mol·L1的氨水,测定其pH约为11,有关的方程式为_____ ,再向该溶液中通入3a mol HCl,溶液中存在的关系式有多种,完成下列关系式(填入恰当的数字):c(H+) =_____ c(NH4+) + _____ c(NH3·H2O) + c(OH-)
(4)工业上用氨水将SO2转化为(NH4)2SO3,再氧化为(NH4)2SO4。已知25 ℃时,0.05 mol·L1 (NH4)2SO4溶液的pH=a,则c(NH4+) ︰c(NH3·H2O)=__________________ (用含a的代数式表示,已知NH3·H2O的电离常数为Kb =1.7 ×103 )
(5)100 ℃时,水的离子积为Kw = 1×10-12,在该温度下,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为____________ (混合后溶液体积的变化忽略不计)。
 Na2S(s) +4H2O(g)该反应的平衡常数表达式为
Na2S(s) +4H2O(g)该反应的平衡常数表达式为(2)常温下,如果取0.1mol·L-1HA溶液与0.1mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化忽略不计),测得混合液的pH=8。混合液中由水电离出的c(OH-)与0.1mol·L-1NaOH溶液中由水电离出的c(OH-)之比为
(3)25℃时,将 a mol NH3通入水中得到0.1 mol·L1的氨水,测定其pH约为11,有关的方程式为
(4)工业上用氨水将SO2转化为(NH4)2SO3,再氧化为(NH4)2SO4。已知25 ℃时,0.05 mol·L1 (NH4)2SO4溶液的pH=a,则c(NH4+) ︰c(NH3·H2O)=
(5)100 ℃时,水的离子积为Kw = 1×10-12,在该温度下,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知水在25℃和95℃时,其电离平衡曲线如图所示:

(1)95℃时水的离子积KW=_____ .
(2)95℃时,0.01mol/LNaOH溶液的PH=_____ .
(3)95℃时水的电离平衡曲线应为___ (填“A”或“B”),请说明理由______________________ .
(4)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为______ .
(5)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是_________________________ .

(1)95℃时水的离子积KW=
(2)95℃时,0.01mol/LNaOH溶液的PH=
(3)95℃时水的电离平衡曲线应为
(4)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(5)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁、钴(Co)、镍(Ni)是同族元素,主要化合价均为+2、+3价,都是较活泼的金属,它们的化合物在工业上有重要的应用.
(1)配制FeSO4溶液时,需加入稀硫酸,其目的是_________________________
(2)写出CoCl2与氯水反应的化学方程式______________________________
(3) Co2+和Fe3+均可与KSCN溶液发生相似的反应,向CoCl2溶液中加入KSCN溶液,生成某种蓝色离子,该离子中钴元素的质量分数约为20%。则该离子的化学式为__________________ 。
(4)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
先向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+,反应的离子方程式有①_____________________ ②NiS+ ClO3-+H+-Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为_________ 。再加入Na2CO3溶液沉镍,即制得碳酸镍,检验Ni2+是否沉淀完全的方法_____________________________________
(1)配制FeSO4溶液时,需加入稀硫酸,其目的是
(2)写出CoCl2与氯水反应的化学方程式
(3) Co2+和Fe3+均可与KSCN溶液发生相似的反应,向CoCl2溶液中加入KSCN溶液,生成某种蓝色离子,该离子中钴元素的质量分数约为20%。则该离子的化学式为
(4)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
先向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+,反应的离子方程式有①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用所学化学反应原理,解决以下问题:
(1)KAl(SO4)2·12H2O可做净水剂,其原理是_________ (用离子方程式表示)
(2)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式_________________ 。
(3)室温下将0.12 mol/L HCl溶液与0.1 mol/L NaOH溶液等体积混合,混合液的pH=_____ 。
(1)KAl(SO4)2·12H2O可做净水剂,其原理是
(2)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式
(3)室温下将0.12 mol/L HCl溶液与0.1 mol/L NaOH溶液等体积混合,混合液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】草酸(H2C2O4)是常见的二元弱酸,0.01 mol/L的H2C2O4溶液中H2C2O4、 、
、 的物质的量分数
的物质的量分数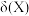 随pH变化如图所示。回答下列问题:
随pH变化如图所示。回答下列问题:

(1)用离子方程式说明Na2C2O4溶液显碱性的原因:_______ 。
(2)根据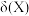 随pH变化图。
随pH变化图。
①反应 的化学平衡常数为
的化学平衡常数为_______ 。
②常温下反应 的平衡常数K=1.0×105,NH3·H2O的电离平衡常数Kb的pKb(-lgKb)值为
的平衡常数K=1.0×105,NH3·H2O的电离平衡常数Kb的pKb(-lgKb)值为_______ 。
(3)0.01 mol/L的NaHCO4溶液中,c(C2O )+c(OH-)=
)+c(OH-)=_______ (填微粒浓度符号);该溶液中离子浓度由大到小的顺序为_______ 。
(4)已知Ksp(CaC2O4)=a。将0.03 mol/L的CaCl2溶液与0.01 mol/L的Na2C2O4溶液等体积混合,混合溶液中 的浓度约为
的浓度约为_______ mol/L。(用含a的代数式表示,混合后溶液体积变化忽略不计)。
 、
、 的物质的量分数
的物质的量分数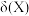 随pH变化如图所示。回答下列问题:
随pH变化如图所示。回答下列问题:
(1)用离子方程式说明Na2C2O4溶液显碱性的原因:
(2)根据
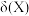 随pH变化图。
随pH变化图。①反应
 的化学平衡常数为
的化学平衡常数为②常温下反应
 的平衡常数K=1.0×105,NH3·H2O的电离平衡常数Kb的pKb(-lgKb)值为
的平衡常数K=1.0×105,NH3·H2O的电离平衡常数Kb的pKb(-lgKb)值为(3)0.01 mol/L的NaHCO4溶液中,c(C2O
 )+c(OH-)=
)+c(OH-)=(4)已知Ksp(CaC2O4)=a。将0.03 mol/L的CaCl2溶液与0.01 mol/L的Na2C2O4溶液等体积混合,混合溶液中
 的浓度约为
的浓度约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Cr2O72-、Cr3+对环境具有极强的污染性,含有Cr2O72-、Cr3+的工业废水常采用NaOH沉淀方法除去。
已知:①常温下,Cr3+完全沉淀(c≤1.0×10−5 mol·L−1) 时,溶液的pH为5;NaOH过量时Cr(OH)3溶解生成CrO2-,②Cr2O72-还原产物为Cr3+。
请回答下列问题:
(1)写出Cr(OH)3溶于NaOH的离子方程式___ 。
(2)常温下,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=___ 。
(3)常温下,向50mL0.005mol·L−1的Cr2(SO4)3溶液中加入0.24mol·L−1的NaOH溶液50mL,充分反应后,溶液pH为___ 。
(4)为了测定工业废水中Na2Cr2O7的浓度,进行如下步骤:
Ⅰ.取100mL滤液;
Ⅱ.用cmol·L−1的标准KMnO4酸性溶液滴定bmL一定浓度的FeSO4溶液,消耗KMnO4溶液bmL;
Ⅲ.取bmL滤液,用上述FeSO4溶液滴定,达到滴定终点时,消耗dmLFeSO4溶液。
①步骤Ⅱ中的滴定过程应选用___ (填“酸式”或“碱式”)滴定管。
②写出步骤Ⅱ中离子反应方程___ 。
已知:①常温下,Cr3+完全沉淀(c≤1.0×10−5 mol·L−1) 时,溶液的pH为5;NaOH过量时Cr(OH)3溶解生成CrO2-,②Cr2O72-还原产物为Cr3+。
请回答下列问题:
(1)写出Cr(OH)3溶于NaOH的离子方程式
(2)常温下,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=
(3)常温下,向50mL0.005mol·L−1的Cr2(SO4)3溶液中加入0.24mol·L−1的NaOH溶液50mL,充分反应后,溶液pH为
(4)为了测定工业废水中Na2Cr2O7的浓度,进行如下步骤:
Ⅰ.取100mL滤液;
Ⅱ.用cmol·L−1的标准KMnO4酸性溶液滴定bmL一定浓度的FeSO4溶液,消耗KMnO4溶液bmL;
Ⅲ.取bmL滤液,用上述FeSO4溶液滴定,达到滴定终点时,消耗dmLFeSO4溶液。
①步骤Ⅱ中的滴定过程应选用
②写出步骤Ⅱ中离子反应方程
您最近一年使用:0次




