甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇。
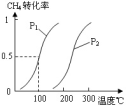
⑴①将1.0 mol CH4和2.0 mol H2O(g)通入容积100L的反应室,一定条件下发生反应:CH4(g) + H2O(g) ⇌ CO(g) + 3H2(g)
Ⅰ,CH4的转化率与温度、压强的关系如图。已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为:_____________ ;
②图中的压强P1_________ P2(填“大于”、“小于”或“等于”),100℃时的平衡常数为:_______ ;
③在其它条件不变的情况下降低温度 ,逆反应 速率将__________ (填“增大”、“减小”或“不变”)。
⑵在压强为0.1 MPa条件下, 将a mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g) + 2H2(g) ⇌ CH3OH(g)
Ⅱ。①若容器容积不变,下列措施可提高甲醇产率的是:________________ ;
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.加入更高效的催化剂
②为了寻找合成甲醇的适宜温度和压强,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中,请帮他完成该表。
表中Ⅰ、Ⅱ、Ⅲ分别为:__________ 、____________ 、____________ 。

⑴①将1.0 mol CH4和2.0 mol H2O(g)通入容积100L的反应室,一定条件下发生反应:CH4(g) + H2O(g) ⇌ CO(g) + 3H2(g)
Ⅰ,CH4的转化率与温度、压强的关系如图。已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为:
②图中的压强P1
③在其它条件不变的情况下
⑵在压强为0.1 MPa条件下, 将a mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g) + 2H2(g) ⇌ CH3OH(g)
Ⅱ。①若容器容积不变,下列措施可提高甲醇产率的是:
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.加入更高效的催化剂
②为了寻找合成甲醇的适宜温度和压强,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中,请帮他完成该表。
| 实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
| A | 150 | 1/3 | 0.1 |
| B | Ⅰ | Ⅱ | 5 |
| C | 350 | 1/3 | Ⅲ |
表中Ⅰ、Ⅱ、Ⅲ分别为:
更新时间:2019-01-09 20:51:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】催化剂在生产和科技领域起到重大作用,某化学研究小组的同学分别设计了如下实验:
(1)用控制变量法比较 和
和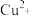 对
对 分解的催化效果。用2.00mol/L的
分解的催化效果。用2.00mol/L的 溶液、0.01mol/L
溶液、0.01mol/L 溶液和0.01mol/L
溶液和0.01mol/L 溶液分别进行下列实验,实验报告如下:
溶液分别进行下列实验,实验报告如下:
①实验1、2研究的是___________ 对 分解速率的影响。
分解速率的影响。
②表中数据a的值应该为___________ ;实验2、3研究的是___________ 对 分解速率的影响。
分解速率的影响。
③定性分析:某同学通过观察实验2、3两支试管产生气泡的快慢,由此得出 和
和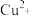 对
对 分解的催化效果,该结论
分解的催化效果,该结论___________ (填“合理”或“不合理”),原因:___________ 。
(2)向50ml 溶液中加入0.10mol
溶液中加入0.10mol 粉末,在标准状况下放出气体的体积和时间的关系如图所示。
粉末,在标准状况下放出气体的体积和时间的关系如图所示。

①实验中放出气体的总体积是___________ mL。
② 的初始物质的量浓度是
的初始物质的量浓度是___________ 。
③a、d两段反应速率大小的顺序为___________ >___________ ,原因:___________ 。
(1)用控制变量法比较
 和
和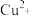 对
对 分解的催化效果。用2.00mol/L的
分解的催化效果。用2.00mol/L的 溶液、0.01mol/L
溶液、0.01mol/L 溶液和0.01mol/L
溶液和0.01mol/L 溶液分别进行下列实验,实验报告如下:
溶液分别进行下列实验,实验报告如下:| 序号 | V( 溶液)/mL 溶液)/mL | V( )溶液)/mL )溶液)/mL | V( )溶液)/mL )溶液)/mL | 反应温度/℃ | V(水)/mL | 结论 |
| 1 | 10 | 1 | 0 | 50 | 9 | |
| 2 | 10 | 1 | 0 | 30 | 9 | |
| 3 | 10 | 0 | 1 | 30 | a |
 分解速率的影响。
分解速率的影响。②表中数据a的值应该为
 分解速率的影响。
分解速率的影响。③定性分析:某同学通过观察实验2、3两支试管产生气泡的快慢,由此得出
 和
和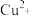 对
对 分解的催化效果,该结论
分解的催化效果,该结论(2)向50ml
 溶液中加入0.10mol
溶液中加入0.10mol 粉末,在标准状况下放出气体的体积和时间的关系如图所示。
粉末,在标准状况下放出气体的体积和时间的关系如图所示。
①实验中放出气体的总体积是
②
 的初始物质的量浓度是
的初始物质的量浓度是③a、d两段反应速率大小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。
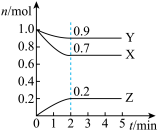
根据图中数据填空:
(1)该反应的化学方程式为_______ 。
(2)反应开始至2min,以气体Z表示的平均反应速率为_______ 。平衡时X的转化率为_______ 。
(3)下列叙述能证明该反应已经达到化学平衡状态的是_______(填序号)。
(4)2min末反应达到平衡,向容器内充入一定量的X,平衡将_______ 移动;增大压强,平衡将_______ 移动;向体系内加催化剂,平衡将_______ 移动(填“正向”“逆向”或“不”)。

根据图中数据填空:
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)下列叙述能证明该反应已经达到化学平衡状态的是_______(填序号)。
| A.Y的体积分数不再发生变化 |
| B.容器内气体压强不再发生变化 |
| C.v(X)∶v(Y)=3∶1 |
| D.单位时间内消耗3n mol X同时生成2n mol Z |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)⇌2NO(g) ΔH>0,已知该反应在240℃,平衡常数K=6.4×10-3。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率___________ 。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志___________。
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是___________ (填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数___________ 。(填“变大”、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应___________ (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是___________ 。
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志___________。
| A.消耗1molN2同时生成1molO2 | B.混合气体密度不变 |
| C.混合气体平均相对分子质量不变 | D.2v正(N2)=v逆(NO) |

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】汽车尾气中含有CO、NO等有害气体。
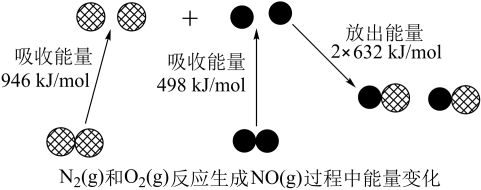
(1)汽车尾气中NO生成过程的能量变化如图所示。1molN2和1molO2完全反应生成NO会___________ (选填“吸收”或“放出”)___________ kJ能量。
(2)一种新型催化剂用于NO和CO的反应: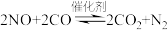 。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
①请将表中数据补充完整:a为___________ 。
②能验证温度对化学反应速率影响规律的是实验___________ (填实验序号)。
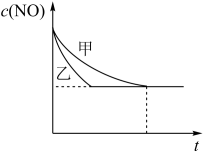
③实验I和实验II中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线___________ (选填“甲”或“乙”)。
(1)汽车尾气中NO生成过程的能量变化如图所示。1molN2和1molO2完全反应生成NO会

(2)一种新型催化剂用于NO和CO的反应:
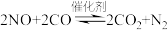 。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。| 实验编号 | t(℃) | NO初始浓度(mol/L) | CO初始浓度(mdl/L) | 催化制的比表面积(m2/g) |
| I | 280 |  |  | 82 |
| II | 280 |  | b | 124 |
| III | 350 | a | 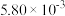 | 82 |
①请将表中数据补充完整:a为
②能验证温度对化学反应速率影响规律的是实验
③实验I和实验II中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】认识化学反应的快慢和限度规律及影响因素,通过调控更好地满足工农业生产和日常生活的实际需要。
Ⅰ.根据所学知识,完成下列各题:
(1)决定化学反应速率的内在因素是_______。
(2)下列过程中,需要加快反应速率的是_______。
Ⅱ.用相同质量的锌片和铜粉跟相同浓度的足量的稀盐酸反应,得到的实验数据如下表所示:
(3)实验①和②表明_______ ,化学反应速率越快。
(4)能表明固体的表面积对反应速率有影响的实验编号是_______ 。
(5)该实验的目的是探究_______ 等因素对锌和稀盐酸反应速率的影响。
(6)请设计一个实验方案探究盐酸的浓度对反应速率的影响。_______
(7)对于2HBr(g) H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
(8)对于平衡体系:FeCl3+3KSCN Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Ⅲ.牙齿表面被一层坚硬的名叫羟基磷酸钙的物质保护着,该物质的组成为Ca5(PO4)3OH,它在唾液中存在下列平衡:Ca5(PO4)3OH(s) 5Ca2+(aq)+3
5Ca2+(aq)+3 (aq)+OH-(aq)
(aq)+OH-(aq)
(9)口腔中的细菌和酶在消化分解食物时,会产生有机酸,从而使羟基磷酸钙溶解。若不及时处理,最终会使牙齿产生蛀洞。适用化学平衡知识解释酸使羟基磷酸钙溶解的原因。_______
Ⅰ.根据所学知识,完成下列各题:
(1)决定化学反应速率的内在因素是_______。
| A.温度和压强 | B.反应物的浓度 |
| C.反应物自身的性质 | D.催化剂 |
| A.钢铁腐蚀 | B.食物腐败 | C.炼钢 | D.塑料老化 |
Ⅱ.用相同质量的锌片和铜粉跟相同浓度的足量的稀盐酸反应,得到的实验数据如下表所示:
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| ① | 薄片 | 15 | 200 |
| ② | 薄片 | 25 | 90 |
| ③ | 粉末 | 25 | 10 |
(4)能表明固体的表面积对反应速率有影响的实验编号是
(5)该实验的目的是探究
(6)请设计一个实验方案探究盐酸的浓度对反应速率的影响。
(7)对于2HBr(g)
 H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。A. | B. | C. | D. |
 Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)| A.其他条件不变,增大FeCl3溶液浓度,溶液的血红色加深 |
| B.其他条件不变,增大KSCN溶液的浓度,平衡正向移动 |
| C.其他条件不变,加入一定量的KCl固体,平衡逆向移动,溶液颜色变浅 |
| D.其他条件不变,加入少量的铁粉,振荡,溶液颜色变浅 |
Ⅲ.牙齿表面被一层坚硬的名叫羟基磷酸钙的物质保护着,该物质的组成为Ca5(PO4)3OH,它在唾液中存在下列平衡:Ca5(PO4)3OH(s)
 5Ca2+(aq)+3
5Ca2+(aq)+3 (aq)+OH-(aq)
(aq)+OH-(aq)(9)口腔中的细菌和酶在消化分解食物时,会产生有机酸,从而使羟基磷酸钙溶解。若不及时处理,最终会使牙齿产生蛀洞。适用化学平衡知识解释酸使羟基磷酸钙溶解的原因。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】二甲醚( )是一种清洁能源,可由合成气(
)是一种清洁能源,可由合成气( 、
、 )来制备,反应原理如下:
)来制备,反应原理如下:
反应Ⅰ: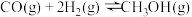

反应Ⅱ: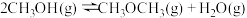

回答下列问题:
(1)上述反应符合“原子经济性”原则的是__________ (填“反应Ⅰ”或“反应Ⅱ”)。
(2)图中使曲线 对应反应按曲线
对应反应按曲线 进行的措施是
进行的措施是__________ ,由合成气( 、
、 )制备
)制备 的热化学方程式为
的热化学方程式为__________ ,该反应自发进行的条件为_________ (填“低温”或“高温”)。

(3)模拟该制备原理,起始时在某容器中充入 和
和 合成
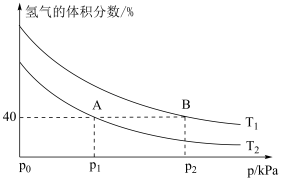
合成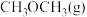 ,平衡时混合物中氢气的体积分数与温度、压强的关系如图所示:
,平衡时混合物中氢气的体积分数与温度、压强的关系如图所示:
①下列有关说法能够证明恒温恒压时,反应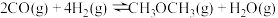
 一定达到平衡状态的是
一定达到平衡状态的是__________ (填序号)。
 .
. 和
和 的转化率相等
的转化率相等
 .反应体系中混合气体密度保持不变
.反应体系中混合气体密度保持不变
 .
. 的值保持不变
的值保持不变
 .反应体系压强保持不变
.反应体系压强保持不变
②图中
________  (填“>”“<”或“=”);理由是
(填“>”“<”或“=”);理由是____________ 。
③在 、
、 两点对应的条件下,该反应从开始到平衡时生成二甲醚的平均速率:
两点对应的条件下,该反应从开始到平衡时生成二甲醚的平均速率: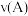
_____ 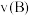 。
。
④ 点对应的
点对应的
_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 )是一种清洁能源,可由合成气(
)是一种清洁能源,可由合成气( 、
、 )来制备,反应原理如下:
)来制备,反应原理如下:反应Ⅰ:
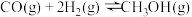

反应Ⅱ:
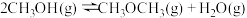

回答下列问题:
(1)上述反应符合“原子经济性”原则的是
(2)图中使曲线
 对应反应按曲线
对应反应按曲线 进行的措施是
进行的措施是 、
、 )制备
)制备 的热化学方程式为
的热化学方程式为
(3)模拟该制备原理,起始时在某容器中充入
 和
和 合成
合成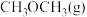 ,平衡时混合物中氢气的体积分数与温度、压强的关系如图所示:
,平衡时混合物中氢气的体积分数与温度、压强的关系如图所示:
①下列有关说法能够证明恒温恒压时,反应
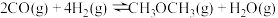
 一定达到平衡状态的是
一定达到平衡状态的是 .
. 和
和 的转化率相等
的转化率相等 .反应体系中混合气体密度保持不变
.反应体系中混合气体密度保持不变 .
. 的值保持不变
的值保持不变 .反应体系压强保持不变
.反应体系压强保持不变②图中

 (填“>”“<”或“=”);理由是
(填“>”“<”或“=”);理由是③在
 、
、 两点对应的条件下,该反应从开始到平衡时生成二甲醚的平均速率:
两点对应的条件下,该反应从开始到平衡时生成二甲醚的平均速率: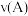
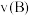 。
。④
 点对应的
点对应的
您最近一年使用:0次
【推荐1】氮有不同价态的氧化物,如NO、N2O3、NO2等,它们在一定条件下可以相互转化。
(1)某温度下,在一体积可变的密闭容器中充入1molN2O3,发生反应N2O3⇌NO2(g)+NO(g),达到平衡后,于t1时刻改变某一条件后,速率与时间的变化图象如图1所示,有关说法
正确的是____

A.t1时刻改变的条件是增大N2O3的浓度,同时减小NO2或NO的浓度
B.t1时刻改变条件后,平衡向正反应方向移动,N2O3的转化率增大
C.在t2时刻达到新的平衡后,NO2的百分含量不变
D.若t1时刻将容器的体积缩小至原容积的一半,则速率~时间图象与上图相同
(2)在1000K下,在某恒容容器中发生下列反应:2NO2(g)⇌2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率α(NO2)随温度变化如图所示。
图2中a点对应温度下。已知NO2的起始压强P0为120kPa,列式计算该温度下反应的平衡常数Kp=______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)对于反应N2O4(g)⇌2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2•p2(NO2).其中,k1、k2是与反应及温度有关的常数。相应的速率﹣压强关系如图所示:一定温度下,k1、k2与平衡常数Kp间的关系是k1=_____ ;在图3标出点中,指出能表示反应达到平衡状态的两个点_____ ,理由是____________________________ 。
(1)某温度下,在一体积可变的密闭容器中充入1molN2O3,发生反应N2O3⇌NO2(g)+NO(g),达到平衡后,于t1时刻改变某一条件后,速率与时间的变化图象如图1所示,有关说法
正确的是

A.t1时刻改变的条件是增大N2O3的浓度,同时减小NO2或NO的浓度
B.t1时刻改变条件后,平衡向正反应方向移动,N2O3的转化率增大
C.在t2时刻达到新的平衡后,NO2的百分含量不变
D.若t1时刻将容器的体积缩小至原容积的一半,则速率~时间图象与上图相同
(2)在1000K下,在某恒容容器中发生下列反应:2NO2(g)⇌2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率α(NO2)随温度变化如图所示。
图2中a点对应温度下。已知NO2的起始压强P0为120kPa,列式计算该温度下反应的平衡常数Kp=
(3)对于反应N2O4(g)⇌2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2•p2(NO2).其中,k1、k2是与反应及温度有关的常数。相应的速率﹣压强关系如图所示:一定温度下,k1、k2与平衡常数Kp间的关系是k1=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在容积为1L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
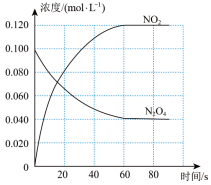
(1)反应的△H______ 0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为________ mol·L-1·s-1
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,10s又达到平衡。T_______ 100℃(填“大于”“小于”)。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向_______ (填“正反应”或“逆反应”)方向移动
(4)再次到达平衡后,向容器中加入合适的正催化剂,则v正_______ v逆_______ ,(填“增大”、“减小”或“不变”),体系的颜色_______ (填“变深” “变浅”或“不变”)。
 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的△H
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,10s又达到平衡。T
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向
(4)再次到达平衡后,向容器中加入合适的正催化剂,则v正
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一定条件下,反应室(容积恒定为2 L)中有反应:A(g)+2B(g)=C(g)。
(1)能说明上述反应达到平衡状态的是________ (填字母,下同)。
A.反应中A与B的物质的量浓度之比为1∶2
B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化
D.2v正(A)=v逆(B)
(2)1 mol A(g)与2 mol B(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:
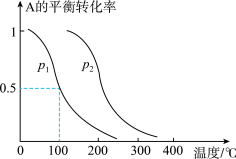
①p1________ (填“<”、“>”或“=”,下同)p2,正反应的ΔH________ 0。
②下列措施中一定能使c(C)/c(A)增大的是________ 。
A.升高温度 B.恒温恒容再充入A
C.恒温恒容再充入B D.恒温恒容再充入1 mol C
(3)100 ℃时将1 mol A和2 mol B通入反应室,保持温度不变,10 min末C(g)的浓度为0.05 mol·L-1,则10 min末B的转化率为________ ,此时v正_______ v逆(填“<”、“>”或“=”)。
(1)能说明上述反应达到平衡状态的是
A.反应中A与B的物质的量浓度之比为1∶2
B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化
D.2v正(A)=v逆(B)
(2)1 mol A(g)与2 mol B(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①p1
②下列措施中一定能使c(C)/c(A)增大的是
A.升高温度 B.恒温恒容再充入A
C.恒温恒容再充入B D.恒温恒容再充入1 mol C
(3)100 ℃时将1 mol A和2 mol B通入反应室,保持温度不变,10 min末C(g)的浓度为0.05 mol·L-1,则10 min末B的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)⇌PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,回答下列问题:
(1)反应在前50s—250s内的用PCl5表示平均速率为___________
(2)该反应的平衡常数K=___________ 。
(3)体系平衡时与反应起始时的压强之比为___________
(4)其它条件均不变,在上述平衡体系中再加入1.0molPCl5,达到新平衡时n(PCl3)_____ 0.4mol(填>,<,=)
(5)相同温度下,起始时向容器中充入0.6molPCl5、0.20molPCl3和0.20molCl2,反应达到平衡前v(正)_________ v(逆)(填>,<,=)
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
(1)反应在前50s—250s内的用PCl5表示平均速率为
(2)该反应的平衡常数K=
(3)体系平衡时与反应起始时的压强之比为
(4)其它条件均不变,在上述平衡体系中再加入1.0molPCl5,达到新平衡时n(PCl3)
(5)相同温度下,起始时向容器中充入0.6molPCl5、0.20molPCl3和0.20molCl2,反应达到平衡前v(正)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】恒温恒压下,在一个可变容积的容器中发生如下反应: A(g) + B(g) C(g)
C(g)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的
量为_____________ mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为_______ mol
(3)若开始时放入xmolA、2molB和1molC,到达平衡后,C的物质的量是3amol,x=________ mol.
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量是_____ mol.
 C(g)
C(g)(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的
量为
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为
(3)若开始时放入xmolA、2molB和1molC,到达平衡后,C的物质的量是3amol,x=
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业合成氨技术反应原理为:N2(g)+3H2(g)  2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-1
(1)T℃时,在有催化剂、体积为1.0L的恒容密闭容器中充入3molH2、1molN2,10min时反应达到平衡,测得c(NH3)=1.2mol L-1。
L-1。
①前10min的平均反应速率v(H2)=___________ mol L-1
L-1 min-1
min-1
②若反应起始时向容器中充入3molH2、1molN2和2molNH3,该反应向哪个方向进行?请结合数据说明你的进行说明___________ 。
(2)T℃时,在有催化剂的恒容密闭容器中充入N2和H2。如图为不同投料比[n(H2)/n(N2)]时某反应物X的平衡转化率变化曲线。_______ (填"N2"或"H2")。
②判断依据是_______ 。
(3)在其他条件相同时,如图为分别测定不同压强、不同温度下,N2的平衡转化率。L表示______ ,其中X1_____ X2(填“>”或“<”)。
 2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-1(1)T℃时,在有催化剂、体积为1.0L的恒容密闭容器中充入3molH2、1molN2,10min时反应达到平衡,测得c(NH3)=1.2mol
 L-1。
L-1。①前10min的平均反应速率v(H2)=
 L-1
L-1 min-1
min-1②若反应起始时向容器中充入3molH2、1molN2和2molNH3,该反应向哪个方向进行?请结合数据说明你的进行说明
(2)T℃时,在有催化剂的恒容密闭容器中充入N2和H2。如图为不同投料比[n(H2)/n(N2)]时某反应物X的平衡转化率变化曲线。
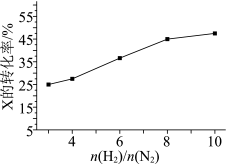
②判断依据是
(3)在其他条件相同时,如图为分别测定不同压强、不同温度下,N2的平衡转化率。L表示

您最近一年使用:0次



