常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合后所得溶液的pH如下表:
请回答:
(1)从①组实验分析,HA是强酸还是弱酸_______ 。
(2)②组实验表明,c____ 0.2(填“大于”“小于”或“等于”)。混合液中离子浓度c(A-)与c(Na+)的大小关系是c(A-)_____ c(Na+)(填“大于”“小于”或“等于”)。
(3)从③组实验结果分析,说明HA的电离程度_____ NaA的水解程度(填“大于”“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是__________ 。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=______ mol·L-1。写出该混合溶液中下列表达式的计算结果:c(Na+)-c(A-)=__ mol·L-1;c(OH-)-c(HA)=____ mol·L-1。
| 实验编号 | HA的物质的量浓度/(mol·L-1) | NaOH的物质的量浓度/(mol·L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
请回答:
(1)从①组实验分析,HA是强酸还是弱酸
(2)②组实验表明,c
(3)从③组实验结果分析,说明HA的电离程度
(4)①组实验所得混合溶液中由水电离出的c(OH-)=
2016高二·全国·课时练习 查看更多[5]
(已下线)练习11 盐类的水解-2020-2021学年【补习教材·寒假作业】高二化学(人教版)浙江省宁波市北仑中学2019-2020学年高二上学期期中考试化学(2-10班)试题宁夏回族自治区长庆高级中学2018-2019学年高二上学期期末考试化学试题高中化学人教版 选修四 第三章 水溶液中的离子反应 第三节 盐类的水解 盐类的水解第二课时(盐类的水解的影响因素和应用)(已下线)同步君 选修4 第3章 第3节 盐类水解的影响因素
更新时间:2019-01-18 01:17:01
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】(1)25 ℃时,0.05 mol·L-1 H2SO4溶液的pH=___ ,0.01 mol·L-1 NaOH溶液的pH=___ 。
(2)某温度下,纯水中的c(H+)=2.0×10-7 mol·L-1,则此时溶液的c(OH-)是____ mol·L-1,这种水显____ (填“酸”“碱”或“中”)性,其理由是_____ ;若温度不变,滴入稀盐酸使c(H+)=5.0×10-6 mol·L-1,则c(OH-)=__ mol·L-1。
(3)25℃时,将25 mL 12 mol·L-1的盐酸与100 mL 2 mol·L-1的NaOH溶液混合后,再稀释至1 L,该溶液的pH是___ ,其中由水电离产生的c(H+)是___ 。
(4)10mLpH=4的盐酸,稀释10倍到100mL时,pH=__________ 。常温下,pH=5和pH=3的盐酸溶液等体积混合后溶液的pH=_________ 。
(5)某温度(t℃)时,水的KW=10-13,则该温度(填大于、等于或小于)______ 25℃,理由是_________________________________________________ ,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,若所得混合溶液为中性,则a:b=_________ ;若所得混合溶液pH=2,则a:b=__________ 。
(2)某温度下,纯水中的c(H+)=2.0×10-7 mol·L-1,则此时溶液的c(OH-)是
(3)25℃时,将25 mL 12 mol·L-1的盐酸与100 mL 2 mol·L-1的NaOH溶液混合后,再稀释至1 L,该溶液的pH是
(4)10mLpH=4的盐酸,稀释10倍到100mL时,pH=
(5)某温度(t℃)时,水的KW=10-13,则该温度(填大于、等于或小于)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】实验表明,液体时纯硫酸的电离能力强于纯硝酸,纯硫酸的导电性强于纯水;又知液态电解质都能像水一样自身电离,而建立电离平衡(即像2H2O H3O++OH-),且在一定温度下都有各自的离子积常数.
H3O++OH-),且在一定温度下都有各自的离子积常数.
据此回答下列问题:
(1)纯硫酸在液态时,自身电离的电离反应方程式是____________________ ,它在25℃时的离子积常数K(H2SO4)比水的离子积常数K(H2O)[K(H2O)=c(H+)·c(OH-)]________ (填“大”“小”或“相等”).
(2)在纯硫酸与纯硝酸的液态混合物中,存在的阴离子主要是________ ;这是因为混合液中不但存在两种电离平衡(即H2SO4和HNO3各自的电离平衡,且硫酸的酸性强于硝酸),又在无水的条件下,混合酸中必发生____________________ (写离子反应方程式)反应而造成的.
 H3O++OH-),且在一定温度下都有各自的离子积常数.
H3O++OH-),且在一定温度下都有各自的离子积常数.据此回答下列问题:
(1)纯硫酸在液态时,自身电离的电离反应方程式是
(2)在纯硫酸与纯硝酸的液态混合物中,存在的阴离子主要是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】现对0.1 mol/L的纯碱溶液进行相关研究。
(1)用pH试纸测定该溶液的pH,其正确的操作__________________ 。
(2)纯碱溶液呈碱性的原因是(用离子方程式表示)___________________ 。
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32—离子不超过其总量10%。请你设计实验证明该同学的观点是否正确。___________________________ 。
(4)某同学根据所学知识对溶液进行分析,写出了以下四个关系式。请你判断:在正确的关系式后面打“ ”,在错误的后面写出正确的关系式。
”,在错误的后面写出正确的关系式。
①c(Na+)=2[c(CO32-)+c(HCO3-)]:_________________________________ ;
②c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-):___________________ ;
③c(OH-)=c(H+)+c(HCO3-)+c(H2CO3):__________________________ ;
④c(Na+)>c(CO32-)>c(OH-)>c(HCO3-):______________________________ 。
(1)用pH试纸测定该溶液的pH,其正确的操作
(2)纯碱溶液呈碱性的原因是(用离子方程式表示)
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32—离子不超过其总量10%。请你设计实验证明该同学的观点是否正确。
(4)某同学根据所学知识对溶液进行分析,写出了以下四个关系式。请你判断:在正确的关系式后面打“
 ”,在错误的后面写出正确的关系式。
”,在错误的后面写出正确的关系式。①c(Na+)=2[c(CO32-)+c(HCO3-)]:
②c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-):
③c(OH-)=c(H+)+c(HCO3-)+c(H2CO3):
④c(Na+)>c(CO32-)>c(OH-)>c(HCO3-):
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】请回答下列问题
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是________ (填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是________ (填字母)。
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是_______ (填字母)。
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是__________ (用序号连接)
(3)对于2NO2(g) N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是____ 。

①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是
(3)对于2NO2(g)
 N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】回答下列问题:
(1)①25℃时,三种弱电解质的电离平衡常数如表:
下列方法中,可以使0.10mol•L-1CH3COOH溶液中CH3COOH电离程度增大的是____ 。
a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
②常温下,0.1mol•L-1的NH3•H2O溶液加水稀释过程,下列表达式的数据一定变小的是____ 。
a.c(OH-) b. c.c(H+)•c(OH-) d.
c.c(H+)•c(OH-) d.
(2)常温下,有pH相同、体积相同的a.CH3COOH溶液和b.HCl溶液,现采取以下措施:
①分别加适量醋酸钠晶体后,CH3COOH溶液中c(H+)____ (填“增大”“减小”或“不变”,下同),HCl溶液中c(H+)____ 。
②分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:CH3COOH溶液____ (填“>”“=”或“<”)HCl溶液。
③温度都升高20℃,CH3COOH溶液中c(H+)____ (填“>”“<”或“=”)HCl溶液中c(H+)。
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是____ (填字母)。(①表示盐酸,②表示醋酸)
a.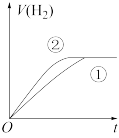 b.
b.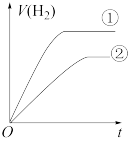 c.
c. 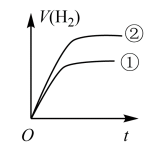 d.
d.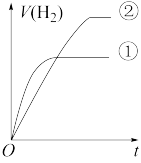
(3)将0.1mol•L-1的CH3COOH溶液加水稀释,下列有关稀释后CH3COOH溶液的说法正确的是____ 。
(1)①25℃时,三种弱电解质的电离平衡常数如表:
| 化学式 | HCOOH | CH3COOH | NH3•H2O |
| 电离平衡常数 | 1.77×10-4 | 1.75×10-5 | 1.76×10-5 |
a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
②常温下,0.1mol•L-1的NH3•H2O溶液加水稀释过程,下列表达式的数据一定变小的是
a.c(OH-) b.
 c.c(H+)•c(OH-) d.
c.c(H+)•c(OH-) d.
(2)常温下,有pH相同、体积相同的a.CH3COOH溶液和b.HCl溶液,现采取以下措施:
①分别加适量醋酸钠晶体后,CH3COOH溶液中c(H+)
②分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:CH3COOH溶液
③温度都升高20℃,CH3COOH溶液中c(H+)
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
a.
 b.
b. c.
c.  d.
d.
(3)将0.1mol•L-1的CH3COOH溶液加水稀释,下列有关稀释后CH3COOH溶液的说法正确的是
| A.电离程度增大 | B.溶液中离子总数增多 |
| C.溶液导电性增强 | D.溶液中醋酸分子增多 |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】(1)现有以下物质:①NaCl晶体②SO2③液态醋酸④铜⑤固体BaSO4⑥纯蔗糖C12H22O11)⑦酒精(C2H5OH)⑧熔化的KHSO4⑨氨水⑩液氯。请回答下列问题。(填相应序号)
I、以上物质能导电的是______ ;
II、以上物质属于非电解质的是______ ;
III、以上物质属于强电解质的是______ ;
(2)写出⑧的电离方程式:______ 。
(3)常温下0.1mol/L的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是______
A.c(H+) B.c(H+)/c(CH3COOH) C.c(OH−) D.c(H+)/c(OH−)
I、以上物质能导电的是
II、以上物质属于非电解质的是
III、以上物质属于强电解质的是
(2)写出⑧的电离方程式:
(3)常温下0.1mol/L的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+) B.c(H+)/c(CH3COOH) C.c(OH−) D.c(H+)/c(OH−)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】回答下列问题
(1)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显___________ (填“酸”“碱”或“中”)性,c(CN-)___________ (填“>”“<”或“=”)c(HCN)。该溶液中各离子浓度由大到小的顺序为___________ 。
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=___________ (小数点后保留4位数字)。
(2)向氨水中加入0.05 mol·L-1稀硫酸至溶液正好呈中性,则c(NH )
)___________ (填“>”“<”或“=”)2c( ),此时混合溶液中c(NH
),此时混合溶液中c(NH )=176c(NH3·H2O),则NH3·H2O的电离常数Kb为
)=176c(NH3·H2O),则NH3·H2O的电离常数Kb为___________ 。
(1)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=
(2)向氨水中加入0.05 mol·L-1稀硫酸至溶液正好呈中性,则c(NH
 )
) ),此时混合溶液中c(NH
),此时混合溶液中c(NH )=176c(NH3·H2O),则NH3·H2O的电离常数Kb为
)=176c(NH3·H2O),则NH3·H2O的电离常数Kb为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸:______ 。
(2)不考虑其他组的实验结果,单从乙组情况分析,c1是否一定等于0.2 mol·L-1?______ (选填“是”或“否”)。混合溶液中离子浓度c(A-)与c(Na+)的大小关系是______ 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是______ 酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是______ 。
(4)写出丁组实验所得混合溶液中下列算式的精确结果(不能做近似计算)。
c(Na+)-c(A-)=______ mol·L-1;
c(OH-)-c(HA)=______ mol·L-1.
| 实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c1 | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸:
(2)不考虑其他组的实验结果,单从乙组情况分析,c1是否一定等于0.2 mol·L-1?
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是
(4)写出丁组实验所得混合溶液中下列算式的精确结果(不能做近似计算)。
c(Na+)-c(A-)=
c(OH-)-c(HA)=
您最近一年使用:0次
【推荐3】25℃时,HA的电离常数是1.75×10-5,按要求回答下列问题。
(1)用水稀释 0.1mol/L的HA溶液时,溶液中随着水量的增加,平衡将_______ 移动(填“向右”、“向左”或“不”),HA的电离程度将_______ (填“增大”、“减小”或“不变”),溶液中c(OH-)将_______ (填“增大”、“减小”或“不变”)。
(2)写出①Na3PO4的电荷守恒_______
②NaH2PO4的物料守恒_______
③Na2HPO4的质子守恒_______
④比较Na2HPO4离子浓度大小_______
(3)氯铝电池是一种新型的燃料电池。试回答下列问题:
①通入Cl2(g)的电极是_______ (填“正”或“负”)极。
②通入Al(s)的电极是_______ (填“正”或“负”)极。
③电子从_______ (填“Al”或“Cl2”)极流向_______ 极(填“正”或“负”)。
④每消耗8.1 g Al(s),电路中通过的电子数目为_______ NA(NA表示阿伏加德罗常数的值)。
(1)用水稀释 0.1mol/L的HA溶液时,溶液中随着水量的增加,平衡将
(2)写出①Na3PO4的电荷守恒
②NaH2PO4的物料守恒
③Na2HPO4的质子守恒
④比较Na2HPO4离子浓度大小
(3)氯铝电池是一种新型的燃料电池。试回答下列问题:
①通入Cl2(g)的电极是
②通入Al(s)的电极是
③电子从
④每消耗8.1 g Al(s),电路中通过的电子数目为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】Ⅰ.NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1 mol·L-1NH4Al(SO4)2溶液中c((NH4+)_________ (填“等于”、“大于”或“小于”) 0.1 mol·L-1NH4HSO4溶液中c(NH4+)
(2)如图是0.1 mol·L-1电解质溶液的pH随温度变化的图象。
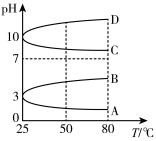
①其中符合0.1 mol·L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是______ (填字母)。
②室温时,0.1 mol·L-1NH4Al(SO4)2溶液中2c(SO42-)- c(NH4+)-3c(Al3+)=________ mol·L-1
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
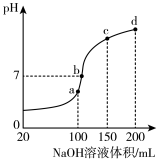
试分析图中a、b、c、d四个点,水的电离程度最大的是____________ ; 在b点,溶液中各离子浓度由大到小的排列顺序是___________________ 。
Ⅱ.pC是指极稀溶液中溶质物质的量浓度的常用对数负值,类似pH。
已知H2CO3溶液中存在下列平衡:CO2+H2O H2CO3 H2CO3
H2CO3 H2CO3 H+ + HCO3- HCO3-
H+ + HCO3- HCO3- H+ + CO32—图为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后达到平衡时溶液中三种成分的pC-pH图。
H+ + CO32—图为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后达到平衡时溶液中三种成分的pC-pH图。
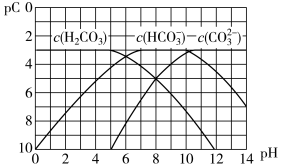
(4)在pH=11时,H2CO3溶液中浓度最大的含碳元素的离子为__________ 。
(5)由图可知,碳酸的一级电离常数Ka1大约为______
(1)相同条件下,0.1 mol·L-1NH4Al(SO4)2溶液中c((NH4+)
(2)如图是0.1 mol·L-1电解质溶液的pH随温度变化的图象。

①其中符合0.1 mol·L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
②室温时,0.1 mol·L-1NH4Al(SO4)2溶液中2c(SO42-)- c(NH4+)-3c(Al3+)=
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。

试分析图中a、b、c、d四个点,水的电离程度最大的是
Ⅱ.pC是指极稀溶液中溶质物质的量浓度的常用对数负值,类似pH。
已知H2CO3溶液中存在下列平衡:CO2+H2O
 H2CO3 H2CO3
H2CO3 H2CO3 H+ + HCO3- HCO3-
H+ + HCO3- HCO3- H+ + CO32—图为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后达到平衡时溶液中三种成分的pC-pH图。
H+ + CO32—图为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后达到平衡时溶液中三种成分的pC-pH图。
(4)在pH=11时,H2CO3溶液中浓度最大的含碳元素的离子为
(5)由图可知,碳酸的一级电离常数Ka1大约为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】亚磷酸(H3PO3)为二元酸,其酸性比磷酸稍强,可用作农药中间体以及有机磷水处理药剂的原料。回答下列问题:
(1)Na2HPO3属于_________ (填“正盐”、“酸式盐”或“无法确定”)。设计一种实验方案, 证明亚磷酸不是强酸:___________ 。
(2)某温度下, H3PO3的电离平衡常数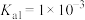 ,
,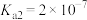 。则NaH2PO3中,
。则NaH2PO3中,
______ 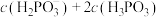 (填“>”、 “<”或“=”)。
(填“>”、 “<”或“=”)。
(1)Na2HPO3属于
(2)某温度下, H3PO3的电离平衡常数
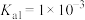 ,
,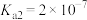 。则NaH2PO3中,
。则NaH2PO3中,
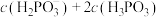 (填“>”、 “<”或“=”)。
(填“>”、 “<”或“=”)。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】研究硫元素及其化合物的性质具有重要意义。
(1)25℃,向0.10mol/LH2S溶液中通入HCl气体或加入NaOH固体调节溶液的pH,溶液的pH与c(S2-)的关系如图所示(忽略溶液体积的变化、H2S的挥发)。
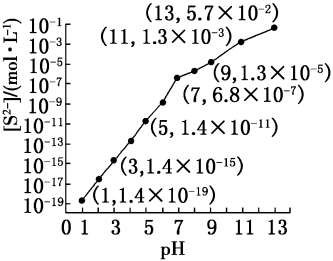
①pH=13时,溶液中的c(H2S)+c(HS-)=___ mol/L。
②pH=7时,c(Na+)___ c(H2S)+c(HS-)+c(S2-)(填“>”、“<”或“=”)。[已知:Ka1(H2S)=1.1×10-7,Ka2(H2S)=1.3×10-13]
③某溶液含0.0040mol/LMn2+、0.0040mol/LFe2+、0.10mol/LH2S,当溶液pH=___ 时,Fe2+开始沉淀;当Fe2+完全沉淀时,溶液中Mn2+___ (填“是”或“否”)生成沉淀。[已知:Ksp(FeS)=5.6×10-18,Ksp(MnS)=2.8×10-13]
(2)25℃,两种酸的电离平衡常数如表。
①将SO2通入0.10mol/LNaOH溶液,当pH=8时溶液中离子浓度由大到小的顺序为___ 。
②将少量SO2通入过量的Na2CO3溶液中反应的离子方程式为___ 。
(1)25℃,向0.10mol/LH2S溶液中通入HCl气体或加入NaOH固体调节溶液的pH,溶液的pH与c(S2-)的关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)=
②pH=7时,c(Na+)
③某溶液含0.0040mol/LMn2+、0.0040mol/LFe2+、0.10mol/LH2S,当溶液pH=
(2)25℃,两种酸的电离平衡常数如表。
| Ka1 | Ka2 | |
| H2SO3 | 1.4×10-2 | 6.0×10-8 |
| H2CO3 | 4.5×10-7 | 4.7×10-11 |
①将SO2通入0.10mol/LNaOH溶液,当pH=8时溶液中离子浓度由大到小的顺序为
②将少量SO2通入过量的Na2CO3溶液中反应的离子方程式为
您最近一年使用:0次



