镍是银白色金属,具有磁性。图1为一种含镍配合物及其配体。
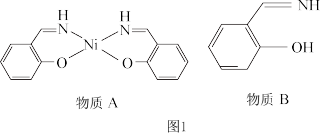
(1)Ni2+基态核外电子排布式为__________________ 。
(2)物质A中碳原子采取的杂化类型为__________ ,所含有的非金属元素的第一电离能 由小到大顺序为__________ (用元素符号表示)。
(3)1 mol物质B中所含σ键的物质的量为__________ mol。
(4)物质B在一定条件下水解生成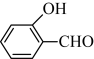 的沸点为197 ℃,而
的沸点为197 ℃,而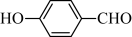 的沸点为247 ℃,导致两种物质沸点相差较大的原因是
的沸点为247 ℃,导致两种物质沸点相差较大的原因是____________ 。
(5)红镍矿是一种重要的含镍矿物,其主要成分的晶胞如图2所示,则每个 Ni原子周围与之紧邻的As原子数为__________ 。
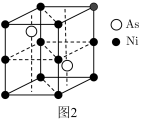
图2。

(1)Ni2+基态核外电子排布式为
(2)物质A中碳原子采取的杂化类型为
(3)1 mol物质B中所含σ键的物质的量为
(4)物质B在一定条件下水解生成
 的沸点为197 ℃,而
的沸点为197 ℃,而 的沸点为247 ℃,导致两种物质沸点相差较大的原因是
的沸点为247 ℃,导致两种物质沸点相差较大的原因是(5)红镍矿是一种重要的含镍矿物,其主要成分的晶胞如图2所示,则每个 Ni原子周围与之紧邻的As原子数为

图2。
更新时间:2019-02-20 20:08:38
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】将氟气通入氢氧化钠溶液中,可得OF2.OF2是一种无色、几乎无味的剧毒气体,主要用于氧化氟化反应、火箭工程助燃剂等。请回答下列问题:
(1)OF2中O的化合价为_______ ,OF2中O原子的杂化轨道类型是_______ ,OF2分子的空间构型为_______ 。
(2)与H2O分子相比,OF2分子的键角更_______ (填“大”或“小”)。
(3)与H2O分子相比,OF2分子的极性更_______ (填“大” 或“小”),原因是_______ ;
(4)OF2 在常温下就能与干燥空气反应生成二氧化氮和无色气体氟化氮,该反应的化学方程式为(已知反应中N2与O2的物质的量之比为4:1)_______ 。
(1)OF2中O的化合价为
(2)与H2O分子相比,OF2分子的键角更
(3)与H2O分子相比,OF2分子的极性更
(4)OF2 在常温下就能与干燥空气反应生成二氧化氮和无色气体氟化氮,该反应的化学方程式为(已知反应中N2与O2的物质的量之比为4:1)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】磷和砷的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)黑磷是新型材料,具有类似石墨一样的片层结构(如图),层与层之间以_____ 结合。从结构上可以看出单层磷烯并非平面结构,但其导电性却优于石墨烯的原因是________________ 。

(2)四(三苯基膦)钯分子结构如下图:
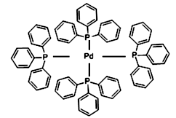

该物质可用于上图所示物质A的合成:物质A中碳原子杂化轨道类型为__________ ;
(3)PCl5是一种白色晶体,熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子.(该晶体的晶胞如图所示).熔体中P-Cl的键长只有198 nm和206 nm两种,写这两种离子的化学式为______________________ ;正四面体形阳离子中键角_____ PCl3的键角(填> 或<或=),原因是______________________________________ .
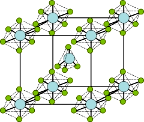
(4)PBr5气态分子的结构与PCl5相似,它的熔体也能导电,经测定知其中只存在一种P-Br键长,试用电离方程式解释PBr5熔体能导电的原因___________________________ 。
(1)黑磷是新型材料,具有类似石墨一样的片层结构(如图),层与层之间以

(2)四(三苯基膦)钯分子结构如下图:


该物质可用于上图所示物质A的合成:物质A中碳原子杂化轨道类型为
(3)PCl5是一种白色晶体,熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子.(该晶体的晶胞如图所示).熔体中P-Cl的键长只有198 nm和206 nm两种,写这两种离子的化学式为

(4)PBr5气态分子的结构与PCl5相似,它的熔体也能导电,经测定知其中只存在一种P-Br键长,试用电离方程式解释PBr5熔体能导电的原因
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】2019年诺贝尔化学奖由来自美、英、日的三人分获,以表彰他们在锂离子电池研究方面做出的贡献,他们最早发明用LiCoO2作离子电池的正极,用聚乙炔作负极。回答下列问题:
(1)基态Co原子电子排布式为____ 。
(2)Co元素位于元素周期表中第____ 周期、第____ 族。
(3)Li可以在二氧化碳中燃烧,生成白色固体和黑色固体,其方程式是____ 。
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯( )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。
①LiBF4中阴离子的空间构型是____ ;与该阴离子互为等电子体的分子有____ 。(列一种)
②碳酸亚乙酯分子中碳原子的杂化方式有____ 。
(1)基态Co原子电子排布式为
(2)Co元素位于元素周期表中第
(3)Li可以在二氧化碳中燃烧,生成白色固体和黑色固体,其方程式是
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯(
 )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。①LiBF4中阴离子的空间构型是
②碳酸亚乙酯分子中碳原子的杂化方式有
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】下列反应的离子方程式不正确 的是_______ 。
A.过量铁粉加入稀硝酸中:3Fe2++4H++ =3Fe3++2H2O+NO↑
=3Fe3++2H2O+NO↑
B.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-= +2H2O
+2H2O
C.Na2CO3溶液中通入过量SO2: +2SO2+H2O=2
+2SO2+H2O=2 +CO2
+CO2
D.明矾溶液与过量氨水混合:Al3++4NH3+4H2O= +4
+4
E.向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+
F.NaOH溶液与过量H2C2O4溶液反应:H2C2O4+2OH-= +2H2O
+2H2O
G.C6H5ONa溶液中通入少量CO2:2C6H5O-+CO2+H2O=2C6H5OH+
H.0.1mol·L-1AgNO3溶液中加入过量浓氨水:Ag++NH3+H2O=AgOH↓+
I.用Na2SO3溶液吸收少量Cl2:3 +Cl2+H2O=2
+Cl2+H2O=2 +2Cl-+
+2Cl-+
J.(NH4)2Fe(SO4)2溶液与少量Ba(OH)2溶液反应: +Ba2+=BaSO4↓
+Ba2+=BaSO4↓
K.漂白粉溶液吸收少量二氧化硫气体:SO2+H2O+ClOˉ= +Clˉ+2H+
+Clˉ+2H+
L.CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3·H2O=Cu(OH)2↓+2
A.过量铁粉加入稀硝酸中:3Fe2++4H++
 =3Fe3++2H2O+NO↑
=3Fe3++2H2O+NO↑B.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=
 +2H2O
+2H2OC.Na2CO3溶液中通入过量SO2:
 +2SO2+H2O=2
+2SO2+H2O=2 +CO2
+CO2D.明矾溶液与过量氨水混合:Al3++4NH3+4H2O=
 +4
+4
E.向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+

F.NaOH溶液与过量H2C2O4溶液反应:H2C2O4+2OH-=
 +2H2O
+2H2OG.C6H5ONa溶液中通入少量CO2:2C6H5O-+CO2+H2O=2C6H5OH+

H.0.1mol·L-1AgNO3溶液中加入过量浓氨水:Ag++NH3+H2O=AgOH↓+

I.用Na2SO3溶液吸收少量Cl2:3
 +Cl2+H2O=2
+Cl2+H2O=2 +2Cl-+
+2Cl-+
J.(NH4)2Fe(SO4)2溶液与少量Ba(OH)2溶液反应:
 +Ba2+=BaSO4↓
+Ba2+=BaSO4↓K.漂白粉溶液吸收少量二氧化硫气体:SO2+H2O+ClOˉ=
 +Clˉ+2H+
+Clˉ+2H+L.CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3·H2O=Cu(OH)2↓+2

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】 、
、 可分别溶于氨水形成
可分别溶于氨水形成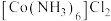 、
、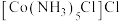 、
、 、
、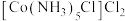 等多种配合物,其中只有
等多种配合物,其中只有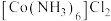 可脱除烟气中的NO并生成新的配合物。
可脱除烟气中的NO并生成新的配合物。
(1)基态Co原子的价电子排布式为___________ 。
(2)其它条件相同、不同pH时,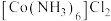 溶液对NO脱除率随时间的变化如图所示。pH=10.25较pH=9.75时的NO脱除率更高,其原因可能是
溶液对NO脱除率随时间的变化如图所示。pH=10.25较pH=9.75时的NO脱除率更高,其原因可能是___________ 。

(3)配合物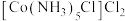 和
和 的配位数之比为
的配位数之比为___________ 。区别这两种配合物的实验方案为___________ 。
(4)将 加入
加入 和浓氨水的混合液中,生成的
和浓氨水的混合液中,生成的 需隔绝空气保存,否则会很快转化为
需隔绝空气保存,否则会很快转化为 。写出转化为
。写出转化为 的化学反应方程式:
的化学反应方程式:___________ 。
(5)不同温度下, 对NO脱除率随时间的变化如图所示。60min后,温度越高,NO脱除率下降趋势越明显,其可能的原因是
对NO脱除率随时间的变化如图所示。60min后,温度越高,NO脱除率下降趋势越明显,其可能的原因是___________ 。

 、
、 可分别溶于氨水形成
可分别溶于氨水形成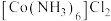 、
、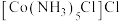 、
、 、
、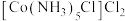 等多种配合物,其中只有
等多种配合物,其中只有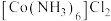 可脱除烟气中的NO并生成新的配合物。
可脱除烟气中的NO并生成新的配合物。(1)基态Co原子的价电子排布式为
(2)其它条件相同、不同pH时,
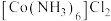 溶液对NO脱除率随时间的变化如图所示。pH=10.25较pH=9.75时的NO脱除率更高,其原因可能是
溶液对NO脱除率随时间的变化如图所示。pH=10.25较pH=9.75时的NO脱除率更高,其原因可能是
(3)配合物
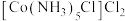 和
和 的配位数之比为
的配位数之比为(4)将
 加入
加入 和浓氨水的混合液中,生成的
和浓氨水的混合液中,生成的 需隔绝空气保存,否则会很快转化为
需隔绝空气保存,否则会很快转化为 。写出转化为
。写出转化为 的化学反应方程式:
的化学反应方程式:(5)不同温度下,
 对NO脱除率随时间的变化如图所示。60min后,温度越高,NO脱除率下降趋势越明显,其可能的原因是
对NO脱除率随时间的变化如图所示。60min后,温度越高,NO脱除率下降趋势越明显,其可能的原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】[化学——选修3:物质结构与性质]
由H、C、O、N、S、Cu等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价电子有____ 种运动状态,未成对电子占据原子轨道的形状为______ 。
(2)碳和氢形成的最简单碳正离子CH3+,其中心原子碳原子的杂化类型为___________ ,该阳离子的空间构型为___________ 。
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是_________________________________ 。
(4)向盛有CuSO4溶液的试管中滴加少量氨水,现象是_____ ,离子反应方程式为____ ;继续滴加氨水至过量得到深蓝色溶液。经测定深蓝色是由于存在[Cu(NH3)4]SO4。其阳离子的结构式为___________ ,中心原子的配位数为___________ 。
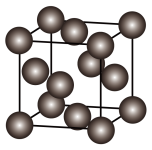
(5)金属晶体铜的晶胞如图所示。其堆积模型是___________ ,铜原子间的最短距离为apm,密度为ρg·cm-3,NA为阿伏伽德罗常数。铜的相对原子质量为___________ (用a、ρ、NA表示,写出计算式即可)。
由H、C、O、N、S、Cu等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价电子有
(2)碳和氢形成的最简单碳正离子CH3+,其中心原子碳原子的杂化类型为
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(4)向盛有CuSO4溶液的试管中滴加少量氨水,现象是
(5)金属晶体铜的晶胞如图所示。其堆积模型是

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】非金属硼的合金及其化合物有着广泛的用途。
(1)硼钢合金的硬度是普通钢材的 4 倍,其主要成分是铁。 画出基态铁原子的价电子排布图_____ 。
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键, 则氨硼烷分子结构式为_____ 。写出一种与氨硼烷互为等电子体的分子_____ (填化学式)。
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如右图所示。
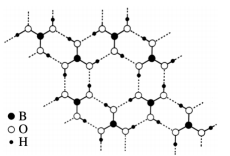
①1 mol H3BO3晶体中含有______ mol 氢键。
②请从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大的原因:__________ 。
(4)硼氢化钠是一种常用的还原剂。其晶胞结构如右图所示:

①该晶体中 Na+的配位数为_____ 。
②H3BO3 分子中的 O—B—O 的键角_____ (填“大于”、“等于”或“小于”) BH4-中的 H—B—H 的键角,判断依据是_____ 。
③已知硼氢化钠晶体的密度为 ρ g/cm3, NA代表阿伏伽德罗常数的值,则 a=_____ (用含 ρ、 NA的代数式表示);④若硼氢化钠晶胞上下底心处的 Na+被 Li+取代,得到的晶体的化学式为_____ 。
(1)硼钢合金的硬度是普通钢材的 4 倍,其主要成分是铁。 画出基态铁原子的价电子排布图
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键, 则氨硼烷分子结构式为
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如右图所示。

①1 mol H3BO3晶体中含有
②请从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大的原因:
(4)硼氢化钠是一种常用的还原剂。其晶胞结构如右图所示:

①该晶体中 Na+的配位数为
②H3BO3 分子中的 O—B—O 的键角
③已知硼氢化钠晶体的密度为 ρ g/cm3, NA代表阿伏伽德罗常数的值,则 a=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】依据所学知识回答:
⑴PH3在常温下是一种无色、剧毒、易自燃的气体,分子结构与NH3相似。PH3与HX作用生成相应的化合物PH4X,PH4X在水溶液中完全水解(PH4+结构类似于CH4)。PH3分子的空间构型是___________ 。
⑵氮是地球上极为丰富的元素,氮元素可形成多种分子或离子,如:NH3、N3―、NH2―、NH4+、N2H5+、N2H62+等。已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于NH4+的性质。
①写出N2H62+在足量浓强碱溶液中反应的离子方程式为___________________ 。
②写出由多个原子构成的含有与N3―电子数相同的物质的化学式______________ 。
③肼(N2H4)分子可视为NH3分子中的一个H原子被―NH2(氨基)取代形成的另一种氮的氢化物,则N2H4分子中氮原子的杂化类型是____________________ 。肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__________ (填标号)。
a、 离子键 b、共价键 c、 配位键 d、 范德华力
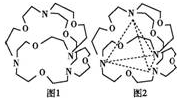
④图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键而予以识别该离子或分子。下列分子或离子中,能被该有机化合物识别的是______ (填标号)。
A、CF4 B、CH4 C、NH4+ D、H2O
⑴PH3在常温下是一种无色、剧毒、易自燃的气体,分子结构与NH3相似。PH3与HX作用生成相应的化合物PH4X,PH4X在水溶液中完全水解(PH4+结构类似于CH4)。PH3分子的空间构型是
⑵氮是地球上极为丰富的元素,氮元素可形成多种分子或离子,如:NH3、N3―、NH2―、NH4+、N2H5+、N2H62+等。已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于NH4+的性质。
①写出N2H62+在足量浓强碱溶液中反应的离子方程式为
②写出由多个原子构成的含有与N3―电子数相同的物质的化学式
③肼(N2H4)分子可视为NH3分子中的一个H原子被―NH2(氨基)取代形成的另一种氮的氢化物,则N2H4分子中氮原子的杂化类型是
a、 离子键 b、共价键 c、 配位键 d、 范德华力
④图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键而予以识别该离子或分子。下列分子或离子中,能被该有机化合物识别的是
A、CF4 B、CH4 C、NH4+ D、H2O

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】硼单质及其化合物有重要的应用。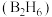 、丁硼烷
、丁硼烷 、己硼烷
、己硼烷 等。
等。 极易发生水解生成
极易发生水解生成 和
和 ,请写出反应的化学方程式:
,请写出反应的化学方程式:_______ ;其中乙硼烷生产中可用来与试剂X反应制备硼氢化钠 ,且符合原子经济性反应,试剂X的化学式为
,且符合原子经济性反应,试剂X的化学式为_______ 。同时硼氢化钠的另一种制备方法为 与试剂X反应,写出该反应的化学方程式:
与试剂X反应,写出该反应的化学方程式:_______ 。
(2)下列说法正确的是_______。
(3)氨硼烷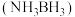 含氢量高、热稳定性好,是一种有潜力的固体储氢材料。氨硼烷分子间存在“双氢键”使氨硼烷的熔点明显升高。“双氢键”能形成的原因是
含氢量高、热稳定性好,是一种有潜力的固体储氢材料。氨硼烷分子间存在“双氢键”使氨硼烷的熔点明显升高。“双氢键”能形成的原因是_______ 。
(4)在一定条件下氨硼烷和水发生反应,产生氢气。其中溶液中的阴离子为 。设计实验检验该反应后的溶液中阳离子
。设计实验检验该反应后的溶液中阳离子_______ 。

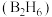 、丁硼烷
、丁硼烷 、己硼烷
、己硼烷 等。
等。 极易发生水解生成
极易发生水解生成 和
和 ,请写出反应的化学方程式:
,请写出反应的化学方程式: ,且符合原子经济性反应,试剂X的化学式为
,且符合原子经济性反应,试剂X的化学式为 与试剂X反应,写出该反应的化学方程式:
与试剂X反应,写出该反应的化学方程式:(2)下列说法正确的是_______。
A.反应①为氧化还原反应,其中 被 被 氧化 氧化 |
B.相同条件下在水中的溶解度:氨硼烷 乙烷 乙烷 |
C. 是一种一元弱酸,可以与甲醇反应生成 是一种一元弱酸,可以与甲醇反应生成 为无机酸酯 为无机酸酯 |
| D.氮化硼(BN)晶体有多种相结构,六方氮化硼结构与石墨相似,熔点低 |
(3)氨硼烷
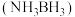 含氢量高、热稳定性好,是一种有潜力的固体储氢材料。氨硼烷分子间存在“双氢键”使氨硼烷的熔点明显升高。“双氢键”能形成的原因是
含氢量高、热稳定性好,是一种有潜力的固体储氢材料。氨硼烷分子间存在“双氢键”使氨硼烷的熔点明显升高。“双氢键”能形成的原因是(4)在一定条件下氨硼烷和水发生反应,产生氢气。其中溶液中的阴离子为
 。设计实验检验该反应后的溶液中阳离子
。设计实验检验该反应后的溶液中阳离子
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】如右图所示,晶体硼的基本结构单元都是由硼原子组成的正二十面体,这个多面体中含有20个等边三角形和一定数目的顶角,每个顶角上各有1个原子。

(1)这个基本结构单元由________ 个硼原子组成,共含有_________ 个B—B键。
(2)假设将此基本结构单元的每个顶角按一定比例且同等程度地削去(切点不重合),可得到另一个多面体,则此多面体含__________ 个五边形,__________ 个六边形。若再设此多面体的每个交点处有一个碳原子,这样就构成了碳元素形成的一种单质分子,此分子的分子式为______ 。

(1)这个基本结构单元由
(2)假设将此基本结构单元的每个顶角按一定比例且同等程度地削去(切点不重合),可得到另一个多面体,则此多面体含
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】氨硼烷是一种特殊的化合物,分子式为NH3BH3。氨硼烷在催化剂作用下水解释放氢气3NH3BH3+6H2O=3NH3+ +9H2。
+9H2。 的结构如图。回答下列问题:
的结构如图。回答下列问题:

(1)写出O原子价电子轨道式_________________ 。
(2)写出NH3BH3分子的电子式__________ ;NH3BH3晶体中含有的微粒间作用力有_______ (填标号)。
a.非极性共价键 b.配位键 c.氢键 d.范德华力 e.金属键
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-)。上述化学反应中,所含元素电负性由小到大的顺序为________ (填元素符号);反应方程式中五种微粒含有sp3杂化原子的微粒有___________ (填微粒化学式)。
(4)有机碱离子 是NH3BH3的等电子体,该离子与Pb2+、I-组成的光电材料,其晶胞如图所示:
是NH3BH3的等电子体,该离子与Pb2+、I-组成的光电材料,其晶胞如图所示:
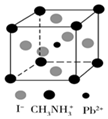
该晶体中 离子与I-离子间的作用力为
离子与I-离子间的作用力为____________ , 的配位数是
的配位数是___________ 。若晶胞参数为a pm,该晶体密度为ρ g·cm-3,阿伏加德罗常数NA可表示为_____ mol-1(列出计算式)。
 +9H2。
+9H2。 的结构如图。回答下列问题:
的结构如图。回答下列问题:
(1)写出O原子价电子轨道式
(2)写出NH3BH3分子的电子式
a.非极性共价键 b.配位键 c.氢键 d.范德华力 e.金属键
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-)。上述化学反应中,所含元素电负性由小到大的顺序为
(4)有机碱离子
 是NH3BH3的等电子体,该离子与Pb2+、I-组成的光电材料,其晶胞如图所示:
是NH3BH3的等电子体,该离子与Pb2+、I-组成的光电材料,其晶胞如图所示:
该晶体中
 离子与I-离子间的作用力为
离子与I-离子间的作用力为 的配位数是
的配位数是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】含氮、磷化合物在生活和生产中有许多重要用途,如:(CH3)3N、磷化硼(BP)、磷青铜(Cu3SnP)等。
回答下列问题:
(1)锡(Sn)是第五周期ⅣA元素。基态锡原子的价电子排布式为_________ ,据此推测,锡的最高正价是_________ 。
(2)与P同周期的主族元素中,电负性比P小的元素有____ 种 ,第一电离能比P大有____ 种。
(3)PH3分子的空间构型为___________ 。PH3的键角小于NH3的原因是__________ 。
(4)化合物(CH3)3N能溶于水,试解析其原因____________ 。
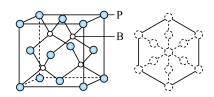
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:
①在一个晶胞中磷原子空间堆积方式为________ ,磷原子的配位数为________ 。
②已知晶胞边长a pm,阿伏伽德罗常数为NA。则磷化硼晶体的密度为______ g/cm3。
③磷化硼晶胞沿着体对角线方向的投影如图,请将表示B原子的圆圈涂黑________ 。
回答下列问题:
(1)锡(Sn)是第五周期ⅣA元素。基态锡原子的价电子排布式为
(2)与P同周期的主族元素中,电负性比P小的元素有
(3)PH3分子的空间构型为
(4)化合物(CH3)3N能溶于水,试解析其原因

(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:
①在一个晶胞中磷原子空间堆积方式为
②已知晶胞边长a pm,阿伏伽德罗常数为NA。则磷化硼晶体的密度为
③磷化硼晶胞沿着体对角线方向的投影如图,请将表示B原子的圆圈涂黑
您最近一年使用:0次



