现代高科技领域使用的新型陶瓷材料氮化硼(BN),用天然硼砂(Na2B4O7∙10H2O)经过下列过程可以制得。
天然硼砂 硼酸(H3BO3)
硼酸(H3BO3) B2O3
B2O3 BN
BN
(1)天然硼砂所含的元素中属于同一周期且原子半径是(用元素符号填写)___ >___ ,由天然硼砂中的三种元素形成的某种离子化合物的电子式为______ 。
(2)与硼元素性质最相似的元素的原子的最外层电子排布为_______ ,该原子核外充有电子的轨道共有____ 个。
(3)试写出天然硼砂与硫酸反应的化学方程式_______ ,制得的氮化硼有不同的结构,其中超硬、耐磨、耐高温的一种属于____ 晶体。制取氮化硼的反应必须在密闭的耐高温容器中进行:B2O3(s)+2NH3(g) 2BN(s)+3H2O(g)+Q(Q<0)
2BN(s)+3H2O(g)+Q(Q<0)
(4)若反应在5L的密闭容器中进行,经2分钟反应炉内固体的质量减少60.0g,则用氨气来表示该反应在2分钟内的平均速率为_____ ,达到平衡后,增大反应容器体积,在平衡移动过程中,逆反应速率的变化状况为______ 。
(5)为提高生产效率,使反应速率加快的同时,化学平衡向多出产品的方向移动,可以采取的措施有_________ ,生产中对尾气的处理方法正确的是(填序号)_____ 。
A.直接排出参与大气循环 B.冷却分离所得气体可以循环使用
C.全部用来进行循环使用 D.冷却分离所得液体可作化工原料
天然硼砂
 硼酸(H3BO3)
硼酸(H3BO3) B2O3
B2O3 BN
BN(1)天然硼砂所含的元素中属于同一周期且原子半径是(用元素符号填写)
(2)与硼元素性质最相似的元素的原子的最外层电子排布为
(3)试写出天然硼砂与硫酸反应的化学方程式
 2BN(s)+3H2O(g)+Q(Q<0)
2BN(s)+3H2O(g)+Q(Q<0)(4)若反应在5L的密闭容器中进行,经2分钟反应炉内固体的质量减少60.0g,则用氨气来表示该反应在2分钟内的平均速率为
(5)为提高生产效率,使反应速率加快的同时,化学平衡向多出产品的方向移动,可以采取的措施有
A.直接排出参与大气循环 B.冷却分离所得气体可以循环使用
C.全部用来进行循环使用 D.冷却分离所得液体可作化工原料
更新时间:2019-04-19 19:54:40
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】(1)在某一容积为 的密闭容器中,某一反应中A、B、C、D四种气体的物质的量
的密闭容器中,某一反应中A、B、C、D四种气体的物质的量 随时间
随时间 的变化曲线如图所示:
的变化曲线如图所示:

回答下列问题:
①该反应的化学方程式为_______ ;
②前2 min用A的浓度变化表示的化学反应速率____ ,在 时,图象发生改变的可能原因是
时,图象发生改变的可能原因是____ (填字母)
A.增大压强 B.降低温度 C.加入催化剂 D.增加A的物质的量
(2)在100℃时,将 的四氧化二氮气体充入
的四氧化二氮气体充入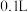 的密闭容器中发生反应,每隔一定时间对该容器内的物质进行分析,得到如下表格:
的密闭容器中发生反应,每隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:达到平衡时四氧化二氮的转化率为_____ ,表中
____  ;a
;a _____ b。(填“>”“<”或“=”)
 的密闭容器中,某一反应中A、B、C、D四种气体的物质的量
的密闭容器中,某一反应中A、B、C、D四种气体的物质的量 随时间
随时间 的变化曲线如图所示:
的变化曲线如图所示:
回答下列问题:
①该反应的化学方程式为
②前2 min用A的浓度变化表示的化学反应速率
 时,图象发生改变的可能原因是
时,图象发生改变的可能原因是A.增大压强 B.降低温度 C.加入催化剂 D.增加A的物质的量
(2)在100℃时,将
 的四氧化二氮气体充入
的四氧化二氮气体充入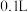 的密闭容器中发生反应,每隔一定时间对该容器内的物质进行分析,得到如下表格:
的密闭容器中发生反应,每隔一定时间对该容器内的物质进行分析,得到如下表格:| 时间/s 浓度/  | 0 | 20 | 40 | 60 | 80 | 100 |
 | 0.100 | 0.070 | 0.050 | c3 | a | b |
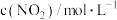 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |

 ;a
;a
您最近一年使用:0次
【推荐2】亚硝酰溴 常用于有机合成等。工业上,常用
常用于有机合成等。工业上,常用 与
与 反应制取
反应制取 ,其制备原理为
,其制备原理为 。
。
(1)实验室常将液溴保存在水中,其原因是_______ 。实验室常用 和浓硫酸混合共热制备
和浓硫酸混合共热制备 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
(2)在恒容恒温条件下,充入 和
和 ,发生上述反应。下列情况表明反应达到化学平衡状态的是_______(填字母)。
,发生上述反应。下列情况表明反应达到化学平衡状态的是_______(填字母)。
(3)某条件下,该反应速率 ,其中
,其中 为速率常数,只与温度、催化剂有关,
为速率常数,只与温度、催化剂有关, 为反应级数,可以取负数、正数;也可以取分数和整数。为了测定反应级数,实验结果如下:
为反应级数,可以取负数、正数;也可以取分数和整数。为了测定反应级数,实验结果如下:
①反应级数 为
为_______ 。
②其他条件相同,升高温度,
_______ (填“增大”“减小”或“不变”)。
(4)在体积相同的甲、乙容器中均充入 和
和 ,在“恒温恒容”、“绝热恒容”条件下发生上述反应,测得压强与时间关系如图所示。提示:①绝热恒容指物质与能量与外界不交换,即对于放热反应,容器温度会升高;②对于恒温恒容条件下,气体总压强与气体总物质的量成正比例;③在体积相同的条件下,一定物质的量的气体,温度越高,压强越大。
,在“恒温恒容”、“绝热恒容”条件下发生上述反应,测得压强与时间关系如图所示。提示:①绝热恒容指物质与能量与外界不交换,即对于放热反应,容器温度会升高;②对于恒温恒容条件下,气体总压强与气体总物质的量成正比例;③在体积相同的条件下,一定物质的量的气体,温度越高,压强越大。

①属于绝热恒容容器的是_______ (填“甲”或“乙”), 中反应物总能量
中反应物总能量_______ (填“高于”或“低于”)产物总能量。气体总物质的量:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
② 点NO的转化率为
点NO的转化率为_______ 。
 常用于有机合成等。工业上,常用
常用于有机合成等。工业上,常用 与
与 反应制取
反应制取 ,其制备原理为
,其制备原理为 。
。(1)实验室常将液溴保存在水中,其原因是
 和浓硫酸混合共热制备
和浓硫酸混合共热制备 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)在恒容恒温条件下,充入
 和
和 ,发生上述反应。下列情况表明反应达到化学平衡状态的是_______(填字母)。
,发生上述反应。下列情况表明反应达到化学平衡状态的是_______(填字母)。| A.混合气体密度不随时间变化 | B.混合气体压强不随时间变化 |
| C.混合气体平均摩尔质量不随时间变化 | D.生成 速率等于消耗 速率等于消耗 速率 速率 |
 ,其中
,其中 为速率常数,只与温度、催化剂有关,
为速率常数,只与温度、催化剂有关, 为反应级数,可以取负数、正数;也可以取分数和整数。为了测定反应级数,实验结果如下:
为反应级数,可以取负数、正数;也可以取分数和整数。为了测定反应级数,实验结果如下:| 实验 | 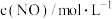 |  |  | 反应速率 |
| Ⅰ | 0.1 | 0.1 | 0.1 |  |
| Ⅱ | 0.2 | 0.1 | 0.1 |  |
| Ⅲ | 0.2 | 0.2 | 0.1 |  |
| Ⅳ | 0.4 | 0.2 | 0.2 |  |
 为
为②其他条件相同,升高温度,

(4)在体积相同的甲、乙容器中均充入
 和
和 ,在“恒温恒容”、“绝热恒容”条件下发生上述反应,测得压强与时间关系如图所示。提示:①绝热恒容指物质与能量与外界不交换,即对于放热反应,容器温度会升高;②对于恒温恒容条件下,气体总压强与气体总物质的量成正比例;③在体积相同的条件下,一定物质的量的气体,温度越高,压强越大。
,在“恒温恒容”、“绝热恒容”条件下发生上述反应,测得压强与时间关系如图所示。提示:①绝热恒容指物质与能量与外界不交换,即对于放热反应,容器温度会升高;②对于恒温恒容条件下,气体总压强与气体总物质的量成正比例;③在体积相同的条件下,一定物质的量的气体,温度越高,压强越大。
①属于绝热恒容容器的是
 中反应物总能量
中反应物总能量
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②
 点NO的转化率为
点NO的转化率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】钪( )是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为
)是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为 、
、 、
、 、
、 )中回收钪,同时会生成聚合硫酸铁铝
)中回收钪,同时会生成聚合硫酸铁铝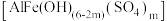 ,其工艺流程如图所示:
,其工艺流程如图所示:
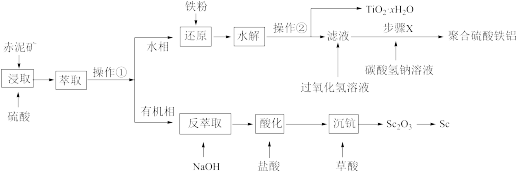
已知:①钪离子可以在不同 下生成
下生成 (n为1~6)。
(n为1~6)。
②“浸取”后 元素转化为
元素转化为 。
。
请回答以下问题:
(1)基态 的价电子轨道表示式为
的价电子轨道表示式为_______ 。
(2)“萃取”时,使用伯胺N1923的煤油溶液作为萃取液,萃取率 受振荡时间和萃取剂浓度的影响,根据表1和表2数据,萃取时适宜的振荡时间和萃取剂浓度分别为
受振荡时间和萃取剂浓度的影响,根据表1和表2数据,萃取时适宜的振荡时间和萃取剂浓度分别为_______ min、_______ %;实验室中要完成操作①所需的玻璃仪器有_______ 。
表1 振荡时间对萃取率的影响
表2 萃取剂浓度对萃取率的影响
(3)向“水解”后的“滤液”中加入过氧化氢溶液,反应的离子方程式为_______ 。
(4)“步骤X”中,若将含42 碳酸氢钠的溶液加入500L混合溶液中,恰好完全反应生成难溶的
碳酸氢钠的溶液加入500L混合溶液中,恰好完全反应生成难溶的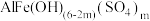 、
、 和
和 ,则产生的
,则产生的 在标准状况下体积为
在标准状况下体积为_______ L。(设气体全部逸出)
(5)沉钪后,在空气中灼烧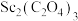 得到
得到 的同时产生
的同时产生 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
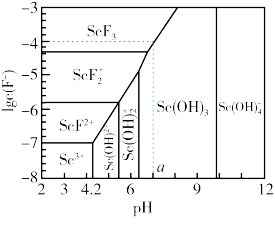
(6)已知:常温下,在有 存在时,
存在时, 的存在形式与
的存在形式与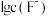 、
、 的关系如图所示。当
的关系如图所示。当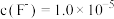
 、
、 时,
时, 的存在形式为
的存在形式为_______ (填化学式);若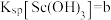 ,则
,则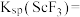
_______ (用含a、b的代数式表示)。
 )是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为
)是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为 、
、 、
、 、
、 )中回收钪,同时会生成聚合硫酸铁铝
)中回收钪,同时会生成聚合硫酸铁铝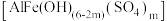 ,其工艺流程如图所示:
,其工艺流程如图所示:
已知:①钪离子可以在不同
 下生成
下生成 (n为1~6)。
(n为1~6)。②“浸取”后
 元素转化为
元素转化为 。
。请回答以下问题:
(1)基态
 的价电子轨道表示式为
的价电子轨道表示式为(2)“萃取”时,使用伯胺N1923的煤油溶液作为萃取液,萃取率
 受振荡时间和萃取剂浓度的影响,根据表1和表2数据,萃取时适宜的振荡时间和萃取剂浓度分别为
受振荡时间和萃取剂浓度的影响,根据表1和表2数据,萃取时适宜的振荡时间和萃取剂浓度分别为表1 振荡时间对萃取率的影响
 | 1 | 3 | 5 | 10 | 15 |
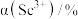 | 85.2 | 89.3 | 91.2 | 98.7 | 98.8 |
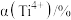 | 4.9 | 8.9 | 9.6 | 10.0 | 11.3 |
 | 0.90 | 1.00 | 1.31 | 1.41 | 1.43 |
表2 萃取剂浓度对萃取率的影响
| 伯胺N1923/% | 1 | 5 | 10 | 15 | 20 |
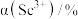 | 86.7 | 93.1 | 94.2 | 98.8 | 98.9 |
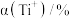 | 8.1 | 9.0 | 9.9 | 10.1 | 11.7 |
 | 0.91 | 1.20 | 1.31 | 1.43 | 2.13 |
(3)向“水解”后的“滤液”中加入过氧化氢溶液,反应的离子方程式为
(4)“步骤X”中,若将含42
 碳酸氢钠的溶液加入500L混合溶液中,恰好完全反应生成难溶的
碳酸氢钠的溶液加入500L混合溶液中,恰好完全反应生成难溶的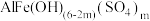 、
、 和
和 ,则产生的
,则产生的 在标准状况下体积为
在标准状况下体积为(5)沉钪后,在空气中灼烧
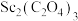 得到
得到 的同时产生
的同时产生 ,该反应的化学方程式为
,该反应的化学方程式为(6)已知:常温下,在有
 存在时,
存在时, 的存在形式与
的存在形式与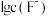 、
、 的关系如图所示。当
的关系如图所示。当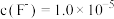
 、
、 时,
时, 的存在形式为
的存在形式为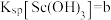 ,则
,则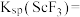

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】探究化学反应的快慢和限度具有十分重要的意义。
I.某实验小组欲通过用酸性 和
和 (草酸)反应测定单位时间内生成
(草酸)反应测定单位时间内生成 的速率研究影响反应速率的因素,设计实验方案如下(
的速率研究影响反应速率的因素,设计实验方案如下( 溶液已酸化),实验装置如图甲所示:
溶液已酸化),实验装置如图甲所示:

(1)上述反应的离子方程式为:___________ ,该实验是探究___________ 对反应速率的影响。
(2)若实验①在2min末收集了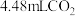 (标准状况下),则在2min末,
(标准状况下),则在2min末,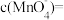
___________ mol/L(假设混合溶液的体积为50mL,反应前后体积变化忽略不计)。
(3)小组同学发现反应速率变化如图乙,其中 时间内速率变快的主要原因可能是:
时间内速率变快的主要原因可能是:___________ 。
Ⅱ.溶液中存在平衡 (橙色)
(橙色)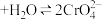 (黄色)
(黄色)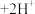 。用溶液进行下列实验:
。用溶液进行下列实验:

(4)向 溶液中加入
溶液中加入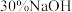 溶液,溶液呈
溶液,溶液呈___________ 色。向 溶液中逐滴加入
溶液中逐滴加入 溶液(已知
溶液(已知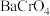 为黄色沉淀),则平衡向着
为黄色沉淀),则平衡向着___________ 方向移动,溶液颜色变化为___________ 。
(5)对比实验②和④可得出的结论是___________ 。
I.某实验小组欲通过用酸性
 和
和 (草酸)反应测定单位时间内生成
(草酸)反应测定单位时间内生成 的速率研究影响反应速率的因素,设计实验方案如下(
的速率研究影响反应速率的因素,设计实验方案如下( 溶液已酸化),实验装置如图甲所示:
溶液已酸化),实验装置如图甲所示:
| 实验序号 | A溶液 | B溶液 |
| ① | 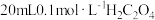 溶液 溶液 | 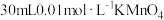 溶液 溶液 |
| ② | 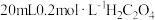 溶液 溶液 | 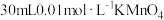 溶液 溶液 |
(2)若实验①在2min末收集了
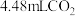 (标准状况下),则在2min末,
(标准状况下),则在2min末,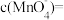
(3)小组同学发现反应速率变化如图乙,其中
 时间内速率变快的主要原因可能是:
时间内速率变快的主要原因可能是:Ⅱ.溶液中存在平衡
 (橙色)
(橙色)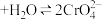 (黄色)
(黄色)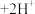 。用溶液进行下列实验:
。用溶液进行下列实验:
(4)向
 溶液中加入
溶液中加入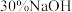 溶液,溶液呈
溶液,溶液呈 溶液中逐滴加入
溶液中逐滴加入 溶液(已知
溶液(已知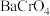 为黄色沉淀),则平衡向着
为黄色沉淀),则平衡向着(5)对比实验②和④可得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】设计的实验方案如下表。(已知I2+2S2O32-=S4O62-+2I-,其中Na2S2O3溶液均足量)
(1)该实验进行的目的是____________ ,该实验是根据__________ 现象记录时间。
(2)表中Vx=______ mL,比较t1、t2、t3大小____________ 。
| 实验 序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
(2)表中Vx=
您最近一年使用:0次
【推荐3】某实验小组为探究含硫化合物(NH4)2S2O8的性质,设计如下实验探究(NH4)2S2O8的氧化性。
实验操作:向小试管中加入 溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量
溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量 溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在
溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在 。
。
(1) 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
(2)检验该溶液中存在 的具体操作及现象为
的具体操作及现象为_______ 。
(3)实验结论: 的氧化性
的氧化性_______ (填“强于”或“弱于”)I2。
已知:I2可与 发生反应:
发生反应: 。为了进一步探究
。为了进一步探究 与
与 的反应速率,小组同学设计下表实验:
的反应速率,小组同学设计下表实验:
(4)上述实验Ⅱ中的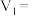
_______ ;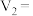
_______ 。
加入 溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
猜想1: 与
与 反应的速率远低于
反应的速率远低于 与
与 反应的速率;
反应的速率;
猜想2: 先与
先与 反应,
反应, 消耗完后才与
消耗完后才与 反应。
反应。
为验证上述猜想,小组同学补充下表实验:
(5)验证猜想1的实验设计为_______ (填“实验Ⅲ”或“实验Ⅳ”下同),验证猜想2的实验设计为_______ 。
(6)实验Ⅲ中下层溶液显浅紫色的原因为_______ 。
(7)由上述实验可知_______ (填“猜想1”或“猜想2”)成立。
实验操作:向小试管中加入
 溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量
溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量 溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在
溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在 。
。(1)
 与
与 反应的离子方程式为
反应的离子方程式为(2)检验该溶液中存在
 的具体操作及现象为
的具体操作及现象为(3)实验结论:
 的氧化性
的氧化性已知:I2可与
 发生反应:
发生反应: 。为了进一步探究
。为了进一步探究 与
与 的反应速率,小组同学设计下表实验:
的反应速率,小组同学设计下表实验:| 试验编号 | 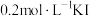 溶液/ 溶液/ | 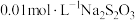 溶液/ 溶液/ | 蒸馏水/ | 0.4%的淀粉溶液/滴 |  溶液/ 溶液/ | 变色时间/s |
| Ⅰ | 4.0 | 0 | 4.0 | 2 | 2.0 | 立即 |
| Ⅱ | 4.0 | 1.0 |  | 2 |  | 30 |
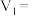
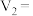
加入
 溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:猜想1:
 与
与 反应的速率远低于
反应的速率远低于 与
与 反应的速率;
反应的速率;猜想2:
 先与
先与 反应,
反应, 消耗完后才与
消耗完后才与 反应。
反应。为验证上述猜想,小组同学补充下表实验:
| 试验编号 | 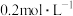  溶液/ 溶液/ |   碘水/ 碘水/ |   溶液/ 溶液/ |  / / | 0.4%的淀粉溶液/滴 | 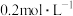 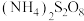 溶液/ 溶液/ | 实验现象 |
| Ⅲ | 2 | 0 | 20 | 10 | 0 | 0.2 | 下层溶液显浅紫色 |
| Ⅳ | 0 | 5 | 20 | 0 | 2 | 20 | 溶液先变蓝,后迅速褪色,一段时间后又变蓝 |
(6)实验Ⅲ中下层溶液显浅紫色的原因为
(7)由上述实验可知
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】 、
、 、
、 、
、 、S、P等元素常用于化工材料的合成。回答下列问题:
、S、P等元素常用于化工材料的合成。回答下列问题:
(1)钴原子的基态电子排布式为_______________________ 。
(2) 有
有________ 几种不同的运动状态的电子, 比
比 更稳定的原因是
更稳定的原因是_________ 。
(3)硒为第四周期元素,相邻元素有砷和溴,则三种元素的电负性从大到小的顺序为_________ (用元素符号表示)。
(4) 的熔点为340℃,加热易升华,固体
的熔点为340℃,加热易升华,固体 属于
属于______ 晶体。 的空间构型为
的空间构型为_____ 。
(5) 可用于制造火柴,其分子结构如图甲所示。
可用于制造火柴,其分子结构如图甲所示。 分子中S的杂化方式为
分子中S的杂化方式为______ 。每个 分子中含有的孤电子对的数目为
分子中含有的孤电子对的数目为_________ 。

(6)铜的某种氧化物晶胞结构如图乙所示,该氧化物的化学式为____________ 。若该晶胞的边长为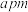 ,阿伏加 德罗常数值为
,阿伏加 德罗常数值为 ,则该氧化物的密度为
,则该氧化物的密度为_________ 
 、
、 、
、 、
、 、S、P等元素常用于化工材料的合成。回答下列问题:
、S、P等元素常用于化工材料的合成。回答下列问题:(1)钴原子的基态电子排布式为
(2)
 有
有 比
比 更稳定的原因是
更稳定的原因是(3)硒为第四周期元素,相邻元素有砷和溴,则三种元素的电负性从大到小的顺序为
(4)
 的熔点为340℃,加热易升华,固体
的熔点为340℃,加热易升华,固体 属于
属于 的空间构型为
的空间构型为(5)
 可用于制造火柴,其分子结构如图甲所示。
可用于制造火柴,其分子结构如图甲所示。 分子中S的杂化方式为
分子中S的杂化方式为 分子中含有的孤电子对的数目为
分子中含有的孤电子对的数目为
(6)铜的某种氧化物晶胞结构如图乙所示,该氧化物的化学式为
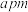 ,阿伏加 德罗常数值为
,阿伏加 德罗常数值为 ,则该氧化物的密度为
,则该氧化物的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和。
请回答下列问题:
(1)分子式为BC2的空间构型为____ ;F2+的核外电子排布式为_____________ 。
(2)A分别与B、C形成的最简单化合物的稳定性B____ C(填“大于”或“小于”);A、C两元素可组成原子个数比为1:1的化合物,C元素的杂化类型为____________ 。
(3)A2C所形成的晶体类型为____ ;F单质形成的晶体类型为____________ ,其采用的堆积方式为____________ 。
(4)F元素氧化物的熔点比其硫化物的____ (填“高”或“低”),请解释其原因____ 。
(5)D跟E可形成离子化合物,其晶胞结构如右图。该离子化合物晶体的密度为pg/cm3,则晶胞的体积是____________ 。(用含p的代数式表示)。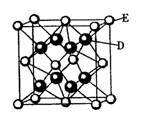
请回答下列问题:
(1)分子式为BC2的空间构型为
(2)A分别与B、C形成的最简单化合物的稳定性B
(3)A2C所形成的晶体类型为
(4)F元素氧化物的熔点比其硫化物的
(5)D跟E可形成离子化合物,其晶胞结构如右图。该离子化合物晶体的密度为pg/cm3,则晶胞的体积是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氨和水都是常用的试剂。请回答下列问题:
(1)氮元素基态原子的核外电子中,未成对电子数成对电子数之比为_____ 。
(2)NH3分子可结合一个H+形成铵根离子(NH4+)。
①NH3分子中N原子的杂化类型是_____ 。
②NH3分子中与H+结合的过程中未发生改变的是_____ (填序号)。
a 微粒的空间构型 b N原子的杂化类型 c H—N—H的键角
(3)将氨气通入CuSO4溶液中,产生蓝色沉淀,继续通过量氨气,沉淀溶解,得到蓝色透明溶液。该过程中微粒的变化是[Cu(H2O)6]2+→Cu(OH)2→[Cu(NH3)4]2+。 [Cu(H2O)6]2+和[Cu(NH3)4]2+中共同含有的化学键类型是_______ 。
(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,则冰晶体中氢键的“键能”是_____ kJ·mol(已知冰的升华热是51 kJ·mol-1),水分子间范德华力的能量为11 kJ·mol-1);水变成冰晶体时,密度减小的主要原因是________________________________ 。
(1)氮元素基态原子的核外电子中,未成对电子数成对电子数之比为
(2)NH3分子可结合一个H+形成铵根离子(NH4+)。
①NH3分子中N原子的杂化类型是
②NH3分子中与H+结合的过程中未发生改变的是
a 微粒的空间构型 b N原子的杂化类型 c H—N—H的键角
(3)将氨气通入CuSO4溶液中,产生蓝色沉淀,继续通过量氨气,沉淀溶解,得到蓝色透明溶液。该过程中微粒的变化是[Cu(H2O)6]2+→Cu(OH)2→[Cu(NH3)4]2+。 [Cu(H2O)6]2+和[Cu(NH3)4]2+中共同含有的化学键类型是
(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,则冰晶体中氢键的“键能”是
您最近一年使用:0次



