东晋 华阳国志
华阳国志 南中志
南中志 卷四中已有关于白铜的记载,云南镍白铜
卷四中已有关于白铜的记载,云南镍白铜 铜镍合金
铜镍合金 闻名中外,曾主要用于造币,亦可用于制作仿银饰品
闻名中外,曾主要用于造币,亦可用于制作仿银饰品 回答下列问题:
回答下列问题:
 镍元素基态原子的电子排布式为
镍元素基态原子的电子排布式为______ ,3d能级上的未成对电子数为______ .
 硫酸镍溶于氨水形成
硫酸镍溶于氨水形成 蓝色溶液.
蓝色溶液.
 中阴离子的立体构型是
中阴离子的立体构型是______ .
 在
在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为___ ,提供孤电子对的成键原子是______ .
 氨是
氨是______ 分子 填“极性”或“非极性”
填“极性”或“非极性” ,中心原子的轨道杂化类型为
,中心原子的轨道杂化类型为______ .
 单质铜及镍都是由
单质铜及镍都是由______ 键形成的晶体;元素铜与镍的第二电离能分别为: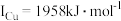 、
、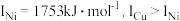 的原因是
的原因是______ .
 某镍白铜合金的立方晶胞结构如图所示.
某镍白铜合金的立方晶胞结构如图所示.
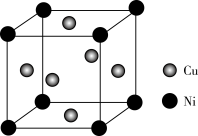
 晶胞中铜原子与镍原子的数量比为
晶胞中铜原子与镍原子的数量比为______ .
 若合金的密度为
若合金的密度为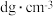 ,晶胞参数
,晶胞参数
______ nm.
 华阳国志
华阳国志 南中志
南中志 卷四中已有关于白铜的记载,云南镍白铜
卷四中已有关于白铜的记载,云南镍白铜 铜镍合金
铜镍合金 闻名中外,曾主要用于造币,亦可用于制作仿银饰品
闻名中外,曾主要用于造币,亦可用于制作仿银饰品 回答下列问题:
回答下列问题: 镍元素基态原子的电子排布式为
镍元素基态原子的电子排布式为 硫酸镍溶于氨水形成
硫酸镍溶于氨水形成 蓝色溶液.
蓝色溶液. 中阴离子的立体构型是
中阴离子的立体构型是 在
在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为 氨是
氨是 填“极性”或“非极性”
填“极性”或“非极性” ,中心原子的轨道杂化类型为
,中心原子的轨道杂化类型为 单质铜及镍都是由
单质铜及镍都是由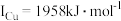 、
、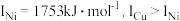 的原因是
的原因是 某镍白铜合金的立方晶胞结构如图所示.
某镍白铜合金的立方晶胞结构如图所示.
 晶胞中铜原子与镍原子的数量比为
晶胞中铜原子与镍原子的数量比为 若合金的密度为
若合金的密度为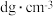 ,晶胞参数
,晶胞参数
更新时间:2019-05-13 15:33:16
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】 被认为是良好的光学基质材料,可由
被认为是良好的光学基质材料,可由 、
、 ,
,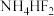 制备,掺杂Fe、Co、Ni等过渡金属的
制备,掺杂Fe、Co、Ni等过渡金属的 可得到不同的荧光材料。
可得到不同的荧光材料。
(1)写出基态氟原子的价电子排布式:___________ 。
(2)实验测定,在 中存在σ键和大π键,σ键由C的
中存在σ键和大π键,σ键由C的___________ 杂化轨道与O的2p轨道形成,4中心6电子的大π键(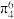 )由C的
)由C的___________ (填“杂化”或“未杂化”)2p空轨道与O的2p轨道形成。
(3)已知:
 的熔点远高于
的熔点远高于 的主要原因是
的主要原因是___________ 。
(4)已知HF与 通过氢键结合成
通过氢键结合成 。
。
①1 mol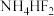 中含有
中含有___________ mol σ键。
②判断 微粒间能否形成氢键,并说明理由:
微粒间能否形成氢键,并说明理由:___________ 。
(5) 、
、 两种晶体的晶胞结构不同,其中
两种晶体的晶胞结构不同,其中 具有钙钛矿型立方结构(如图所示):
具有钙钛矿型立方结构(如图所示): 晶体中,
晶体中, 周围最邻近且距离相等的
周围最邻近且距离相等的 的个数为
的个数为___________ 。
②已知 晶胞的体积为V cm
晶胞的体积为V cm ,晶体密度为ρ g⋅cm
,晶体密度为ρ g⋅cm ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则一个晶胞中
,则一个晶胞中 的个数为
的个数为___________ (用含V,ρ, 的代数式表示)。
的代数式表示)。
 被认为是良好的光学基质材料,可由
被认为是良好的光学基质材料,可由 、
、 ,
,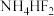 制备,掺杂Fe、Co、Ni等过渡金属的
制备,掺杂Fe、Co、Ni等过渡金属的 可得到不同的荧光材料。
可得到不同的荧光材料。(1)写出基态氟原子的价电子排布式:
(2)实验测定,在
 中存在σ键和大π键,σ键由C的
中存在σ键和大π键,σ键由C的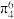 )由C的
)由C的(3)已知:
| 物质 |  |  | 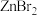 | 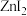 |
| 熔点/℃ | 872 | 290 | 394 | 446 |
 的熔点远高于
的熔点远高于 的主要原因是
的主要原因是(4)已知HF与
 通过氢键结合成
通过氢键结合成 。
。①1 mol
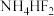 中含有
中含有②判断
 微粒间能否形成氢键,并说明理由:
微粒间能否形成氢键,并说明理由:(5)
 、
、 两种晶体的晶胞结构不同,其中
两种晶体的晶胞结构不同,其中 具有钙钛矿型立方结构(如图所示):
具有钙钛矿型立方结构(如图所示):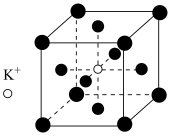
 晶体中,
晶体中, 周围最邻近且距离相等的
周围最邻近且距离相等的 的个数为
的个数为②已知
 晶胞的体积为V cm
晶胞的体积为V cm ,晶体密度为ρ g⋅cm
,晶体密度为ρ g⋅cm ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则一个晶胞中
,则一个晶胞中 的个数为
的个数为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】三明清流“天芳悦潭”温泉富含“锗”元素。其中锗石含有硒、锌、镍、钴、锰、钙等多种对人体有益的微量元素。回答下列问题:
(1)基态Ge原子价电子轨道表示式为_______ 。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: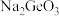 ;二锗酸钠:
;二锗酸钠: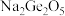 等),也能形成类似于烷烃的锗烷
等),也能形成类似于烷烃的锗烷 。推测
。推测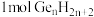 中含有的σ键的数目是
中含有的σ键的数目是_______ (用 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)
(3)利用离子液体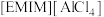 可电沉积还原金属Ge,其熔点只有7℃,其中
可电沉积还原金属Ge,其熔点只有7℃,其中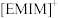 结构如图所示。
结构如图所示。

①该物质的晶体类型是_______ 。
②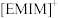 中组成元素的电负性由小到大的顺序是
中组成元素的电负性由小到大的顺序是_______ 。
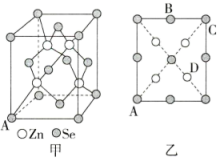
(4)硒化锌( )是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是_______ ;已知晶胞边长为apm,乙图为甲图的俯视图,A点坐标为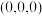 ,B点坐标为
,B点坐标为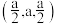 ,则D点坐标为
,则D点坐标为_______ ;若该晶胞密度为 ,则阿伏加德罗常数的值NA为
,则阿伏加德罗常数的值NA为_______ (只列出计算式)。
(1)基态Ge原子价电子轨道表示式为
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
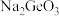 ;二锗酸钠:
;二锗酸钠: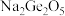 等),也能形成类似于烷烃的锗烷
等),也能形成类似于烷烃的锗烷 。推测
。推测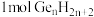 中含有的σ键的数目是
中含有的σ键的数目是 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)(3)利用离子液体
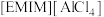 可电沉积还原金属Ge,其熔点只有7℃,其中
可电沉积还原金属Ge,其熔点只有7℃,其中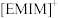 结构如图所示。
结构如图所示。
①该物质的晶体类型是
②
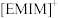 中组成元素的电负性由小到大的顺序是
中组成元素的电负性由小到大的顺序是(4)硒化锌(
 )是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是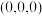 ,B点坐标为
,B点坐标为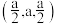 ,则D点坐标为
,则D点坐标为 ,则阿伏加德罗常数的值NA为
,则阿伏加德罗常数的值NA为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】我国磷、铬、锂等矿产资源储量丰富。回答下列问题:
(1)基态铬原子核外共有___________ 种不同运动状态的电子;基态铬原子的价电子轨道表示式为___________ 。
(2)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图所示(其晶胞参数或边长为a pm);
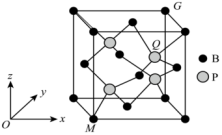
①固态磷化硼属于___________ (填“分子”“离子”或“共价”)晶体。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0),则Q点的原子分数坐标为___________ 。
③磷化硼晶体的密度为___________  (列出计算式)。
(列出计算式)。
(3)物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___________(填标号)。
(4)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:
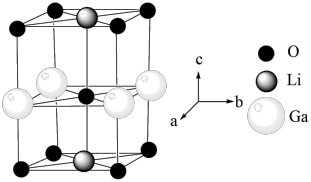
①该晶体的化学式为___________ 。
②上述晶胞沿着a轴的投影图为___________ (填选项字母)。
A.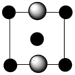 B.
B. C.
C.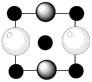
(1)基态铬原子核外共有
(2)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图所示(其晶胞参数或边长为a pm);

①固态磷化硼属于
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0),则Q点的原子分数坐标为
③磷化硼晶体的密度为
 (列出计算式)。
(列出计算式)。(3)物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___________(填标号)。
A.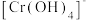 | B.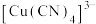 | C.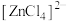 | D. |

①该晶体的化学式为
②上述晶胞沿着a轴的投影图为
A.
 B.
B. C.
C.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数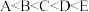 。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。
。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。 为产生温室效应的主要气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24。请根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
为产生温室效应的主要气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24。请根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_______ 。
(2)B的氢化物分子的立体构型是_______ ;
(3)写出化合物 的电子式
的电子式_______ ;
(4)E的核外电子排布式是_______ 。
(5)元素A的原子核外共有_______ 种不同运动状态的电子,有_______ 种不同能级的电子。
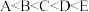 。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。
。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。 为产生温室效应的主要气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24。请根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
为产生温室效应的主要气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24。请根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物分子的立体构型是
(3)写出化合物
 的电子式
的电子式(4)E的核外电子排布式是
(5)元素A的原子核外共有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】下列表格是元素周期表的一部分。请按要求填空。
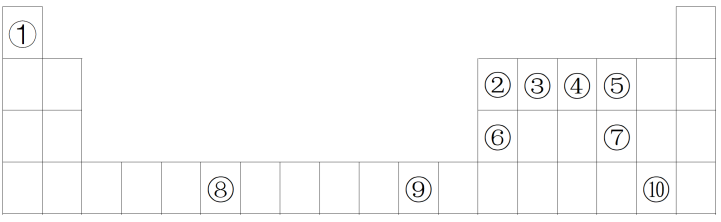
(1)写出一种由元素①和⑤形成的常见化合物的电子式为_______
(2)由②形成的单质是一种是硬度很大,熔点很高的晶体,则该晶体属于_______ 晶体。
(3)③④⑤三种元素的第一电离能从大到小排序为_______ 。
(4)写出工业上冶炼⑥单质的化学方程式_______ 。
(5)列举元素⑦形成的最高价含氧酸的用途_______ (至少列举两种)。
(6)元素⑧的核外电子排布式为_______ 。
(7)下图为⑨晶体的晶胞结构。若晶胞的棱长为acm,则两个最近的⑨原子之间的距离是_______ cm,晶胞密度为_______ g·cm-3(⑨的摩尔质量用M表示,阿伏加德罗常数的值用NA表示)。

(8)天津市有着丰富的海水资源,海水中含有丰富的各种元素,化学兴趣小组采用“空气吹出法”从浓海水吹出元素⑩形成的单质Br2,常温下,Br2的颜色为深红棕色液体,吹出的溴用纯碱溶液吸收,吸收溴的主要反应为:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),当吸收1molBr2时,转移电子的物质的量为_______ mol。反应产物 的VSEPR模型名称为
的VSEPR模型名称为_______

(1)写出一种由元素①和⑤形成的常见化合物的电子式为
(2)由②形成的单质是一种是硬度很大,熔点很高的晶体,则该晶体属于
(3)③④⑤三种元素的第一电离能从大到小排序为
(4)写出工业上冶炼⑥单质的化学方程式
(5)列举元素⑦形成的最高价含氧酸的用途
(6)元素⑧的核外电子排布式为
(7)下图为⑨晶体的晶胞结构。若晶胞的棱长为acm,则两个最近的⑨原子之间的距离是

(8)天津市有着丰富的海水资源,海水中含有丰富的各种元素,化学兴趣小组采用“空气吹出法”从浓海水吹出元素⑩形成的单质Br2,常温下,Br2的颜色为深红棕色液体,吹出的溴用纯碱溶液吸收,吸收溴的主要反应为:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),当吸收1molBr2时,转移电子的物质的量为
 的VSEPR模型名称为
的VSEPR模型名称为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D是元素周期表中前10号元素,它们的原子半径依次减小。D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3杂化。请回答下列问题。
(1)A、B、C的第一电离能由小到大的顺序为____________________ (用元素符号表示)。
(2)M是含有__________ 键(填“极性”或“非极性”)的__________ 分子(填“极性”或“非极性”)。
(3)N是一种易液化的气体,请简述其易液化的原因:__________________________ 。
(4)W分子的VSEPR模型的空间构型为________ ,W分子的空间构型为________ 。
(5)AB-离子中和B2分子的π键数目比为____________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)M是含有
(3)N是一种易液化的气体,请简述其易液化的原因:
(4)W分子的VSEPR模型的空间构型为
(5)AB-离子中和B2分子的π键数目比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】在人类文明的历程中,改变世界的事物很多,其中铁、硝酸钾、青霉素、二氧化硅等17种物质重点改变过人类世界。
(1)铁原子在基态时,价电子排布式为__________________________________ 。
(2) 硝酸钾中NO3-的空间构型为________ ,写出与NO3-互为等电子体的一种非极性分子化学式_________________________________ 。
(3)6-氨基青霉烷酸的结构如图所示,其中采用sp3杂化的原子有___________ 。

(4)下图甲所示为血红素的结构。血红素中四种非金属元素的电负性由小到大的顺序是_______ 请在图乙中用适当的方式标出配位键________ 。

(5)在二氧化硅晶体中,硅原子的价电子层原子轨道发生了杂化,杂化的方式是______ ,O-Si-O 夹角是____________________ 。
(1)铁原子在基态时,价电子排布式为
(2) 硝酸钾中NO3-的空间构型为
(3)6-氨基青霉烷酸的结构如图所示,其中采用sp3杂化的原子有

(4)下图甲所示为血红素的结构。血红素中四种非金属元素的电负性由小到大的顺序是

(5)在二氧化硅晶体中,硅原子的价电子层原子轨道发生了杂化,杂化的方式是
您最近一年使用:0次
【推荐2】硫、硒(Se)等元素在化合物中衣现出多种氧化态,其化合物在研究和生产中有许多重要的用途。请回答下列问题:
(1)H2S的沸点低于H2O,原因为___________ 。
(2)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒:
①金属钠可以导电的原因为___________ 。
② 的键角为
的键角为___________ 。
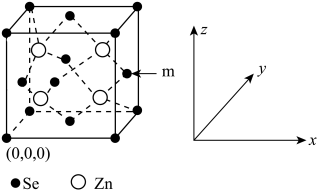
(3)硒化锌(晶胞结构如图所示)属于立方体系,可用于半导体掺杂物。
①两个距离最近的Se原子之间的距离为___________ (用含α的代数式表示)nm。
②m原子的分数坐标为___________ 。
③阿伏加德罗常数的值NA=___________ 。
④请在所提供的图中画出该晶胞沿z轴方向的投影图_________ ,___________ (填化学式),其原因为___________ 。
(1)H2S的沸点低于H2O,原因为
(2)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒:
①金属钠可以导电的原因为
②
 的键角为
的键角为(3)硒化锌(晶胞结构如图所示)属于立方体系,可用于半导体掺杂物。
①两个距离最近的Se原子之间的距离为
②m原子的分数坐标为
③阿伏加德罗常数的值NA=
④请在所提供的图中画出该晶胞沿z轴方向的投影图

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、P、Q为周期表前四周期中原子序数依次增大的元素。X原子2p能级有两个未成对电子,但没有空轨道。Y原子K层的电子数与M层的电子数的乘积等于其L层的电子数。Z与X同族。P原子的基态+2价阳离子的价电子排布为3d2。Q位于第ⅠB族。根据以上信息,回答下列问题。
(1)X的基态原子核外有________ 种不同运动状态的电子。
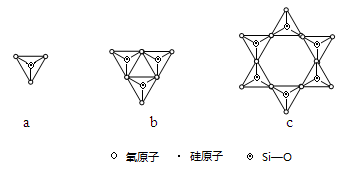
(2)Y与X可以形成多种复杂阴离子,如图所示,若其中a对应的阴离子化学式为SiO44—,则c对应的阴离子的化学式为______ 。
(3)Z能形成很多种含氧酸,如H2ZO3、H2ZO4。Z的某种含氧酸分子式为H2Z2O7,属于二元酸,已知其结构中所有原子都达到稳定结构,且不存在非极性键,试写出其结构式______ (配位键须注明)。
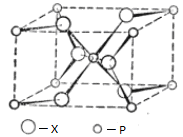
(4)P与X形成的某种晶体的晶胞结构如图所示,其晶体的化学式为_____ ,P的配位数为_________ 。
(5)向盛有QZX4的溶液中加入氨水至过量,现象为__________ ,相关反应的离子方程式为__________ 。NF3的空间构型是________ ,NF3不易与Cu2+形成配离子,其原因是__________ 。
(1)X的基态原子核外有
(2)Y与X可以形成多种复杂阴离子,如图所示,若其中a对应的阴离子化学式为SiO44—,则c对应的阴离子的化学式为

(3)Z能形成很多种含氧酸,如H2ZO3、H2ZO4。Z的某种含氧酸分子式为H2Z2O7,属于二元酸,已知其结构中所有原子都达到稳定结构,且不存在非极性键,试写出其结构式
(4)P与X形成的某种晶体的晶胞结构如图所示,其晶体的化学式为

(5)向盛有QZX4的溶液中加入氨水至过量,现象为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等铁的配合物用途非常广泛。回答下列问题:
(1)基态Fe原子价层电子的电子排布式为_______ 。
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是_______ 。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是_______ 。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(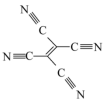 )。
)。
①CH3CN中碳原子的杂化方式是_______ 。
②TCNE中第一电离能较大的是_______ (填元素符号),分子中所有原子_______ (填“在”或“不在”)同一平面,分子中σ 键与π键的数目之比是_______ 。
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成,Fe3C的晶胞结构如图所示(NA代表阿伏加德罗常数的数值):

Fe3C的密度为_______ (列出计算式)g·cm-3(1Å=10-8 cm)。
(1)基态Fe原子价层电子的电子排布式为
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(
 )。
)。①CH3CN中碳原子的杂化方式是
②TCNE中第一电离能较大的是
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成,Fe3C的晶胞结构如图所示(NA代表阿伏加德罗常数的数值):

Fe3C的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】[化学——选修3:物质结构与性质]原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36。已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T位于周期表的ds区,且最外层只有一个电子。
(1)Y原子核外共有_______ 种不同运动状态的电子,T原子的价层电子排布式_______ 。
(2)由X、Y、Z形成的离子ZXY -与XZ2互为等电子体,则ZXY -中X原子的杂化轨道类型为____ 。
(3)Z与R能形成化合物甲,1mol甲中含_____ mol共价键,甲与氢氟酸反应,生成物的分子空间构型分别为________ 。
(4)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为__________ 。

(5)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为__________ 。
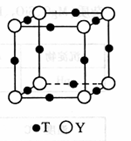
(6)T和Y形成的晶体的晶胞结构如图所示,Y离子的配位数是___ 。设晶胞棱长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为_______ (用含a、b的式子表示)。
(1)Y原子核外共有
(2)由X、Y、Z形成的离子ZXY -与XZ2互为等电子体,则ZXY -中X原子的杂化轨道类型为
(3)Z与R能形成化合物甲,1mol甲中含
(4)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为

(5)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为
(6)T和Y形成的晶体的晶胞结构如图所示,Y离子的配位数是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】总订单数已经超过1000架的国产大飞机C919预定在今年交付,其制造使用了较多含硼材料(如硼纤维、氮化硼等),多项技术打破了外国垄断。
(1)原子的能量由核电荷数、电子数、_______ 三个因素共同决定;基态B原子的核外电子填充在_______ 个轨道中。
(2)耐高温材料立方BN制备流程中用到NH3、BCl3和触媒剂Ca3B2N4。
①Ca、B、N三种元素电负性从大到小的顺序为_______ 。
②BCl3中B原子的_______ 轨道与Cl原子的_______ 轨道形成σ键;形成BCl3过程中基态B原子价电子层电子先激发,再杂化,激发后B原子的价电子排布图为_______ 。
③BCl3在四氯化碳中的溶解度远大于NH3,原因是_______ 。
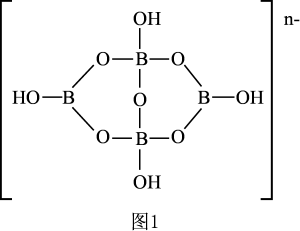
(3)硼砂是非常重要的含硼矿物。一种硼砂阴离子的结构如图1所示,则1mol该阴离子存在的配位键物质的量为_______ ,n=_______ 。
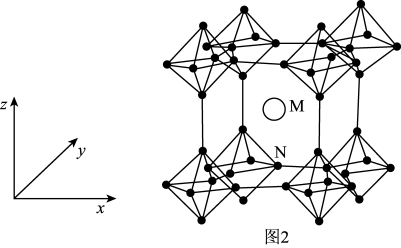
(4)制造硼合金的原料硼化钙(CaB6)晶胞结构如图2所示,硼原子全部组成B6正八面体,各个顶点通过B-B键互相连接成三维骨架。已知该晶体晶胞参数为apm,B6八面体中B-B键的键长为dpm,M点原子的坐标参数为( ,
, ,
, ),则N点原子的坐标参数为(___,1,0)。
),则N点原子的坐标参数为(___,1,0)。_______
(1)原子的能量由核电荷数、电子数、
(2)耐高温材料立方BN制备流程中用到NH3、BCl3和触媒剂Ca3B2N4。
①Ca、B、N三种元素电负性从大到小的顺序为
②BCl3中B原子的
③BCl3在四氯化碳中的溶解度远大于NH3,原因是
(3)硼砂是非常重要的含硼矿物。一种硼砂阴离子的结构如图1所示,则1mol该阴离子存在的配位键物质的量为

(4)制造硼合金的原料硼化钙(CaB6)晶胞结构如图2所示,硼原子全部组成B6正八面体,各个顶点通过B-B键互相连接成三维骨架。已知该晶体晶胞参数为apm,B6八面体中B-B键的键长为dpm,M点原子的坐标参数为(
 ,
, ,
, ),则N点原子的坐标参数为(___,1,0)。
),则N点原子的坐标参数为(___,1,0)。
您最近一年使用:0次



