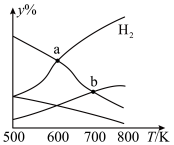
以二氧化碳和氢气为原料制取乙醇的反应为2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1:3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是
CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1:3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是
 CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1:3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是
CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1:3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是
| A.a点的平衡常数小于b点 |
| B.b点,v正(CO2)=v逆(H2O) |
| C.a点,H2和H2O物质的量相等 |
| D.其他条件恒定,充入更多H2,v(CO2)不变 |
14-15高三下·福建宁德·阶段练习 查看更多[12]
贵州省凯里市第一中学2021-2022学年高二上学期期中考试化学(理科)试题四川省汉源县第二中学2019-2020学年高二下学期第二次月考化学试题河南省洛阳市新安县第一高级中学2020-2021学年高二10月月考化学试题辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题山东省潍坊市临朐县实验中学2020-2021学年高二9月月考化学试题广东省第二师范学院番禺附属中学2019-2020学年高二下学期期中段考化学试题广东省蕉岭县蕉岭中学2019-2020学年高二上学期第一次段考化学试题贵州省凯里市第一中学2019-2020学年高二上学期期中考试化学(理)试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题2016届河北省衡水中学高三下一调考试理综化学试卷2015届福建省宁德市普通高中高三毕业班5月质检化学试卷
更新时间:2019-10-30 14:10:08
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.对于 的 的 溶液,升高温度,溶液pH上升 溶液,升高温度,溶液pH上升 |
| B.温度越高,化学反应速率越快,化学平衡常数越大 |
C.常温下,能证明乙酸是弱电解质的事实是 CH3COONa溶液pH大于7 CH3COONa溶液pH大于7 |
| D.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容器中充入一定量M和N,发生反应: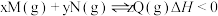 ,平衡时M的浓度为
,平衡时M的浓度为 ,平衡后第
,平衡后第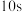 时保持温度不变,将容器的容积扩大到原来的2倍,第
时保持温度不变,将容器的容积扩大到原来的2倍,第 再次达到平衡时,测得M的浓度为
再次达到平衡时,测得M的浓度为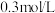 。下列有关判断正确的是
。下列有关判断正确的是
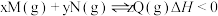 ,平衡时M的浓度为
,平衡时M的浓度为 ,平衡后第
,平衡后第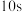 时保持温度不变,将容器的容积扩大到原来的2倍,第
时保持温度不变,将容器的容积扩大到原来的2倍,第 再次达到平衡时,测得M的浓度为
再次达到平衡时,测得M的浓度为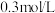 。下列有关判断正确的是
。下列有关判断正确的是A.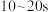 之间,M的平均反应速率为 之间,M的平均反应速率为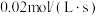 |
| B.降低温度,M的体积分数增大 |
| C.增大压强,平衡正向移动,平衡常数增大 |
D.反应方程式中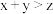 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】臭氧是理想的烟气脱硝试剂,其脱硝反应为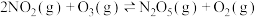 ,若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
,若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是

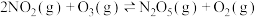 ,若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
,若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
A.0~3s内,反应速率为 |
| B.降低温度,平衡常数增大 |
C. 时的改变可能是加入了催化剂或改变压强,平衡不移动 时的改变可能是加入了催化剂或改变压强,平衡不移动 |
D. 时刻,该反应达平衡状态 时刻,该反应达平衡状态 |
您最近半年使用:0次
单选题
|
适中
(0.65)
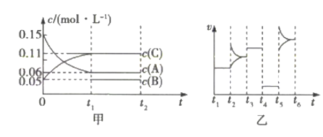
【推荐2】向某密闭容器中充入0.3mol A、0.1mol C和一定量的B三种气体。一定条件下发生反应,各物质的浓度随时间的变化如甲图所示[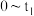 阶段的c(B)变化未画出]。乙图为
阶段的c(B)变化未画出]。乙图为 时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,
时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,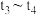 阶段改变的条件为使用催化剂。下列说法不正确的是
阶段改变的条件为使用催化剂。下列说法不正确的是
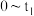 阶段的c(B)变化未画出]。乙图为
阶段的c(B)变化未画出]。乙图为 时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,
时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同, 阶段改变的条件为使用催化剂。下列说法不正确的是
阶段改变的条件为使用催化剂。下列说法不正确的是
A.若 =15s,则用A的浓度变化表示的0~ =15s,则用A的浓度变化表示的0~ 阶段的平均反应速率为0.006 阶段的平均反应速率为0.006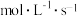 |
B. 阶段改变的条件一定为减小压强,即增大容器体积 阶段改变的条件一定为减小压强,即增大容器体积 |
| C.起始时该容器的容积为2 L,B的起始物质的量为0.02 mol |
D.该反应的化学方程式为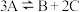 |
您最近半年使用:0次
【推荐1】一定温度下,在三个容积均为1.0L的恒容密闭容器中,充入一定量的 和
和 发生反应:
发生反应: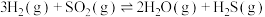
下列说法正确的是
 和
和 发生反应:
发生反应: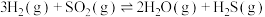
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
 |  |  |  | ||
| 容器I | 300 | 0.3 | 0.1 | / | 0.02 |
| 容器II | 300 | 0.6 | 0.2 | / | / |
| 容器III | 240 | 0.3 | 0.1 | / | 0.01 |
A.该反应的 |
B.达到平衡所需时间: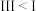 |
C.容器II达到平衡时 的物质的量是0.04mol 的物质的量是0.04mol |
D.240℃时,起始时向容器III中充入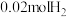 、 、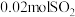 、 、 、 、 ,此时反应将向正反应方向进行 ,此时反应将向正反应方向进行 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某温度时,在体积为 2L 的恒容容器中发生反应, 2A(g) 2B(g) C(g) ΔH <0 ,起始时加入2 mol A 气体,测得 C 的物质的量随时间变化如表所示:
下列说法正确的是
t / min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
C 物质的量/mol | 0 | 0.50 | 0.70 | 0.80 | 0.85 | 0.86 | 0.86 |
| A.当时间达到 60 min 时,反应恰好达到平衡状态 |
| B.在 20—30 min 内以 C 表示的反应速率为 0.005mol·L-1·min-1 |
| C.平衡时容器内压强为起始时容器内压强的 2.86 倍 |
| D.平衡时 A 的转化率为 43% |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】甲酸(HCOOH)具有液氢储存材料和清洁制氢的巨大潜力,产生氢气的反应为: ,在T℃时,向体积不等的恒容密闭容器中分别加入一定量的
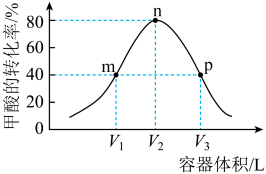
,在T℃时,向体积不等的恒容密闭容器中分别加入一定量的 ,反应相同时间,测得各容器中甲酸的转化率与容器体积的关系如图所示,其中m、n点反应达平衡。下列说法正确的是
,反应相同时间,测得各容器中甲酸的转化率与容器体积的关系如图所示,其中m、n点反应达平衡。下列说法正确的是
 ,在T℃时,向体积不等的恒容密闭容器中分别加入一定量的
,在T℃时,向体积不等的恒容密闭容器中分别加入一定量的 ,反应相同时间,测得各容器中甲酸的转化率与容器体积的关系如图所示,其中m、n点反应达平衡。下列说法正确的是
,反应相同时间,测得各容器中甲酸的转化率与容器体积的关系如图所示,其中m、n点反应达平衡。下列说法正确的是
A.m、p两点中,甲酸的浓度: |
B. |
C.n点时再充入一定量 ,达平衡时甲酸的转化率升高 ,达平衡时甲酸的转化率升高 |
D.p点时 的体积分数约为 的体积分数约为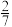 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】拥有中国自主知识产权的全球首套煤制乙醇工业化项目投产成功。某煤制乙醇过程表示如下:
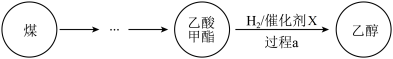
过程a包括以下3个主要反应:
I.

Ⅱ.

Ⅲ.

相同时间内,测得乙酸甲酯转化率随温度的变化如图1所示,乙醇和乙酸乙酯的选择性[乙醇选择性 ]随温度的变化如图2所示。
]随温度的变化如图2所示。

下列说法不正确的是

过程a包括以下3个主要反应:
I.


Ⅱ.


Ⅲ.


相同时间内,测得乙酸甲酯转化率随温度的变化如图1所示,乙醇和乙酸乙酯的选择性[乙醇选择性
 ]随温度的变化如图2所示。
]随温度的变化如图2所示。
下列说法不正确的是
| A.205℃后反应Ⅲ开始发生反应 |
| B.225~235℃,反应I处于平衡状态 |
| C.温度可影响催化剂的选择性,从而影响目标产物乙醇的选择性 |
| D.205℃时,CH3COOCH3起始物质的量为5mol,转化率为30%,则最终生成乙醇0.6mol |
您最近半年使用:0次

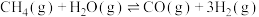 。研究
。研究 和
和 的反应机理,有利于开发新的氨气合成技术。向一恒容密闭容器中加入1mol
的反应机理,有利于开发新的氨气合成技术。向一恒容密闭容器中加入1mol 和一定量的
和一定量的 ,发生反应
,发生反应 随温度的变化如图所示。下列说法正确的是
随温度的变化如图所示。下列说法正确的是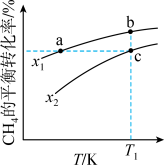



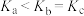
 ,在温度为
,在温度为 时,平衡体系中
时,平衡体系中 的体积分数随压强的变化曲线如图所示。下列说法正确的是
的体积分数随压强的变化曲线如图所示。下列说法正确的是

 两点的正反应速率:
两点的正反应速率:
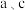 两点气体的颜色:a深,c浅
两点气体的颜色:a深,c浅
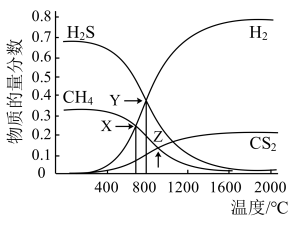
 CS2(g)+4H2(g)。向恒容密闭容器中充入0.lmolCH4和0.2molH2S,下图所示:
CS2(g)+4H2(g)。向恒容密闭容器中充入0.lmolCH4和0.2molH2S,下图所示: