研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)现有反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0。在850℃时,K=1。
CH3OH(g)+H2O(g) ΔH<0。在850℃时,K=1。
①如果上述反应的平衡常数K值变大,该反应___ (填字母)。
a.一定向正反应方向移动 b.在平衡移动过程中正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动过程中逆反应速率先减小后增大
②若反应容器的容积为2.0L,反应时间4.0min,容器内气体的物质的量减小了0.8mol,在这段时间内CO2的平均反应速率为___ 。
③在850℃时,若向1L的密闭容器中同时充入3.0mol CO2、1.0molH2、1.0molCH3OH、5.0molH2O(g),上述反应向___ (填“正反应”或“逆反应”)方向进行。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是___ 。
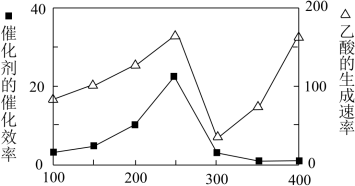
②为了提高该反应中CO2的转化率,可以采取的措施是___ 。(写一条即可)
(1)现有反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0。在850℃时,K=1。
CH3OH(g)+H2O(g) ΔH<0。在850℃时,K=1。①如果上述反应的平衡常数K值变大,该反应
a.一定向正反应方向移动 b.在平衡移动过程中正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动过程中逆反应速率先减小后增大
②若反应容器的容积为2.0L,反应时间4.0min,容器内气体的物质的量减小了0.8mol,在这段时间内CO2的平均反应速率为
③在850℃时,若向1L的密闭容器中同时充入3.0mol CO2、1.0molH2、1.0molCH3OH、5.0molH2O(g),上述反应向
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是

②为了提高该反应中CO2的转化率,可以采取的措施是
更新时间:2019-11-21 16:35:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】水溶性硝态氮(以NO 、NO
、NO 等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。
等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。
(1)在反硝化细菌作用下,用葡萄糖处理酸性废水中的NO ,产生两种对大气无污染的气体。该反应的离子方程式为
,产生两种对大气无污染的气体。该反应的离子方程式为___________ 。
(2)纳米铁铜双金属有巨大的比表面积和很高的反应活性,可用于水体脱硝。
① 纳米铁铜双金属与普通铁铜双金属脱硝效果(以处理某硝酸盐为例)如图-1所示。在0到20min内,纳米铁铜双金属脱硝效果显著,其原因可能是___________ 。
② 研究表明水体中溶解氧的存在降低了纳米铁铜双金属脱硝的效果,验证的实验方案是______ 。

(3)Jetten 等人提出了利用厌氧氨氧化菌细胞中的三种酶处理废水中NH3和NO 的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为
的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为___________ 、___________ 。
 、NO
、NO 等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。
等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。(1)在反硝化细菌作用下,用葡萄糖处理酸性废水中的NO
 ,产生两种对大气无污染的气体。该反应的离子方程式为
,产生两种对大气无污染的气体。该反应的离子方程式为(2)纳米铁铜双金属有巨大的比表面积和很高的反应活性,可用于水体脱硝。
① 纳米铁铜双金属与普通铁铜双金属脱硝效果(以处理某硝酸盐为例)如图-1所示。在0到20min内,纳米铁铜双金属脱硝效果显著,其原因可能是
② 研究表明水体中溶解氧的存在降低了纳米铁铜双金属脱硝的效果,验证的实验方案是

(3)Jetten 等人提出了利用厌氧氨氧化菌细胞中的三种酶处理废水中NH3和NO
 的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为
的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某化学小组利用硫代硫酸钠进行了相关的实验。
Ⅰ.已知:Na2S2O3+H2 SO4 Na2SO4+SO2↑+S↓+H2O,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)该实验①、②可探究温度对反应速率的影响,因此V1=V2=____ ,V3=___ ;
(2)若V4=10.0,V5=6.0,则实验①、③可探究_____ 对反应速率的影响。
Ⅱ.利用反应:I2+2Na2S2O3 Na2S4O6+2NaI可定量测定硫代硫酸钠(Mr=158)的纯度,现在称取wg硫代硫酸钠固体样品,配成250mL的溶液,取25.00mL置于锥形瓶中,加入指示剂,用amol/L的碘水滴定,消耗碘水b mL,则:
(3)滴定时,将碘水注入___ (填“酸式”或“碱式”)滴定管中,滴定应选择的指示剂是____ ,滴定终点的现象为________ 。
(4)对于该滴定实验的有关操作或误差分析正确的是____ 。
a.滴定前,要用对应装入的溶液润洗锥形瓶和滴定管
b.滴定过程中,标准液滴到锥形瓶外,会使所测得的结果偏大
c.滴定开始时滴定管尖嘴有气泡,滴定结束后气泡消失,测得纯度将偏小
d.滴定前仰视读数而滴定结束时平视读数,则所测得的纯度将会偏小
(5)样品中硫代硫酸钠纯度的表达式为____ 。
Ⅰ.已知:Na2S2O3+H2 SO4 Na2SO4+SO2↑+S↓+H2O,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(1)该实验①、②可探究温度对反应速率的影响,因此V1=V2=
(2)若V4=10.0,V5=6.0,则实验①、③可探究
Ⅱ.利用反应:I2+2Na2S2O3 Na2S4O6+2NaI可定量测定硫代硫酸钠(Mr=158)的纯度,现在称取wg硫代硫酸钠固体样品,配成250mL的溶液,取25.00mL置于锥形瓶中,加入指示剂,用amol/L的碘水滴定,消耗碘水b mL,则:
(3)滴定时,将碘水注入
(4)对于该滴定实验的有关操作或误差分析正确的是
a.滴定前,要用对应装入的溶液润洗锥形瓶和滴定管
b.滴定过程中,标准液滴到锥形瓶外,会使所测得的结果偏大
c.滴定开始时滴定管尖嘴有气泡,滴定结束后气泡消失,测得纯度将偏小
d.滴定前仰视读数而滴定结束时平视读数,则所测得的纯度将会偏小
(5)样品中硫代硫酸钠纯度的表达式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】汽车尾气中的CO、NO2在一定条件下可以发生反应:4CO(g)+2NO2(g)4CO2(g)+N2(g) ΔH=−1 200 kJ·mol-1。在一定温度下,向容积固定为2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示:

(1)0~10 min内该反应的平均速率v(CO)=________ ,从11 min起其他条件不变,压缩容器的容积变为1 L,则n(NO2)的变化曲线可能为图中的______ (填字母)。
(2)恒温恒容条件下,不能说明该反应已达到平衡状态的是________ (填字母)。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2)
D.容器内混合气体密度保持不变

(1)0~10 min内该反应的平均速率v(CO)=
(2)恒温恒容条件下,不能说明该反应已达到平衡状态的是
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2)
D.容器内混合气体密度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知:已知: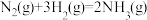
 。
。
某温度下,将一定量的N2和H2的混合气体充入1L的密闭容器中,充分反应后达到平衡。请回答:
(1)若反应速率分别用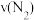 ,
,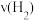 表示,则
表示,则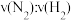
___________
(2)若保持其他条件不变,升高温度,平衡___________ (填“向正反应方向移动”、“向逆反应方向移动”或“不移动”),化学平衡常数___________ (填增大、减小或不变)
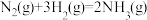
 。
。某温度下,将一定量的N2和H2的混合气体充入1L的密闭容器中,充分反应后达到平衡。请回答:
(1)若反应速率分别用
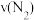 ,
,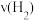 表示,则
表示,则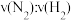
(2)若保持其他条件不变,升高温度,平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
Ⅰ.一定条件下,在容积为 的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
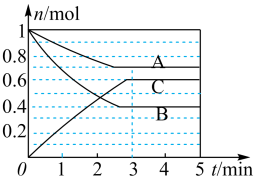
(1)达到平衡后加压,C的含量_______ (填写“变大”“变小”或“不变”)。
(2)该反应的反应速率v随时间t的关系如图所示。
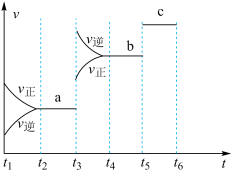
①根据图判断,在 时刻改变的外界条件是
时刻改变的外界条件是_______ 。
②a、b、c对应的平衡状态中,A的转化率最大的是状态_______ 。
Ⅱ.在密闭容器中充入一定量的 ,发生反应
,发生反应
 。如图所示为
。如图所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。

(3)该反应的逆反应是_______ (填“吸热反应”或“放热反应”)。
(4)N点 的体积分数是
的体积分数是_______ 。
(5)M点对应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅰ.一定条件下,在容积为
 的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
(1)达到平衡后加压,C的含量
(2)该反应的反应速率v随时间t的关系如图所示。

①根据图判断,在
 时刻改变的外界条件是
时刻改变的外界条件是②a、b、c对应的平衡状态中,A的转化率最大的是状态
Ⅱ.在密闭容器中充入一定量的
 ,发生反应
,发生反应
 。如图所示为
。如图所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)该反应的逆反应是
(4)N点
 的体积分数是
的体积分数是(5)M点对应的平衡常数

 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)在一定条件下,可逆反应mA+nB⇌pC达到平衡,若:
①A、B、C都是气体,减小压强,平衡正向移动,则m+n和p的关系是_______ 。
②A、C是气体,增加B的量,平衡不移动,则B为_______ 。
③A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是_______ 。
④加热后,可使C的质量增加,则正反应是_______ (填“放热”或“吸热”)反应。
(2)现有可逆反应A(气)+B(气)⇌3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
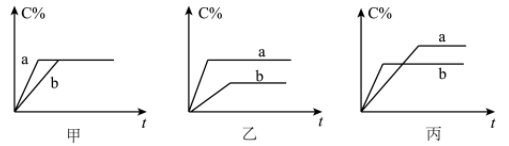
Ⅰ.若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则_______ 曲线是表示有催化剂时的情况。
Ⅱ.若乙图中的a曲线表示200℃和b曲线表示100℃时的情况,则此可逆反应的正反应是_______ (填“放热”或“吸热”)反应。
Ⅲ.若丙图中两条曲线分别表示不同压强下的情况,则_______ 曲线是表示压强较大的情况。
(1)在一定条件下,可逆反应mA+nB⇌pC达到平衡,若:
①A、B、C都是气体,减小压强,平衡正向移动,则m+n和p的关系是
②A、C是气体,增加B的量,平衡不移动,则B为
③A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
④加热后,可使C的质量增加,则正反应是
(2)现有可逆反应A(气)+B(气)⇌3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:

Ⅰ.若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则
Ⅱ.若乙图中的a曲线表示200℃和b曲线表示100℃时的情况,则此可逆反应的正反应是
Ⅲ.若丙图中两条曲线分别表示不同压强下的情况,则
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在一密闭容器中发生反应N2(g)+3H2(g) 2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是_________ 。
A.增大压强 B.降低温度 C.使用催化剂 D.增大反应物的浓度
(2)上述反应达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
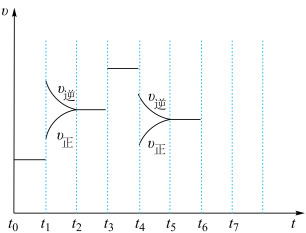
t1、t3、t4时刻分别改变了反应的一个条件,其中t1时刻改变的条件是________ ;某时刻改变的条件是保持压强不变,向容器中冲入氩气,这个时刻是________ 。
(3)下列时间段中,混合气体中氮气百分含量最高的是________ ,氢气浓度最大的是________
A.t0~t1 B.t2~t3 C.t4~t5 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为________ 。
(5)合成氨及其相关工业中,部分物质间的转化关系如下:
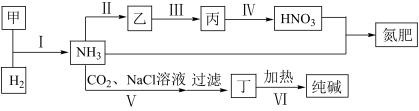
下列说法不正确的是( )
A.甲、乙、丙三种物质都含有氮元素
B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用
D.丁为NaHCO3
E. V过程中先通入CO2 ,再通入NH3
 2NH3(g) ΔH<0
2NH3(g) ΔH<0(1)改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是
A.增大压强 B.降低温度 C.使用催化剂 D.增大反应物的浓度
(2)上述反应达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。

t1、t3、t4时刻分别改变了反应的一个条件,其中t1时刻改变的条件是
(3)下列时间段中,混合气体中氮气百分含量最高的是
A.t0~t1 B.t2~t3 C.t4~t5 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为
(5)合成氨及其相关工业中,部分物质间的转化关系如下:

下列说法不正确的是
A.甲、乙、丙三种物质都含有氮元素
B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用
D.丁为NaHCO3
E. V过程中先通入CO2 ,再通入NH3
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】研究 对节能减排有重要意义,回答下列问题:
对节能减排有重要意义,回答下列问题:
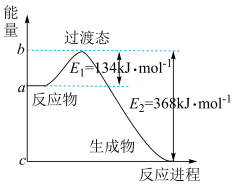
(1)如图是 和
和 反应生成
反应生成 和
和 过程中能量变化示意图,请写出
过程中能量变化示意图,请写出 和
和 反应的热化学方程式:
反应的热化学方程式:___________ ,若反应中转移了 ,则参加反应的
,则参加反应的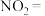
___________ g。
(2)已知反应: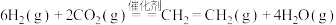 ,温度对
,温度对 的平衡转化率和催化剂催化效率的影响如图所示:
的平衡转化率和催化剂催化效率的影响如图所示:
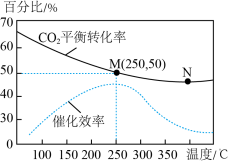
①此反应正反应为___________ 反应。
②化学平衡常数: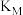
___________  (填“>”或“<”)。
(填“>”或“<”)。
③若初始投料比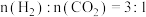 ,则图中
,则图中 点的乙烯体积分数约为
点的乙烯体积分数约为___________ 。
④ 时,
时,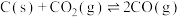 的平衡常数
的平衡常数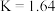 ,此反应的
,此反应的
___________ 0(填“>”或“<”),相同条件下测得高炉内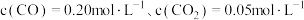 ,此时反应向
,此时反应向___________ (填“正”或“逆”)方向进行。
 对节能减排有重要意义,回答下列问题:
对节能减排有重要意义,回答下列问题:
(1)如图是
 和
和 反应生成
反应生成 和
和 过程中能量变化示意图,请写出
过程中能量变化示意图,请写出 和
和 反应的热化学方程式:
反应的热化学方程式: ,则参加反应的
,则参加反应的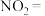
(2)已知反应:
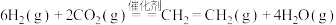 ,温度对
,温度对 的平衡转化率和催化剂催化效率的影响如图所示:
的平衡转化率和催化剂催化效率的影响如图所示:
①此反应正反应为
②化学平衡常数:
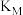
 (填“>”或“<”)。
(填“>”或“<”)。③若初始投料比
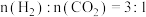 ,则图中
,则图中 点的乙烯体积分数约为
点的乙烯体积分数约为④
 时,
时,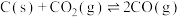 的平衡常数
的平衡常数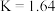 ,此反应的
,此反应的
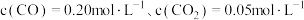 ,此时反应向
,此时反应向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究NO2、SO2、CO等大气污染物的处理具有重要意义。NO2可用下列反应来处理:
6 NO2(g)+8NH3(g) 7N2(g)+12H2O(g)+Q(Q>0)。
7N2(g)+12H2O(g)+Q(Q>0)。
完成下列填空:
(1)反应的平衡常数大,处理NO2的效率高。增大该反应平衡常数的措施有___________ 。
(2)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是___________ 。
a.c(NO2)∶c(NH3) = 3∶4 b.6v(NO2) = 7v(N2)
c.容器内气体总压强不再变化 d.容器内气体密度不再变化
(3)若平衡时NO2和N2的浓度之比为 ,保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比
,保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比_________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
(4)某温度下,在一个容积为2升的反应容器内,上述反应2分钟后达到平衡,测得刚好有3mol电子发生转移,则在2分钟内NH3的平均反应速率为:
v(NH3) =_______________________ 。
6 NO2(g)+8NH3(g)
 7N2(g)+12H2O(g)+Q(Q>0)。
7N2(g)+12H2O(g)+Q(Q>0)。完成下列填空:
(1)反应的平衡常数大,处理NO2的效率高。增大该反应平衡常数的措施有
(2)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是
a.c(NO2)∶c(NH3) = 3∶4 b.6v(NO2) = 7v(N2)
c.容器内气体总压强不再变化 d.容器内气体密度不再变化
(3)若平衡时NO2和N2的浓度之比为
 ,保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比
,保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。(4)某温度下,在一个容积为2升的反应容器内,上述反应2分钟后达到平衡,测得刚好有3mol电子发生转移,则在2分钟内NH3的平均反应速率为:
v(NH3) =
您最近一年使用:0次



