[化学—选修3:物质结构与性质]国务院批复通过的《全国矿产资源规划(2016﹣﹣2020年)》中,首次将萤石等24种矿产列入战略性矿产目录。萤石为氟化钙的俗名,其重要用途是生产氢氟酸。
(1)基态F原子核外电子共有_____ 种运动状态,基态Ca2+的最外层电子排布图为_____ 。
(2)实验室制氟化氢是用萤石与浓硫酸反应,但该反应不可以在玻璃器皿中进行,请用化学反应方程式解释原因_____ ,该反应涉及的元素电负性最大的是_____ (用元素符号表示)。该反应的产物之一会与反应物继续反应生成H2SiF6,则H2SiF6分子的中心原子价层电子对数为_____ 。
(3)CaF2与CaCl2熔点比较低的物质是_____ ,原因是_______________ 。CaF2晶胞如图,其中Ca2+的配位数为_____ 。在CaF2晶体中Ca2+的离子半径为a cm,F﹣的离子半径为bcm;则CaF2的密度为_____ g⋅cm﹣3(设阿伏加 德罗常数的值为NA)。

(1)基态F原子核外电子共有
(2)实验室制氟化氢是用萤石与浓硫酸反应,但该反应不可以在玻璃器皿中进行,请用化学反应方程式解释原因
(3)CaF2与CaCl2熔点比较低的物质是

更新时间:2019-12-20 13:12:56
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】三草酸合铁酸钾{K3[Fe(C2O4)3]·3H2O}是制备铁触媒的主要原料,在光照下能分解:2 K3[Fe(C2O4)3]·3H2O 3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:
3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:
(1)基态Fe原子的电子排布式为___________ ,基态Fe2+与Fe3+中未成对电子的数目之比为___________ 。
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是___________ (填元素符号,下同),电负性最大的是___________ 。
(3)H2O分子的立体构型为___________ 。
(4)金刚石的晶胞结构如图1所示,碳原子分别位于顶点、面心和体内。
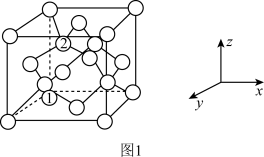
若图中原子1的坐标为(0,0,0),则原子2的坐标为___________ 。若金刚石的晶胞边长为apm,则其中碳碳键的键长d___________ (用含a的代数式表示)pm。
(5)铁有δ、γ、α三种同素异形体(如图2),三种晶体在不同温度下能发生转化。
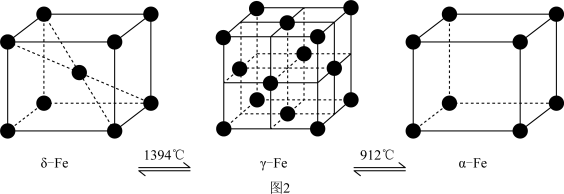
①δ、γ、α三种晶体晶胞中铁原子的配位数之比为___________ 。
②若δ-Fe晶胞边长为acm,α-Fe晶胞边长为bcm,则两种晶胞的密度之比为___________ (用含a、b的代数式表示)。
 3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:
3K2C2O4+2FeC2O4+2CO2↑+6H2O。回答下列问题:(1)基态Fe原子的电子排布式为
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是
(3)H2O分子的立体构型为
(4)金刚石的晶胞结构如图1所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为(0,0,0),则原子2的坐标为
(5)铁有δ、γ、α三种同素异形体(如图2),三种晶体在不同温度下能发生转化。

①δ、γ、α三种晶体晶胞中铁原子的配位数之比为
②若δ-Fe晶胞边长为acm,α-Fe晶胞边长为bcm,则两种晶胞的密度之比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】铁、钴、镍等金属及其化合物在科学研究和工业生产中应用非常广泛。回答下列问题:
(1)基态铁原子的核外电子排布式为___________ 。
(2)K3[Fe(CN)6 ]溶液可以检验Fe2+。K3[Fe(CN)6]中含有的σ键与π键的数目之比___________ , 与CN-互为等电子体的分子有___________ (举一例,填化学式)。
(3)酞菁钴的结构简式如图所示,其中三种非金属元素的电负性由大到小的顺序为___________ 。

(4)NiSO4是制备磁性材料和催化剂的重要中间体, 的空间构型为
的空间构型为___________ ,硫原子的杂化方式为___________ 。
(5)某氮化铁的晶胞结构如图所示:
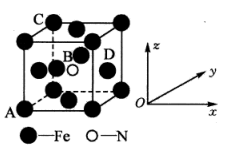
①原子坐标参数表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数A(0,0,0);B为( ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为___________ 。
②若该晶体的密度是ρg·cm-3 ,则晶胞中两个最近的Fe的核间距为___________ cm(用含ρ的代数式表示,NA表示阿伏加德罗常数的值)。
(1)基态铁原子的核外电子排布式为
(2)K3[Fe(CN)6 ]溶液可以检验Fe2+。K3[Fe(CN)6]中含有的σ键与π键的数目之比
(3)酞菁钴的结构简式如图所示,其中三种非金属元素的电负性由大到小的顺序为

(4)NiSO4是制备磁性材料和催化剂的重要中间体,
 的空间构型为
的空间构型为(5)某氮化铁的晶胞结构如图所示:

①原子坐标参数表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数A(0,0,0);B为(
 ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为②若该晶体的密度是ρg·cm-3 ,则晶胞中两个最近的Fe的核间距为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】国际权威学术期刊《自然》最近报道,我国科学家选择碲化锆(ZrTe5)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应。请回答下列问题:
(1)Zr是Ti的同族相邻元素,位于周期表的_______ 区;基态Te原子的价电子排布式是_______ 。
(2)周期表中As、Te分别与Se相邻,这三种元素第一电离能由大到小的顺序是_______ 。
(3)Cd2+与NH3可形成配离子[Cd(NH3)4]2+
①该离子中不含的化学键类型有_______ (填字母)。
A.离子键 B.配位键 C.σ键 D.共价键 E.氢键 F.π键
②已知该离子中2个NH3被2个Cl- 替代只得到一种结构,则该离子的立体构型为_______ 。
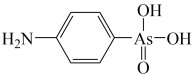
(4)含砷有机物“对氨基苯砷酸”的结构简式如图所示,As原子的轨道杂化类型为_______ ,1 个对氨基苯砷酸分子中含有σ键的数目为_______ 。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系Cd-Sn-As形成的化合物的晶胞结构如图所示,晶胞棱边夹角均为90° ,晶胞中部分原子的分数坐标如下表所示。
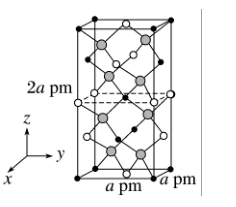
①找出此晶胞中距离Cd(0,0,0)最远的As的位置_______ (用分数坐标表示)。
②该化合物的化学式为_______ ,此晶体的密度为_______ g·cm-3(列出计算式,阿伏。加德罗常数的值为NA)。
(1)Zr是Ti的同族相邻元素,位于周期表的
(2)周期表中As、Te分别与Se相邻,这三种元素第一电离能由大到小的顺序是
(3)Cd2+与NH3可形成配离子[Cd(NH3)4]2+
①该离子中不含的化学键类型有
A.离子键 B.配位键 C.σ键 D.共价键 E.氢键 F.π键
②已知该离子中2个NH3被2个Cl- 替代只得到一种结构,则该离子的立体构型为
(4)含砷有机物“对氨基苯砷酸”的结构简式如图所示,As原子的轨道杂化类型为

(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系Cd-Sn-As形成的化合物的晶胞结构如图所示,晶胞棱边夹角均为90° ,晶胞中部分原子的分数坐标如下表所示。

| 坐标原子 | x | y | z |
| Cd | 0 | 0 | 0 |
| Sn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0. 125 |
②该化合物的化学式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】利用铁矿石(Fe2O3),可以制得Fe3[Fe(CN)6]2和Fe(SCN)3,请回答下列问题:
(1)基态Fe3+的价电子排布式为___________ 。
(2)O、S、C三种元素的电负性由大到小的顺序为___________ ,Fe(CO)5是一种浅黄色液体,熔点-20℃,沸点103℃。Fe(CO)5晶体类型是___________ 。
(3)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的分子为___________ (任写一种),SCN-中碳原子的杂化类型为___________ 。第一电离能I1(N)___________ I1(O)(填“大于”、“小于”或“等于”),理由是___________ 。
(4)钾晶体(其晶胞结构如图所示)的晶胞参数为apm。假定金属钾原子为等径的刚性小球且处于体对角线上的三个球相切,则钾原子的半径为___________ pm,晶体钾的密度计算式是___________ g/m3(设NA为阿伏伽德罗常数的值)

(1)基态Fe3+的价电子排布式为
(2)O、S、C三种元素的电负性由大到小的顺序为
(3)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的分子为
(4)钾晶体(其晶胞结构如图所示)的晶胞参数为apm。假定金属钾原子为等径的刚性小球且处于体对角线上的三个球相切,则钾原子的半径为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】原子序数小于等于36的Q、W、X、Y、Z五种元素,其中Q是形成化合物种类最多的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是______ 。
(2)1molQWX与1molWQ2Y所含σ键的比值为______ 。
(3)根据等电子体理论可以预测WXY-的空间构型为______ 。
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为______ 。
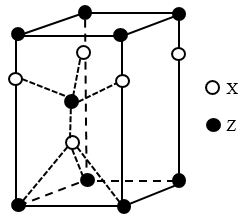
(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为。______ 。
②该化合物所属晶体类型为______ 晶体,预测其熔点应______ 金刚石(填“高于”或“低于”)。
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是
(2)1molQWX与1molWQ2Y所含σ键的比值为
(3)根据等电子体理论可以预测WXY-的空间构型为
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为

(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为。
②该化合物所属晶体类型为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】(1)Cd与Zn同族且相邻,若Cd基态原子将次外层1个d电子激发进入最外层的np能级,则该激发态原子的外围电子排布式为_______ 。
(2)一水合甘氨酸锌[(H2NCH2COO)2Zn·H2O]是一种饲料添加剂,该化合物中所涉及的 第二周期元素的第一电离能由大到小的顺序是_______ (用元素符号表示);
(3)噻吩(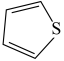 )和吡咯(
)和吡咯(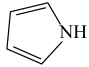 )形成配位化合物。噻吩难溶于水,吡咯能溶于水,原因为:
)形成配位化合物。噻吩难溶于水,吡咯能溶于水,原因为:_______ 。
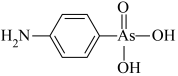
(4)含砷有机物“对氨基苯胂酸”的结构简式如图,As原子轨道杂化类型为_______ ,1mol对氨基苯胂酸含σ键数目为_______
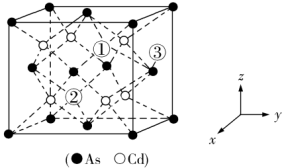
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构如图,As为面心立方堆积,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,如图“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为_______ 。晶胞参数为apm,阿伏加德罗常数的值为NA,砷化镉的摩尔质量为Mg·mol-1,则该晶胞的密度为_______ g·cm-3(列计算式即可)
(2)一水合甘氨酸锌[(H2NCH2COO)2Zn·H2O]是一种饲料添加剂,该化合物中所涉及的 第二周期元素的第一电离能由大到小的顺序是
(3)噻吩(
 )和吡咯(
)和吡咯( )形成配位化合物。噻吩难溶于水,吡咯能溶于水,原因为:
)形成配位化合物。噻吩难溶于水,吡咯能溶于水,原因为:(4)含砷有机物“对氨基苯胂酸”的结构简式如图,As原子轨道杂化类型为

(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构如图,As为面心立方堆积,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,如图“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
 ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____ ,基态S原子电子占据最高能级的电子云轮廓图为______ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为_____ 。
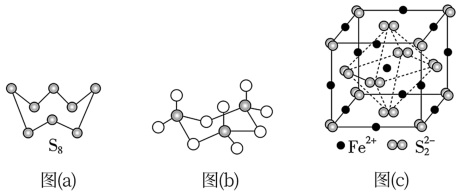
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____ 形,其中共价键的类型有_____ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为_____ 。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为____ g·cm−3;晶胞中Fe2+位于S22-所形成的正八面体的体心,该正八面体的边长为____ nm。1molFeS2晶体中含有阴阳离子总数为____
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 168.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】对题目(1)至(5)所提问题进行判断并提供合理解释。对题目(6)和(7)则按所给条件和要求解答。
(1)丙酮和六氟丙酮中哪个分子偶极矩更大_____ 。
(2)2,4-戊二酮的烯醇含量在水中还是在正己烷中高?将溶剂水换成二甲亚砜,2,4-戊酮的pKa是降低还是升高_____ 。
(3)(2E,4Z,6E)-辛-2,4,6-三烯在光照下关环后两个甲基是顺式的还是反式的?_____ 。
(4)乙酸乙酯、乙酰氯、N,N-二甲基乙酰胶中哪个化合物a-氢酸性最强?_____ 。
(5)吡啶和六氢吡啶中哪个分子偶极矩更大?_____ 。
(6)2-氟-5-三氟甲基吡啶与乙醇钠/乙醇的反应速率要比2,5-二氟吡啶快得多。为什么?_____ 。
(7)下表中列出酰肢化反应中常用的一些活化试剂。画出RCOOH被以下等量试剂活化后的中间体结构式(接下来与胺反应形成酰胺)_____ 。
(1)丙酮和六氟丙酮中哪个分子偶极矩更大
(2)2,4-戊二酮的烯醇含量在水中还是在正己烷中高?将溶剂水换成二甲亚砜,2,4-戊酮的pKa是降低还是升高
(3)(2E,4Z,6E)-辛-2,4,6-三烯在光照下关环后两个甲基是顺式的还是反式的?
(4)乙酸乙酯、乙酰氯、N,N-二甲基乙酰胶中哪个化合物a-氢酸性最强?
(5)吡啶和六氢吡啶中哪个分子偶极矩更大?
(6)2-氟-5-三氟甲基吡啶与乙醇钠/乙醇的反应速率要比2,5-二氟吡啶快得多。为什么?
(7)下表中列出酰肢化反应中常用的一些活化试剂。画出RCOOH被以下等量试剂活化后的中间体结构式(接下来与胺反应形成酰胺)
| 8-7-1PPh3,CBrCl3 | 8-7-2CyN=C=NCy | 8-7-3(CH3CO)2O |
8-7-4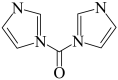 | 8-7-5 | 8-7-6 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态Fe原子价层电子的轨道表示式为_________ ,基态S原子电子占据最高能级的电子云轮廓图为________ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是____________ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为___________ 。
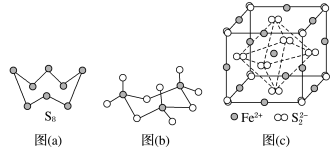
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为____________ 形,其中共价键的类型有________ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为__________ 。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M、阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为______ g·cm-3。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的轨道表示式为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M、阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为
您最近一年使用:0次
【推荐1】氧缺位体( )是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是(
)是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是( ,含
,含 、
、 等杂质)、为原料制备
等杂质)、为原料制备 的流程如下:
的流程如下:

已知:①酸浸后溶液中的金属离子有 、
、 、
、 和
和
②25℃时已知几种金属离子沉淀的pH如表所示:
请回答下列问题:
(1)Cu位于元素周期表第四周期,第___________ 族。
(2) “焙烧”时生成三种氧化物,其化学方程式为
“焙烧”时生成三种氧化物,其化学方程式为___________ 。
(3)加Cu“还原”的目是___________ 。
(4)滤渣2的主要成分为___________ 。
(5)已知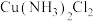 有两种同分异构体,则“沉铁”过程中生成的
有两种同分异构体,则“沉铁”过程中生成的 的空间构型是
的空间构型是___________ 。
(6)充分“煅烧”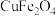 得到的氧缺位体(
得到的氧缺位体( )的质量为原质量的98%,则
)的质量为原质量的98%,则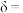
___________ 。
氧缺位体分解水制氢分两步:
第一步___________ (完成方程式);
第二步:
(7)四方晶系 晶胞结构如图所示,已知(
晶胞结构如图所示,已知( 晶体的密度是
晶体的密度是 ,则
,则
___________ (设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

 )是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是(
)是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是( ,含
,含 、
、 等杂质)、为原料制备
等杂质)、为原料制备 的流程如下:
的流程如下:
已知:①酸浸后溶液中的金属离子有
 、
、 、
、 和
和
②25℃时已知几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 1.9 | 3.4 | 6.4 | 7.0 |
| 完全沉淀的pH | 3.2 | 4.7 | 7.6 | 9.0 |
(1)Cu位于元素周期表第四周期,第
(2)
 “焙烧”时生成三种氧化物,其化学方程式为
“焙烧”时生成三种氧化物,其化学方程式为(3)加Cu“还原”的目是
(4)滤渣2的主要成分为
(5)已知
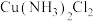 有两种同分异构体,则“沉铁”过程中生成的
有两种同分异构体,则“沉铁”过程中生成的 的空间构型是
的空间构型是(6)充分“煅烧”
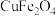 得到的氧缺位体(
得到的氧缺位体( )的质量为原质量的98%,则
)的质量为原质量的98%,则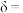
氧缺位体分解水制氢分两步:
第一步
第二步:

(7)四方晶系
 晶胞结构如图所示,已知(
晶胞结构如图所示,已知( 晶体的密度是
晶体的密度是 ,则
,则
 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ.尿素[CO(NH2)2]是人工合成的第一种有机物,可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3。
(1)[Fe(H2NCONH2)6](NO3)3中所含元素的电负性由大到小的顺序是______________ 。
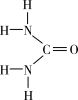
(2)尿素中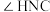
______________ 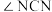 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是______________ 。
(3)[Fe(H2NCONH2)6](NO3)3中不存在 的化学键____________ (填序号)。
A.离子键 B.金属键 C.配位键 D. 键 E.
键 E. 键
键
Ⅱ. 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体,边长为
晶胞形状为如图立方体,边长为 ,
, 原子占据顶点和面心,
原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
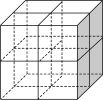
(4) 原子的价电子排布式为
原子的价电子排布式为______________ 。
(5) 位于
位于 原子形成的
原子形成的______________ (填“八面体空隙”或“四面体空隙”)。
(6)该晶体的密度为___________  (用含a、
(用含a、 代数式表示)。
代数式表示)。

(1)[Fe(H2NCONH2)6](NO3)3中所含元素的电负性由大到小的顺序是
(2)尿素中
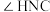
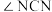 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是(3)[Fe(H2NCONH2)6](NO3)3中
A.离子键 B.金属键 C.配位键 D.
 键 E.
键 E. 键
键Ⅱ.
 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体,边长为
晶胞形状为如图立方体,边长为 ,
, 原子占据顶点和面心,
原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
(4)
 原子的价电子排布式为
原子的价电子排布式为(5)
 位于
位于 原子形成的
原子形成的(6)该晶体的密度为
 (用含a、
(用含a、 代数式表示)。
代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起广泛关注。一种含Se的新型AIE分子IV的合成路线如图:
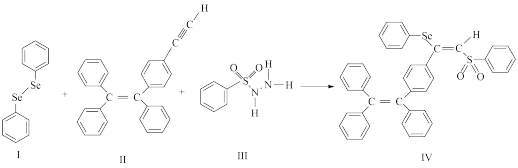
(1)Se与S同族,基态硒原子的价电子排布式为____ 。
(2)H2Se的沸点低于H2O,其原因是____ 。
(3)关于I~III三种反应物,下列说法不正确的有 (填标号)。
(4)IV中具有孤对电子的原子有____ 。
(5)硒的两种含氧酸的酸性强弱为H2SeO4____ H2SeO3(选填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒。SeO 的立体构型为
的立体构型为____ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
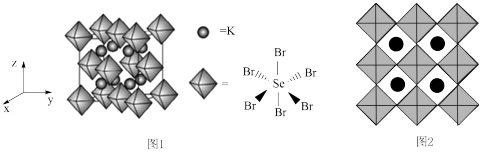
①X的化学式为____ 。
②设X的化学式的相对分子质量为M,晶体密度为ρg/cm3,则X中相邻K原子之间的最短距离为____ nm(列出计算式,设NA为阿伏加德罗常数的值)。

(1)Se与S同族,基态硒原子的价电子排布式为
(2)H2Se的沸点低于H2O,其原因是
(3)关于I~III三种反应物,下列说法不正确的有 (填标号)。
| A.I中仅有σ键 | B.I中的Se-Se键为非极性共价键 |
| C.II中碳原子的杂化轨道类型只有sp2 | D.III含有的元素中,O的电负性最大 |
(5)硒的两种含氧酸的酸性强弱为H2SeO4
 的立体构型为
的立体构型为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的化学式的相对分子质量为M,晶体密度为ρg/cm3,则X中相邻K原子之间的最短距离为
您最近一年使用:0次



