铁、钴、镍等金属及其化合物在科学研究和工业生产中应用非常广泛。回答下列问题:
(1)基态铁原子的核外电子排布式为___________ 。
(2)K3[Fe(CN)6 ]溶液可以检验Fe2+。K3[Fe(CN)6]中含有的σ键与π键的数目之比___________ , 与CN-互为等电子体的分子有___________ (举一例,填化学式)。
(3)酞菁钴的结构简式如图所示,其中三种非金属元素的电负性由大到小的顺序为___________ 。

(4)NiSO4是制备磁性材料和催化剂的重要中间体, 的空间构型为
的空间构型为___________ ,硫原子的杂化方式为___________ 。
(5)某氮化铁的晶胞结构如图所示:
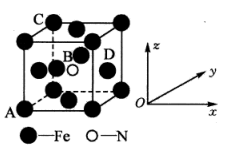
①原子坐标参数表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数A(0,0,0);B为( ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为___________ 。
②若该晶体的密度是ρg·cm-3 ,则晶胞中两个最近的Fe的核间距为___________ cm(用含ρ的代数式表示,NA表示阿伏加德罗常数的值)。
(1)基态铁原子的核外电子排布式为
(2)K3[Fe(CN)6 ]溶液可以检验Fe2+。K3[Fe(CN)6]中含有的σ键与π键的数目之比
(3)酞菁钴的结构简式如图所示,其中三种非金属元素的电负性由大到小的顺序为

(4)NiSO4是制备磁性材料和催化剂的重要中间体,
 的空间构型为
的空间构型为(5)某氮化铁的晶胞结构如图所示:

①原子坐标参数表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数A(0,0,0);B为(
 ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为②若该晶体的密度是ρg·cm-3 ,则晶胞中两个最近的Fe的核间距为
更新时间:2022-06-10 10:51:14
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】新型铜锌锡硫化合物(CuxZnySnzSn)薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
(1)Zn位于元素周期表的_______ 区。
(2)Si、P、S第一电离能由大到小的顺序是_______ 。其中电负性最大的元素是_______ 。
(3) 和
和 键角较小的是
键角较小的是_______ ,原因是_______ 。
(4)锌黄锡矿(K型)是制备薄膜太阳能电池的重要原料,其晶胞结构如图所示(晶胞参数 90°)。该晶体的化学式为
90°)。该晶体的化学式为_______ ,密度
_______  (用含有NA的代数式表示)。
(用含有NA的代数式表示)。

(1)Zn位于元素周期表的
(2)Si、P、S第一电离能由大到小的顺序是
(3)
 和
和 键角较小的是
键角较小的是(4)锌黄锡矿(K型)是制备薄膜太阳能电池的重要原料,其晶胞结构如图所示(晶胞参数
 90°)。该晶体的化学式为
90°)。该晶体的化学式为
 (用含有NA的代数式表示)。
(用含有NA的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】以银锰精矿(主要含 、MnS、
、MnS、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下:
)为原料联合提取银和锰的一种流程示意图如下:
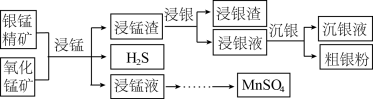
已知:Ⅰ.酸性条件下, 的氧化性强于
的氧化性强于 ;
;
Ⅱ.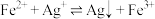 。
。
(1)“浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出,矿石中的银以
,有利于后续银的浸出,矿石中的银以 的形式残留于浸锰渣中。
的形式残留于浸锰渣中。
①写出Mn元素基态原子的价层电子排布式:________ 。
②“浸锰”过程中,发生反应: ,则可推断:
,则可推断: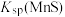
________ (填“>”或“<”)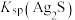 。
。
③在 溶液中,银锰精矿中的
溶液中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有________ 。
(2)“浸银”时,使用过量 、HCl和
、HCl和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出。
形式浸出。
①将“浸银”反应的离子方程式补充完整:_____ 。
________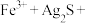 ________
________ ________
________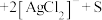
②结合平衡移动原理,解释浸出剂中 、
、 的作用:
的作用:________ 。
(3)“沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有 和
和________ 。
②一定温度下,Ag的沉淀率随反应时间的变化如图所示。解释t分钟后Ag的沉淀率逐渐减小的原因:________ 。
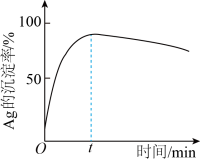
(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析这种联合提取银和锰方法的优势:________ 。
 、MnS、
、MnS、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下:
)为原料联合提取银和锰的一种流程示意图如下:
已知:Ⅰ.酸性条件下,
 的氧化性强于
的氧化性强于 ;
;Ⅱ.
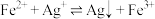 。
。(1)“浸锰”过程是在
 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出,矿石中的银以
,有利于后续银的浸出,矿石中的银以 的形式残留于浸锰渣中。
的形式残留于浸锰渣中。①写出Mn元素基态原子的价层电子排布式:
②“浸锰”过程中,发生反应:
 ,则可推断:
,则可推断: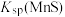
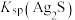 。
。③在
 溶液中,银锰精矿中的
溶液中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有(2)“浸银”时,使用过量
 、HCl和
、HCl和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出。
形式浸出。①将“浸银”反应的离子方程式补充完整:
________
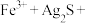 ________
________ ________
________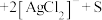
②结合平衡移动原理,解释浸出剂中
 、
、 的作用:
的作用:(3)“沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有
 和
和②一定温度下,Ag的沉淀率随反应时间的变化如图所示。解释t分钟后Ag的沉淀率逐渐减小的原因:

(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析这种联合提取银和锰方法的优势:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】硫、锌及其化合物用途非常广泛。回答下列问题:
(1)基态锌原子核外能量不同的电子有___________ 种;锌的第二电离能I2(Zn)小于铜的第二电离能I2(Cu),其原因是___________ 。
(2)已知KH2PO2是次磷酸的正盐,H3PO2的结构式为___________ ,其中P 采取___________ 杂化方式。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为___________ 。
(4)含氧酸的通式可写为(HO)mROn,根据化学学科的规律下列几种酸中酸性与H3PO4相近的有___________。
(5)磷酸通过分子间脱水缩合形成多磷酸,如:

如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为___________ 。
(6)砷化镉可以看作是石墨烯的3D版,其晶胞结构如图,As 为面心立方堆积,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,如图“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ), 则③号位原子坐标参数为
), 则③号位原子坐标参数为___________ 。晶胞参数为apm,阿伏加德罗常数的值为NA,砷化镉的摩尔质量为Mg·mol-l,则该晶胞的密度为___________ g· cm-3(列计算式即可)

(1)基态锌原子核外能量不同的电子有
(2)已知KH2PO2是次磷酸的正盐,H3PO2的结构式为
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为(4)含氧酸的通式可写为(HO)mROn,根据化学学科的规律下列几种酸中酸性与H3PO4相近的有___________。
| A.HClO | B.HClO3 | C.H2SO3 | D.HNO2 |

如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为
(6)砷化镉可以看作是石墨烯的3D版,其晶胞结构如图,As 为面心立方堆积,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,如图“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
 ,
, ,
, ), 则③号位原子坐标参数为
), 则③号位原子坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】前四周期很多元素在工业及生活方面有很多重要应用。回答下列问题:
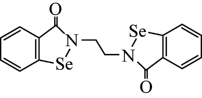
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构简式如图:
①基态 原子的核外电子有
原子的核外电子有____ 种空间运动状态。
②该新药分子中有_____ 种不同化学环境的H原子。
③比较键角大小:气态SeO3分子____ SeO 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是_____ 。
(2)“钛”被称为21世纪金属,基态钛原子价电子的排布图为____ 。
(3)CrO5中有4个-1价的O。CrO5中π键与σ键个数比为____ 。
(4)[Co(NH3)4Cl2]+呈八面体结构,其中Co3+采取的杂化类型为____ (填编号①dsp2、②sp3d、③sp3d2)。能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是____ (填标号)。
a.浓氨水 b.NaOH溶液 c.稀H2SO4 d.AgNO3溶液
(5)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是____ (填元素符号),写出与CN-互为等电子体的一种分子的化学式为____ 。
(6)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为( ,
, ,0)。此晶胞中与n点最远的S的坐标为
,0)。此晶胞中与n点最远的S的坐标为____ 。若Zn与S弹性相切,其半径分别为apm和bpm,则ZnS的密度为____ g•cm-3(用含a、b、NA的式子表示)。

(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构简式如图:

①基态
 原子的核外电子有
原子的核外电子有②该新药分子中有
③比较键角大小:气态SeO3分子
 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)“钛”被称为21世纪金属,基态钛原子价电子的排布图为
(3)CrO5中有4个-1价的O。CrO5中π键与σ键个数比为
(4)[Co(NH3)4Cl2]+呈八面体结构,其中Co3+采取的杂化类型为
a.浓氨水 b.NaOH溶液 c.稀H2SO4 d.AgNO3溶液
(5)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是
(6)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为(
 ,
, ,0)。此晶胞中与n点最远的S的坐标为
,0)。此晶胞中与n点最远的S的坐标为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】学习化学一定要领悟好问题情景。
(1)①书写以下各微粒的电子式。
—OH___________ ,HBrO___________ ,CS2___________ ,NH4H___________ ;
②用电子式表示Na和S形成Na2S的过程___________ 。
(2)氮元素的化合物种类繁多,性质也各不相同。请回答下列问题:
已知:①N2(g)+O2(g)=2NO(g)ΔH=+180.5kJ·mol-1
②2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol-1
③N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ·mol-1
则反应:④4NH3(g)+5O2(g)=4NO(g)+6H2O(g)的ΔH=___________ kJ·mol-1。
(3)电负性与原子所处的具体的化学环境紧密相关。有机化合物CH3I和CF3I发生水解时的主要反应分别是:CH3I+H2O→CH3OH+HI和CF₃I+H₂O→CF3H+HIO。从电负性的角度分析,为什么CF3I水解的产物不是HI的原因___________ 。
(4)工业上用Na2SO3吸收尾气中SO2使之转化为NaHSO3,再以SO2为原料设计原电池,然后电解(惰性电极)NaHSO3制取H2SO4,装置如下:
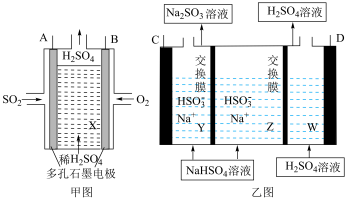
①甲图中A电极上的反应式为___________ 。
②甲图中B与乙图___________ (填“C”或“D”)极相连,进行电解时乙图Z中Na+向___________ (填“Y”或“W”)中移动。
③该电解池阴极的电极反应式为___________ ;
(5)Ni可活化C2H6放出CH4,其反应历程如下图所示:

下列关于活化历程的说法错误的是
(1)①书写以下各微粒的电子式。
—OH
②用电子式表示Na和S形成Na2S的过程
(2)氮元素的化合物种类繁多,性质也各不相同。请回答下列问题:
已知:①N2(g)+O2(g)=2NO(g)ΔH=+180.5kJ·mol-1
②2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol-1
③N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ·mol-1
则反应:④4NH3(g)+5O2(g)=4NO(g)+6H2O(g)的ΔH=
(3)电负性与原子所处的具体的化学环境紧密相关。有机化合物CH3I和CF3I发生水解时的主要反应分别是:CH3I+H2O→CH3OH+HI和CF₃I+H₂O→CF3H+HIO。从电负性的角度分析,为什么CF3I水解的产物不是HI的原因
(4)工业上用Na2SO3吸收尾气中SO2使之转化为NaHSO3,再以SO2为原料设计原电池,然后电解(惰性电极)NaHSO3制取H2SO4,装置如下:

①甲图中A电极上的反应式为
②甲图中B与乙图
③该电解池阴极的电极反应式为
(5)Ni可活化C2H6放出CH4,其反应历程如下图所示:

下列关于活化历程的说法错误的是
| A.活化能最大的步骤:中间体2→中间体3 |
| B.只涉及极性键的断裂和生成 |
| C.在此反应过程中Ni的成键数目发生变化 |
D.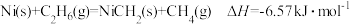 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍。回答下列问题:
(1)B2A4分子中σ键和π键个数比为_______ 。
(2)A、B、C、D四种元素的电负性从大到小的顺序为_______ (用元素符号表示)。
(3)元素B的一种氧化物与元素C的一种氧化物互为等电子体,元素C的这种氧化物的分子式是_______ 。
(4)元素E能形成多种配合物,如:E(CO)5等。
①基态E原子的价电子排布图为_______ 。
②E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断E(CO)5晶体属于_______ (填晶体类型),该晶体中E的化合价为_______ 。
(5)E和C形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为_______ 。若两个最近的E原子间的距离为acm,则该晶体的密度是_______ g·mL-1。

(1)B2A4分子中σ键和π键个数比为
(2)A、B、C、D四种元素的电负性从大到小的顺序为
(3)元素B的一种氧化物与元素C的一种氧化物互为等电子体,元素C的这种氧化物的分子式是
(4)元素E能形成多种配合物,如:E(CO)5等。
①基态E原子的价电子排布图为
②E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断E(CO)5晶体属于
(5)E和C形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】氮族元素N、P、As等元素在农药、化肥等领域有广泛应用。回答下列问题:
(1)基态砷原子中,电子占据的最高能层符号为____ ,砷原子在该能层上占据能量最高轨道电子的电子云在空间有___ 个伸展方向。
(2)基态As原子的价电子的排布式为____ 。
(3)N、P、As均是VA的元素,其简单氢化物的沸点由高到低的顺序为____ ,其理由是____ 。
(4)磷元素的常见含氧酸根为PO ,其空间构型为
,其空间构型为___ ,其中P的杂化方式为___ 。NO 和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为
和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为___ (用元素符号表示)。1mol该配离子中含有的σ键数目为___ NA。
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的晶胞结构如图所示。

①A、B点的原子坐标如图所示,则C点的原子坐标为___ 。
②磷化铝的晶胞参数a=546.35pm,其密度为___ g•cm-3(列出计算式即可,NA表示阿伏加德罗常数的值)。
(1)基态砷原子中,电子占据的最高能层符号为
(2)基态As原子的价电子的排布式为
(3)N、P、As均是VA的元素,其简单氢化物的沸点由高到低的顺序为
(4)磷元素的常见含氧酸根为PO
 ,其空间构型为
,其空间构型为 和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为
和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的晶胞结构如图所示。

①A、B点的原子坐标如图所示,则C点的原子坐标为
②磷化铝的晶胞参数a=546.35pm,其密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛。
(1)基态C原子的空间运动状态有______ 个,其未成对电子对应的电子云形状为_______ 。
(2)金刚石和石墨是碳元素的两种常见单质,下列关于这两种单质的叙述中正确的是_______ 。
A.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化。
B.两种晶体中碳碳键的键长:金刚石<石墨
C.晶体中共价键的键角:金刚石>石墨
D.晶体的熔点:金刚石<石墨
E.金刚石中只存在共价键,而石墨晶体中除共价键外还存在离子键和范德华力
(3)CO2是碳的重要化合物之一,它的某一种等电子体(A离子),实验室常用来检验Fe3+离子,写出A离子的结构式_______ ;A离子中心原子的价层电子对数是_______ 对;它的另一种等电子体CS2是一种_______ 溶剂(填“极性”或“非极性”),请说出CS2的沸点高于CO2的原因是_______ 。
(4)碳酸铯与盐酸反应可得到CsCl,CsCl晶胞是中学常见晶胞。
①该晶胞类型为_______ 。
②已知该晶体中CsCl的键长为apm,阿伏加德罗常数为NA,CsCl的摩尔质量为Mg/mol,则该晶体的密度为_______ g/cm3(用含字母a的关系式表示)
(5)孔雀石[Cu2(OH)2CO3]是自然界中一种含碳元素的重要矿物质,加热分解得CuO,CuO溶于稀硫酸得蓝色溶液,再滴加乙二胺(NH2CH2CH2NH2)溶液,溶液变为紫色。
查阅资料:①Cu2+易形成配位数为4的配合离子。②H2O和乙二胺都能与过渡金属离子形成配合离子。
孔雀石[Cu2(OH)2CO3]中各非金属元素第一电离能从小到大排序为_______ 。写出Cu2+的价层电子排布式_______ 。紫色溶液中含有铜元素形成的配离子的化学式_______ ,其中配位原子在空间形成形状为_______ 。
(1)基态C原子的空间运动状态有
(2)金刚石和石墨是碳元素的两种常见单质,下列关于这两种单质的叙述中正确的是
A.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化。
B.两种晶体中碳碳键的键长:金刚石<石墨
C.晶体中共价键的键角:金刚石>石墨
D.晶体的熔点:金刚石<石墨
E.金刚石中只存在共价键,而石墨晶体中除共价键外还存在离子键和范德华力
(3)CO2是碳的重要化合物之一,它的某一种等电子体(A离子),实验室常用来检验Fe3+离子,写出A离子的结构式
(4)碳酸铯与盐酸反应可得到CsCl,CsCl晶胞是中学常见晶胞。
①该晶胞类型为
②已知该晶体中CsCl的键长为apm,阿伏加德罗常数为NA,CsCl的摩尔质量为Mg/mol,则该晶体的密度为
(5)孔雀石[Cu2(OH)2CO3]是自然界中一种含碳元素的重要矿物质,加热分解得CuO,CuO溶于稀硫酸得蓝色溶液,再滴加乙二胺(NH2CH2CH2NH2)溶液,溶液变为紫色。
查阅资料:①Cu2+易形成配位数为4的配合离子。②H2O和乙二胺都能与过渡金属离子形成配合离子。
孔雀石[Cu2(OH)2CO3]中各非金属元素第一电离能从小到大排序为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】【化学一选修3:物质结构与性质】
卤族元素单质与许多物质反应形成多种化合物。请利用所学物质结构与性质的相关知识回答:
(1)写出基态碘原子的价电子排布式___________ ;
(2)卤族元素的含氧酸中酸性最强的是____ (写化学式),该酸根离子的立体构型为_________ 。
(3)比较下列锗的卤化物的熔点和沸点,分析其变化规律及原因_________ 。
(4)已知高碘酸有两种形式,化学式分别为H5IO6( )和HIO4,前者为五元酸,后者为一元酸,二者酸性强弱顺序为H5IO6
)和HIO4,前者为五元酸,后者为一元酸,二者酸性强弱顺序为H5IO6_____ HIO4(填“>”、“<”或“=”)。H5IO6中σ键与π键的个数比为________ 。
(5)已知氯元素与第四周期最外层只有1个电子、次外层的所有原子轨道均充满电子的元素M形成的一种化合物的立方晶胞如图所示。
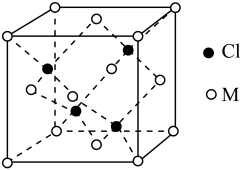
①该化合物的化学式为_______ ,已知晶胞参数a=0.542 nm,此晶体的密度为_____ g/cm3。(写出计算式,不要求计算结果,阿伏伽德罗常数为NA)
卤族元素单质与许多物质反应形成多种化合物。请利用所学物质结构与性质的相关知识回答:
(1)写出基态碘原子的价电子排布式
(2)卤族元素的含氧酸中酸性最强的是
(3)比较下列锗的卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
 )和HIO4,前者为五元酸,后者为一元酸,二者酸性强弱顺序为H5IO6
)和HIO4,前者为五元酸,后者为一元酸,二者酸性强弱顺序为H5IO6(5)已知氯元素与第四周期最外层只有1个电子、次外层的所有原子轨道均充满电子的元素M形成的一种化合物的立方晶胞如图所示。

①该化合物的化学式为
您最近一年使用:0次
【推荐1】碳是形成单质和化合物最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)C原子的价电子轨道表达式为______________________ 。
(2)碳元素是组成有机物必不可少的元素。1828年,化学家维勒首次用加热的方法将无机物氰酸铵[NH4(OCN)]转化为有机物尿素,开启了人造有机物的大门。氰酸铵中阳离子的立体构型是___________ 。有机物M(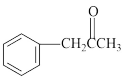 )在一定条件下生成N(
)在一定条件下生成N(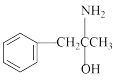 )
)
①沸点:M___________ N(填“大于”或“小于”)。
②M中碳原子的杂化类型为___________ ,不同杂化类型的碳原子数之比为___________ 。
(3)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图所示。该配离子的配位数是___________ ,配体中碳原子的杂化方式有_________ 。
(4)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图所示,图中用实线标出了石墨的一个六方晶胞。

①石墨中C原子上未参与杂化的所有p轨道相互平行且重叠,使p轨道中的电子可在整个碳原子平面中运动而导电。六方氮化硼(BN)与石墨晶体结构类似,硼原子和氮原子交替相连,而六方BN却无法导电,其原因是___________ 。
②晶胞有两个基本要素:石墨一种晶胞结构和部分晶胞参数如图。

a.原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为A(0,0,0)、B(0,1, ),则C原子的坐标参数为
),则C原子的坐标参数为___________ 。
b. 晶胞参数用以描述晶胞的大小和形状。已知石墨晶胞底边长为acm,层间距为 d cm,阿伏伽德罗常数的值为NA,则石墨的密度为___________ g·cm-3(写出表达式即可)
(1)C原子的价电子轨道表达式为
(2)碳元素是组成有机物必不可少的元素。1828年,化学家维勒首次用加热的方法将无机物氰酸铵[NH4(OCN)]转化为有机物尿素,开启了人造有机物的大门。氰酸铵中阳离子的立体构型是
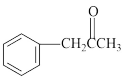 )在一定条件下生成N(
)在一定条件下生成N( )
)①沸点:M
②M中碳原子的杂化类型为
(3)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图所示。该配离子的配位数是

(4)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图所示,图中用实线标出了石墨的一个六方晶胞。

①石墨中C原子上未参与杂化的所有p轨道相互平行且重叠,使p轨道中的电子可在整个碳原子平面中运动而导电。六方氮化硼(BN)与石墨晶体结构类似,硼原子和氮原子交替相连,而六方BN却无法导电,其原因是
②晶胞有两个基本要素:石墨一种晶胞结构和部分晶胞参数如图。

a.原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为A(0,0,0)、B(0,1,
 ),则C原子的坐标参数为
),则C原子的坐标参数为b. 晶胞参数用以描述晶胞的大小和形状。已知石墨晶胞底边长为acm,层间距为 d cm,阿伏伽德罗常数的值为NA,则石墨的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】锌是人体必需的微量元素之一,起着极其重要的作用,回答下列问题:
(1)请写出Zn2+的核外电子排布式_______ 。
(2)ZnCl2熔点为275 ℃,而CaCl2的熔点为782 ℃,请分析熔点不同的原因:_______ 。
(3)Zn2+能与多种微粒形成配合物,如Zn2+与CNO−可形成[Zn(CNO)4]2−,[Zn(CNO)4]2−中配位原子为_______ ,[Zn(CNO)4]2−的组成中非金属元素的电负性大小顺序为_______ ;Zn2+与CN−可形成[Zn(CN)4]2−,[Zn(CN)4]2−中σ键、π键和配位键的个数比为_______ ;配合物Zn(NH3)4CO3中阴离子的空间构型为_______ ,N原子的杂化方式为_______ 。
(4)Zn与S所形成化合物的晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图:_______ 。
②晶胞中最近的两个S原子之间的距离为_______ pm。
③设阿伏加 德罗常数的值为NA,则该晶胞的密度是_______ g·cm−3(列出计算表达式)。
(1)请写出Zn2+的核外电子排布式
(2)ZnCl2熔点为275 ℃,而CaCl2的熔点为782 ℃,请分析熔点不同的原因:
(3)Zn2+能与多种微粒形成配合物,如Zn2+与CNO−可形成[Zn(CNO)4]2−,[Zn(CNO)4]2−中配位原子为
(4)Zn与S所形成化合物的晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图:

②晶胞中最近的两个S原子之间的距离为
③设阿伏加 德罗常数的值为NA,则该晶胞的密度是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】翡翠是一类名贵的装饰品,其主要成分为硅酸铝钠(NaAlSi2O6),常含微量Cr、Ni、Mn等元素。回答下列问题:
(1)基态硅原子的电子排布式为__ ;基态铬原子的价电子排布图不能写成 形式,其原因是违背了
形式,其原因是违背了___ 。
(2)NaAlSi2O6中四种元素第一电离能由大到小的顺序为___ (填元素符号),灼烧硅酸铝钠时,当钠元素的价电子由__ (填“激发态”或“基态”)跃迁到另一状态时产生黄色火焰。
(3)工业上冶炼金属铝的方程式为__ 。硅与碳类似,能与氢元素形成SiH4、Si2H4、Si3H8,此三种分子中硅原子为sp3杂化的有___ ;分子空间构型属于正四面体的是__ 。
(4)已知氧化钠、氧化铝的熔点分别为1132℃、2054℃,从结构的角度解释导致这种差异的主要原因:___ 。
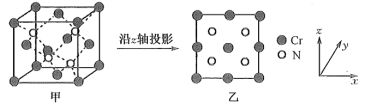
(5)某N、Cr元素组成的化合物具有高的硬度和良好的耐磨性,是一种很受重视的耐磨涂层,其晶胞结构如图甲,图乙为晶胞沿z轴投影图,该化合物的化学式为__ 。知该晶体密度为ρg·cm-3。晶体中Cr原子和N的最近核间距为___ pm(NA表示阿伏加德罗常数值)。
(1)基态硅原子的电子排布式为
 形式,其原因是违背了
形式,其原因是违背了(2)NaAlSi2O6中四种元素第一电离能由大到小的顺序为
(3)工业上冶炼金属铝的方程式为
(4)已知氧化钠、氧化铝的熔点分别为1132℃、2054℃,从结构的角度解释导致这种差异的主要原因:
(5)某N、Cr元素组成的化合物具有高的硬度和良好的耐磨性,是一种很受重视的耐磨涂层,其晶胞结构如图甲,图乙为晶胞沿z轴投影图,该化合物的化学式为

您最近一年使用:0次



