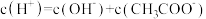常温下,用0.1 mol·L-1的CH3COOH溶液滴定20 mL 0.1 mol·L-1的NaOH溶液,当滴加V mL CH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确的是( )
A.Ka= | B.V= | C.Ka= | D.Ka= |
15-16高三上·湖北·期中 查看更多[13]
2016届湖北省华中师大第一附属中学高三上期中理综化学试卷2016届山东省日照一中高三上期末理综化学试卷2016-2017学年四川省成都市第七中学高二下学期半期考试化学试卷河南省南阳市2017-2018学年高二上学期期末考试化学试题江西省赣州市寻乌中学2019-2020学年高二上学期第二次段考化学试题安徽省舒城中学2020-2021学年高二上学期第三次月考化学试题湖南省长沙市长郡中学2022-2023学年高二上学期期末考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第46练 弱电解质的电离平衡辽宁省沈阳市第一二〇中学2023-2024学年高二上学期第二次质量监测化学试题辽宁省沈阳市第一二〇中学2023-2024学年高二上学期第二次质量检测化学试题山西省实验中学2023-2024学年高二上学期期中考试化学试题湖南省衡阳市八中2023-2024学年高二上学期第三次月考化学试题江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
更新时间:2019-12-28 16:04:47
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】常温时,草酸的电离常数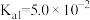 ,
,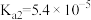 ,CaC2O4的
,CaC2O4的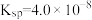 。下列有关说法正确的是
。下列有关说法正确的是
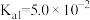 ,
,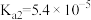 ,CaC2O4的
,CaC2O4的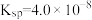 。下列有关说法正确的是
。下列有关说法正确的是| A.草酸钙是弱电解质 |
B.NaHC2O4在水溶液中的电离方程式: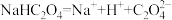 |
C.常温时,0.01mol/L草酸溶液中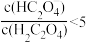 |
D.CaC2O4浊液中存在平衡: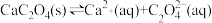 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法错误的是( )
| A.强电解质在溶液中完全电离 |
| B.在溶液中导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
| C.同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同 |
D. 的电离方程式为 的电离方程式为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】常温下,用0.1000mol·L-1 NaOH溶液滴定20.00mL 0.1000 mol·L-1某酸(HA)溶液,溶液中HA、A-的物质的量分数δ(X)随pH的变化如图所示。[已知δ(X)=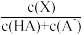 ]下列说法正确的是
]下列说法正确的是

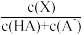 ]下列说法正确的是
]下列说法正确的是
| A.Ka(HA)的数量级为10-5 |
| B.溶液中由水电离出的c(H+):a点>b点 |
| C.当pH=4.7时,c(A-)+c(OH-)=c(HA)+c(H+) |
| D.当pH=7时,消耗NaOH溶液的体积为20.00mL |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下, CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20mL浓度均为0.1mol/L的NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液体积(V)的关系如图所示。下列说法不正确的是( )


| A.a=20,b=40,且溶液呈中性时处于A、B两点之间 |
B.B点溶液中: c(CH3COO-)>c(Na+)>c( ) ) |
| C.C点溶液的pH≈5 |
| D.A、B、C三点中,B点溶液中水的电离程度最大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】类比和推理是重要的学习方法。下列类比或推理合理的是
| 选项 | 已知 | 方法 | 结论 |
| A | 常温下,Kb(NH3·H2O)=1.8×10-5、Ka(HF)=6.3×10-4 | 推理 | NH4F溶液显酸性 |
| B | Ksp:Ag2CrO4<AgCl | 推理 | 溶解度:Ag2CrO4<AgCl |
| C | Fe+CuSO4(aq)=FeSO4+Cu | 类比 | 2Na+CuSO4(aq)=Na2SO4+Cu |
| D | 工业电解熔融氯化镁制镁 | 类比 | 工业电解熔融氯化铝制铝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

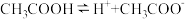 ,下列各项不正确的是
,下列各项不正确的是