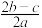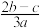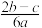已知0.1mol·L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是( )
| A.在Na2A、NaHA两溶液中,离子种类相同 |
| B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等 |
| C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)+c(H2A) |
| D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-) |
更新时间:2020-01-15 15:04:04
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
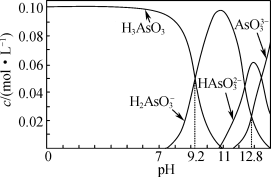
【推荐1】亚砷酸(H3AsO3)可用于白血病的治疗。室温下,配制一组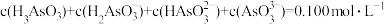 的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
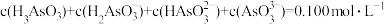 的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
| A.H3AsO3的电离常数Ka1的数量级为10-9 |
B.c(Na+)=0.100 mol·L-1的溶液中: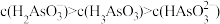 |
C.通常情况下,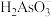 电离程度大于水解程度 电离程度大于水解程度 |
D.pH=12.8的溶液中: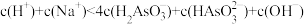 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关说法正确的是
| A.AgCl难溶于水,AgCl是弱电解质 |
B. 是弱电解质, 是弱电解质, 溶液的导电性比NaOH溶液弱 溶液的导电性比NaOH溶液弱 |
C. 是弱酸,其电离方程式为: 是弱酸,其电离方程式为: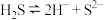 |
D.在相同温度下,pH相等的盐酸、 溶液, 溶液, |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.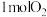 含有的原子数为 含有的原子数为 | B.标准状况下,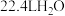 中含有的水分子数为 中含有的水分子数为 |
C. 中含有的电子数为 中含有的电子数为 | D. 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】反应 放热且产生气体,可用于冬天石油开采。设
放热且产生气体,可用于冬天石油开采。设 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是
 放热且产生气体,可用于冬天石油开采。设
放热且产生气体,可用于冬天石油开采。设 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是A.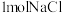 中含 中含 分子数为 分子数为 |
B.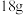 水中所含电子数目为 水中所含电子数目为 |
C. 的 的 溶液中所含 溶液中所含 的数目为 的数目为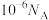 |
D. 溶液中所含氢原子的数目为 溶液中所含氢原子的数目为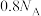 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知NaHSO4在水中电离方程式为:NaHSO4=Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
| A.该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好是中性 |
| B.水电离出来的c(H+)=1×10-10mol·L-1 |
| C.c(H+)=c(OH-)+c(SO42-) |
| D.该温度高于25℃ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】设 为阿伏加德罗常数,下列说法不正确的是
为阿伏加德罗常数,下列说法不正确的是
 为阿伏加德罗常数,下列说法不正确的是
为阿伏加德罗常数,下列说法不正确的是A.0.05 液态 液态 中含有0.05 中含有0.05 个阳离子 个阳离子 |
B.0.1  溶液中含有 溶液中含有 微粒数小于0.1 微粒数小于0.1 |
C.0.5  溶于水,溶液中的 溶于水,溶液中的 、 、 、 、 、 、 微粒总数和为0.5 微粒总数和为0.5 |
D.将1  溶于稀氨水中使溶液呈中性,溶液中 溶于稀氨水中使溶液呈中性,溶液中 数目为 数目为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,浓度均为0.1mol·L-1的NaX和NaY盐溶液的pH分别为9和11,下列判断不正确 的是
| A.NaX溶液中:c(Na+)> c(X-) > c(OH-)>c(H+) |
| B.电离常数:Ka(HX) > Ka(HY) |
| C.X-结合H+的能力大于Y-结合H+的能力 |
| D.HX与NaY能发生反应:HX + Y-= HY + X- |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】相同温度相同物质的量浓度的六种溶液:①NaHCO3 ②CH3COONa ③NaOH④Ba(OH)2 ⑤NaHSO4 ⑥H3PO4按pH值由大到小的顺序是
| A.⑥⑤②①④③ | B.⑥⑤①②③④ |
| C.④③②①⑤⑥ | D.④③①②⑥⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】CO2溶于水生成碳酸。已知下列数据:
现有常温下1mol/L的(NH4)2CO3溶液,下列说法正确的是
| 弱电解质 | H2CO3 | NH3·H2O |
| 电离平衡常数(25℃) | Ka1=4.5×10-7 Ka2=4.7×10-11 | Kb=1.8×10-5 |
| A.由数据可判断该溶液呈酸性 |
B.c( )>c( )>c( )>c( )>c( )>c(NH3·H2O) )>c(NH3·H2O) |
C.c( )+c(NH3·H2O)=2c( )+c(NH3·H2O)=2c( )+2c( )+2c( )+2c(H2CO3) )+2c(H2CO3) |
D.c( )+c(H+)=( )+c(H+)=( )+c(OH-)+c( )+c(OH-)+c( ) ) |
您最近一年使用:0次

 )俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。乙二酸与氧化剂作用易被氧化成二氧化碳和水,如
)俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。乙二酸与氧化剂作用易被氧化成二氧化碳和水,如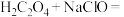
 。下列说法正确的是
。下列说法正确的是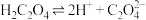
 原子的电子排布式写为
原子的电子排布式写为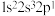 ,则违背了洪特规则
,则违背了洪特规则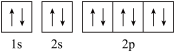
 、
、 、
、 、
、
 、
、 、
、 、
、
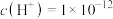 的溶液中:
的溶液中: 、
、
 、
、