向少量Mg(OH)2悬浊液中加入适量的饱和NH4Cl溶液,结果固体完全溶解。对此甲、乙两同学各自作了自己的解释:
甲:Mg(OH)2(s) Mg2++2OH-①,NH4++H2O
Mg2++2OH-①,NH4++H2O NH3·H2O+H+②,H++OH-=H2O③,由于③反应的发生,使平衡①右移,Mg(OH)2溶解。
NH3·H2O+H+②,H++OH-=H2O③,由于③反应的发生,使平衡①右移,Mg(OH)2溶解。
乙:Mg(OH)2(s) Mg2++2OH-①,NH4++ OH-
Mg2++2OH-①,NH4++ OH- NH3·H2O②,由于②反应的发生,使平衡①右移,沉淀溶解。
NH3·H2O②,由于②反应的发生,使平衡①右移,沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是用下面的一种试剂重做了该实验,证明甲、乙的解释只有一种正确。他用的试剂是________ 。
A.NH4NO3B.CH3COONH4C.(NH4)2SO4D.氨水
(2)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理____ (填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊溶解的离子方程式______ 。
甲:Mg(OH)2(s)
 Mg2++2OH-①,NH4++H2O
Mg2++2OH-①,NH4++H2O NH3·H2O+H+②,H++OH-=H2O③,由于③反应的发生,使平衡①右移,Mg(OH)2溶解。
NH3·H2O+H+②,H++OH-=H2O③,由于③反应的发生,使平衡①右移,Mg(OH)2溶解。乙:Mg(OH)2(s)
 Mg2++2OH-①,NH4++ OH-
Mg2++2OH-①,NH4++ OH- NH3·H2O②,由于②反应的发生,使平衡①右移,沉淀溶解。
NH3·H2O②,由于②反应的发生,使平衡①右移,沉淀溶解。(1)丙同学不能肯定哪位同学的解释合理,于是用下面的一种试剂重做了该实验,证明甲、乙的解释只有一种正确。他用的试剂是
A.NH4NO3B.CH3COONH4C.(NH4)2SO4D.氨水
(2)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理
更新时间:2020-01-01 08:45:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请按照下列要求回答问题:
(1)电解氯化钠溶液的化学方程式:__________________________________ 。
(2)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:__________________________ 。
(3)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理__________________________ 。
(4)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=__________________________ 。(溶液体积变化忽略不计)。
(5)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=__________________________ 。
(6)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于____________________________ 。
(1)电解氯化钠溶液的化学方程式:
(2)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:
(3)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理
(4)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=
(5)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=
(6)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)明矾净水原理___________________________________ (离子方程式表示),胶体具有________________ 性。
(2)在25℃时,将pH=13的强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比为___________
(3)NH4Cl溶液显______________ (填“酸性”、“中性”或“碱性”),理由是_________ (用离子方程式或必要的文字说明).
(4)NaHCO3溶液中,下列表述正确的是_______
A.c(Na+) + c(H+)= c(HCO3﹣)+ c(CO32﹣)+ c(OH﹣)
B. c(OH﹣)= c(H2CO3)+ c(H+)-c(CO32﹣)
C.c(OH﹣)= c(HCO3﹣)+ c(H+)+c(H2CO3)
D.c (Na+)= c(HCO3﹣)+ c(CO32﹣) + c(H2CO3)
(2)在25℃时,将pH=13的强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比为
(3)NH4Cl溶液显
(4)NaHCO3溶液中,下列表述正确的是
A.c(Na+) + c(H+)= c(HCO3﹣)+ c(CO32﹣)+ c(OH﹣)
B. c(OH﹣)= c(H2CO3)+ c(H+)-c(CO32﹣)
C.c(OH﹣)= c(HCO3﹣)+ c(H+)+c(H2CO3)
D.c (Na+)= c(HCO3﹣)+ c(CO32﹣) + c(H2CO3)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①_________ 和_________ 两种粒子的物质的量之和等于0.1mol。
②_________ 和_________ 两种粒子的物质的量之和比OH―多0.05mol。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是_________ ,上述离子浓度大小顺序关系中正确的是(选填序号)__________ 。
②若上述关系中C是正确的,则溶液中溶质的化学式是__________ 。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同)________ c(NH3·H2O), 混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)___________ c(Cl-)。
①
②
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是
②若上述关系中C是正确的,则溶液中溶质的化学式是
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,可以减少SO2的排放,但产生的CO又会与CaSO4发生化学反应,从而降低脱硫效率。相关的热化学方程式如下:
①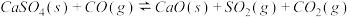
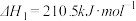
②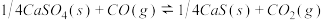
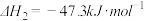
请回答下列问题:
(1)反应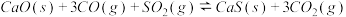 △H2=
△H2=________ kJ•mol-1;平衡时增大压强,此反应________ (“正向”、“逆向”、“不”)移动。
(2)已知298K时,Ksp(CaCO3)=m×10-p,Ksp(CaSO4)=m×10-q。则反应: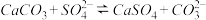 的平衡常数数值表示式为
的平衡常数数值表示式为_________________ (用含m、n、p、q的式子表示)。
(3)用碘量法可测定排放烟气中二氧化硫的含量,请写出碘溶液与二氧化硫发生氧化还原反应的离子方程式_________________ ;
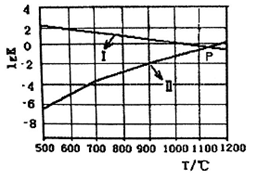
(4)反应①②的平衡常数的对数lgK随反应T的变化曲线见图,其中曲线Ⅰ代表_______ 反应,P为两曲线交点,则在该温度下两反应均达平衡时,体系中c(SO2)=___________ mol•L-1,从减少二氧化硫排放的角度来考虑,本体系适宜的反应条件是_______________________ 。
①
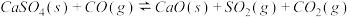
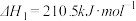
②
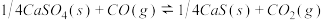
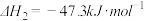
请回答下列问题:
(1)反应
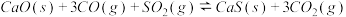 △H2=
△H2=(2)已知298K时,Ksp(CaCO3)=m×10-p,Ksp(CaSO4)=m×10-q。则反应:
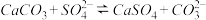 的平衡常数数值表示式为
的平衡常数数值表示式为(3)用碘量法可测定排放烟气中二氧化硫的含量,请写出碘溶液与二氧化硫发生氧化还原反应的离子方程式
(4)反应①②的平衡常数的对数lgK随反应T的变化曲线见图,其中曲线Ⅰ代表
| A.低温低压 | B.低温高压 | C.高温高压 | D.高温低压 |

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学在生产生活中有着广泛的应用,请回答下列问题:
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化______ (填“能”或“不能”)用勒夏特列原理解释。
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:______ 。
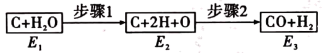
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为______ (填离子符号),再加碱调节至pH为______ 时,铁刚好沉淀完全(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全);继续加碱至pH为6时,锌开始沉淀。若上述过程不加H2O2后果是______ 。(已知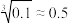 ,lg2
,lg2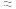 0.3)
0.3)
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:
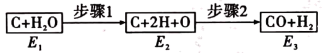
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为
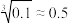 ,lg2
,lg2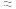 0.3)
0.3)| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp的近似值 | 10-17 | 10-17 | 10-39 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
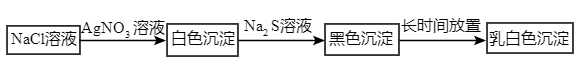
【推荐3】某小组探究 沉淀向
沉淀向 沉淀转化过程中发生了异常现象,便进一步探究原因:
沉淀转化过程中发生了异常现象,便进一步探究原因:
(1)已知 时,
时, 的溶度积
的溶度积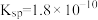 ,则下列说法正确的是
,则下列说法正确的是___________ 。
A.温度一定,当溶液中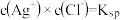 时,此溶液为
时,此溶液为 的饱和溶液
的饱和溶液
B. 溶液与
溶液与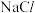 溶液混合后的溶液中,一定有
溶液混合后的溶液中,一定有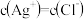
C.向饱和 水溶液中加入盐酸,
水溶液中加入盐酸, 值变大
值变大
D. 时,与水中相比,
时,与水中相比, 在
在 溶液中的溶解度、
溶液中的溶解度、 均要小
均要小
(2)写出 沉淀向
沉淀向 沉淀转化的离子方程式:
沉淀转化的离子方程式:___________ 。
(3)该小组同学认为长时间放置后产生乳白色沉淀与空气中的氧气有关,其反应的化学方程式为: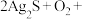 □
□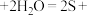 □
□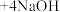 (请在答题卷的方框中填入物质及计量数)
(请在答题卷的方框中填入物质及计量数) ___________ 。
(4)为避免 沉淀向
沉淀向 沉淀转化过程中出现异常现象,需控制的反应条件是
沉淀转化过程中出现异常现象,需控制的反应条件是___________ 。
 沉淀向
沉淀向 沉淀转化过程中发生了异常现象,便进一步探究原因:
沉淀转化过程中发生了异常现象,便进一步探究原因:
(1)已知
 时,
时, 的溶度积
的溶度积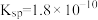 ,则下列说法正确的是
,则下列说法正确的是A.温度一定,当溶液中
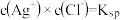 时,此溶液为
时,此溶液为 的饱和溶液
的饱和溶液B.
 溶液与
溶液与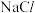 溶液混合后的溶液中,一定有
溶液混合后的溶液中,一定有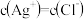
C.向饱和
 水溶液中加入盐酸,
水溶液中加入盐酸, 值变大
值变大D.
 时,与水中相比,
时,与水中相比, 在
在 溶液中的溶解度、
溶液中的溶解度、 均要小
均要小(2)写出
 沉淀向
沉淀向 沉淀转化的离子方程式:
沉淀转化的离子方程式:(3)该小组同学认为长时间放置后产生乳白色沉淀与空气中的氧气有关,其反应的化学方程式为:
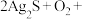 □
□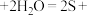 □
□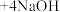 (请在答题卷的方框中填入物质及计量数)
(请在答题卷的方框中填入物质及计量数) (4)为避免
 沉淀向
沉淀向 沉淀转化过程中出现异常现象,需控制的反应条件是
沉淀转化过程中出现异常现象,需控制的反应条件是
您最近一年使用:0次



