某温度时,在水中的电离常数: ;在冰醋酸中
;在冰醋酸中 ;
; 则下列说法不正确的是
则下列说法不正确的是

 ;在冰醋酸中
;在冰醋酸中 ;
; 则下列说法不正确的是
则下列说法不正确的是

A. 在水中为强酸,在冰醋酸中为弱酸 在水中为强酸,在冰醋酸中为弱酸 |
B.在冰醋酸中可能发生反应: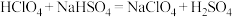 |
C.在某温度下,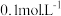 氨水和醋酸溶液中, 氨水和醋酸溶液中, |
D.氨水和 溶液反应后,若 溶液反应后,若 ,则溶液呈酸性 ,则溶液呈酸性 |
更新时间:2020-01-27 09:57:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向20 mL0.1 mol·L-1的醋酸溶液中滴加未知浓度的NaOH溶液,测得混合溶液的温度、pH随加入NaOH体积的变化如图所示,下列说法错误的是


| A.NaOH溶液的物质的量浓度为0.1 mol·L-1 |
| B.整个滴定过程中,b点水的电离程度最大 |
| C.c点溶液中存在c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.a、b、c三点对应醋酸的电离平衡常数:K(b)>K(a)>K(c) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用平衡移动原理,分析常温下Ni2+在不同pH的Na2CO3体系中的可能产物。已知:图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系;图2中曲线I的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 ;[注:起始Na2CO3体系中
;[注:起始Na2CO3体系中 ;不同pH下
;不同pH下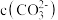 由图1得到]。下列说法正确的是
由图1得到]。下列说法正确的是
 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 ;[注:起始Na2CO3体系中
;[注:起始Na2CO3体系中 ;不同pH下
;不同pH下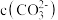 由图1得到]。下列说法正确的是
由图1得到]。下列说法正确的是
A. 时,碳酸钠溶液体系中存在: 时,碳酸钠溶液体系中存在: |
B.M点时,溶液中存在 |
C.初始状态 、 、 ,平衡后存在 ,平衡后存在 |
D.沉淀 制备 制备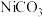 时,选用 时,选用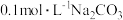 溶液比 溶液比 溶液效果好 溶液效果好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温时,下列溶液的pH或微粒的物质的量浓度关系错误的是
| A.某溶液中由水电离出的c(H+)=1×10-amol·L-1,若a>7时,该溶液pH一定为14-a |
| B.0.1mol·L-1的KHA溶液,其pH=10,c(K+)>c(HA-)>c(OH-)>c(A2-) |
| C.将0.2mol·L-1的某一元酸HA溶液和0.1mol·L-1NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(HA)>c(Na+)>c(A-) |
| D.等体积、等物质的量浓度的Na2CO3溶液与 NaHCO3溶液混合:2c(Na+)=3c(CO32-)+3c( HCO3-)+3c(H2CO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA是阿伏加德罗常数的值,下列说法正确的是
A.1 L1 mol/L溴化铵水溶液中 与H+离子数之和为NA 与H+离子数之和为NA |
| B.58 g正丁烷和异丁烷的混合物中共价键数目为13NA |
| C.1 mol重水比1 mol水多NA个质子 |
| D.常温下,pH=9的CH3COONa溶液中,水电离出的OH—数为10-5NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知25 ℃时有关弱酸的电离平衡常数:
由此可得出
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡 常数(25 ℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A.对应钠盐溶液pH关系为: pH(Na2CO3) > pH(NaCN) > pH(CH3COONa) |
| B.CO2通入NaCN溶液中有:CO2+H2O+2NaCN→Na2CO3+2HCN |
| C.冰醋酸中逐滴加水,溶液的导电性、pH均先增大后减小 |
| D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-) +2c(CO32-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】生产上用过量烧碱溶液处理某矿物 含
含 、
、 ,过滤后得到的滤液用
,过滤后得到的滤液用  溶液处理,测得溶液的pH和
溶液处理,测得溶液的pH和 生成的量随加入
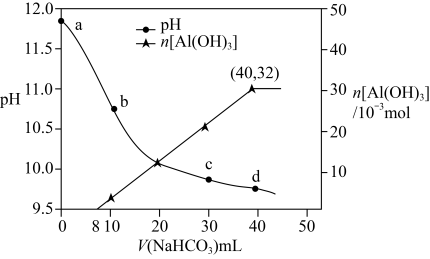
生成的量随加入 溶液体积变化的曲线如下图所示。下列有关说法错误的是( )
溶液体积变化的曲线如下图所示。下列有关说法错误的是( )
 含
含 、
、 ,过滤后得到的滤液用
,过滤后得到的滤液用  溶液处理,测得溶液的pH和
溶液处理,测得溶液的pH和 生成的量随加入
生成的量随加入 溶液体积变化的曲线如下图所示。下列有关说法错误的是( )
溶液体积变化的曲线如下图所示。下列有关说法错误的是( )
A.a点溶液中存在: |
| B.水的电离程度:a点小于c点 |
C.原 溶液中 溶液中 |
D.生成沉淀的离子方程式为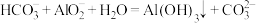 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是


| A.在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
| C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+) |
您最近一年使用:0次

 与S反应生成
与S反应生成 ,则
,则 与S反应可生成
与S反应可生成
 根据化合价规律可表示为
根据化合价规律可表示为 ,则
,则 可表示为
可表示为
 通入
通入 溶液生成
溶液生成 溶液生成
溶液生成

 的
的 溶液:
溶液: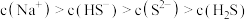
 溶液加水稀释后,溶液中
溶液加水稀释后,溶液中 的值减小
的值减小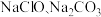 混合溶液中:
混合溶液中:


