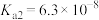0.2 mol/L CH3COOH溶液和0.1 mol/L NaOH溶液等体积混合,则溶液显_______ ,溶液中离子浓度大小关系是______ 。
更新时间:2020-02-18 16:43:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知溶液中只存在OH-、H+、Na+、CH3COO-四种离子,试回答下列问题:
(1)若溶液中只溶解了一种溶质,则该溶质是___________ ,溶液中c(H+)_____ c(OH-)(填“>”、“=”或“<”)。
(2)若溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则该溶液中的溶质为_____________ ,若溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则该溶液中溶质为_________________ 。
(3)若该溶液是由体积相等的NaOH溶液和醋酸溶液混合而成,且恰好呈中性,则混合前c(NaOH)__________ c(CH3COOH),混合前碱中c(OH-)和酸中c(H+)的关系c(OH-)__________ c(H+)(填“>”,“=”或“<”)。
(1)若溶液中只溶解了一种溶质,则该溶质是
(2)若溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则该溶液中的溶质为
(3)若该溶液是由体积相等的NaOH溶液和醋酸溶液混合而成,且恰好呈中性,则混合前c(NaOH)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知水在25℃和100℃时,其电离平衡曲线如图所示:
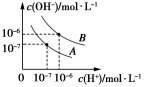
(1)100℃时,水的离子积KW =_______ ,0.01mol/L NaOH溶液的pH =_____ ,水的电离平衡曲线应为_____ (填“A”或“B”)。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为_____
(3)25℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是_________________ 。

(1)100℃时,水的离子积KW =
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(3)25℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据表中数据(室温),回答下列问题:
已知氢氟酸、醋酸、次氯酸(HClO)、碳酸的电离常数分别为:
(1)写出以下反应的离子方程式:
①足量的氢氟酸与碳酸钠溶液混合:___________ ;
②少量的CO2通入NaClO溶液:___________ 。
(2)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)___________ mol/L(填精确值), =
=___________ 。
(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为___________ 。
(4)室温下pH=9的NaOH溶液和pH=10的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于___________ 。
(5)甲醇与CO可以生成醋酸,常温下将amol/L的醋酸与bmol∙L-1Ba(OH)2溶液以2∶1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO-),则醋酸的电离平衡常数为_______ (用含a和b的代数式表示)。
已知氢氟酸、醋酸、次氯酸(HClO)、碳酸的电离常数分别为:
| HF | Ka=6.8×10-4mol•L-1 |
| CH3COOH | Ka=1.7×10-5mol•L-1 |
| HClO | Ka=2.9×10-8mol•L-1 |
| H2CO3 | Ka1=4.4×10-7mol•L-1 Ka2=4.7×10-11mol•L-1 |
①足量的氢氟酸与碳酸钠溶液混合:
②少量的CO2通入NaClO溶液:
(2)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)
 =
=(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为
(4)室温下pH=9的NaOH溶液和pH=10的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于
(5)甲醇与CO可以生成醋酸,常温下将amol/L的醋酸与bmol∙L-1Ba(OH)2溶液以2∶1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO-),则醋酸的电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
(1)25℃时,pH相等的三种溶液①CH3COONa溶液、②Na2CO3溶液、③NaCN溶液,浓度由大到小的顺序为_______ 。(填序号)
(2)碳酸第一步电离的电离平衡常数表达式为_______ 。
(3)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为_______ 。
(4)将浓度为0.02 mol·L-1的HCN与0.01 mol·L-1 NaOH溶液等体积混合后,溶液呈碱性,则混合溶液中c (Na+)_______ c (CN-)(填“<”或“>”或“=”)
| 氢氰酸 | 碳酸 | 醋酸 |
| Ka=4.0×10-10 | Ka1=4.2×10-7 Ka2=4.8×10-11 | Ka=1.8×10-5 |
(2)碳酸第一步电离的电离平衡常数表达式为
(3)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为
(4)将浓度为0.02 mol·L-1的HCN与0.01 mol·L-1 NaOH溶液等体积混合后,溶液呈碱性,则混合溶液中c (Na+)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】25℃时,50mL 0.10mol/L的醋酸中存在着如下平衡:CH3COOH  CH3COO―+H+。若分别作如下改变,对上述平衡有何影响
CH3COO―+H+。若分别作如下改变,对上述平衡有何影响
(1)加入少量冰醋酸,平衡将_______________________ ,溶液中c(H+)将________________ ;
(2)加入一定量蒸馏水,平衡将__________________ ,溶液中c(H+)将__________ ;
(3)加入少量0.10mol/L盐酸,平衡将________________ ,溶液中c(H+)将_________________ ;
(4)加入20 mL 0.10mol/L的NaOH溶液,平衡将__________________ ,溶液中c(H+)将__________________ 。
 CH3COO―+H+。若分别作如下改变,对上述平衡有何影响
CH3COO―+H+。若分别作如下改变,对上述平衡有何影响(1)加入少量冰醋酸,平衡将
(2)加入一定量蒸馏水,平衡将
(3)加入少量0.10mol/L盐酸,平衡将
(4)加入20 mL 0.10mol/L的NaOH溶液,平衡将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知298K时,几种物质的电离平衡常数(K)如下表:
(1)25℃时, 和
和 混合溶液的
混合溶液的 ,则溶液中的
,则溶液中的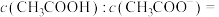
________ 。
(2) 溶液和
溶液和 溶液反应的离子方程式为
溶液反应的离子方程式为________ 。
(3)25℃时,浓度均为 的NaClO溶液和
的NaClO溶液和 溶液,二者离子总浓度
溶液,二者离子总浓度________ (填字母)。
A.前者大 B.后者大 C.相等
(4)若将 的HCl和
的HCl和 两溶液分别加水稀释,pH变化如图所示,图中a、b、c三点对应溶液的导电能力由强到弱的顺序是
两溶液分别加水稀释,pH变化如图所示,图中a、b、c三点对应溶液的导电能力由强到弱的顺序是________ 。

(5)25℃时,将 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,用含a的代数式表示
,用含a的代数式表示 的电离常数
的电离常数
________ 。
化学式 | HClO |
|
|
|
电离常数 |
|
|
|
|
 和
和 混合溶液的
混合溶液的 ,则溶液中的
,则溶液中的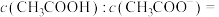
(2)
 溶液和
溶液和 溶液反应的离子方程式为
溶液反应的离子方程式为(3)25℃时,浓度均为
 的NaClO溶液和
的NaClO溶液和 溶液,二者离子总浓度
溶液,二者离子总浓度A.前者大 B.后者大 C.相等
(4)若将
 的HCl和
的HCl和 两溶液分别加水稀释,pH变化如图所示,图中a、b、c三点对应溶液的导电能力由强到弱的顺序是
两溶液分别加水稀释,pH变化如图所示,图中a、b、c三点对应溶液的导电能力由强到弱的顺序是
(5)25℃时,将
 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,用含a的代数式表示
,用含a的代数式表示 的电离常数
的电离常数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用 氨水滴定
氨水滴定 浓度均为
浓度均为 的
的 和
和 的混合液,回答下列问题:
的混合液,回答下列问题:
(1)在氨水滴定前, 和
和 的混合液中
的混合液中
_______  (填“>”、“<”或“=”,下同);
(填“>”、“<”或“=”,下同);
(2)当滴入氨水 时,
时,
_______  ;
;
(3)当滴入氨水 时,
时,
_______ 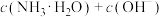 ;
;
(4)当溶液呈中性时,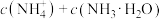
_______  。
。
 氨水滴定
氨水滴定 浓度均为
浓度均为 的
的 和
和 的混合液,回答下列问题:
的混合液,回答下列问题:(1)在氨水滴定前,
 和
和 的混合液中
的混合液中
 (填“>”、“<”或“=”,下同);
(填“>”、“<”或“=”,下同);(2)当滴入氨水
 时,
时,
 ;
;(3)当滴入氨水
 时,
时,
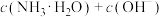 ;
;(4)当溶液呈中性时,
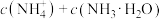
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,现有浓度均为0.1 mol•L-1的下列溶液:①盐酸,②醋酸,③氢氧化钠,④氯化铵,⑤醋酸铵,⑥硫酸氢铵,⑦氨水,请回答下列问题:
(1)溶液③的pH=_______ 。
(2)④、⑤、⑥、⑦四种溶液中 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号)_______ 。
(3)①、②、③、⑦四种溶液pH由大到小的顺序是(填序号)_______ 。
(4)已知t℃时,Kw=1×10-13,则t℃_______ (填“>”“<”或“=”)25℃。
(5)①,③等体积混合后pH_______ 7(填“>”“<”或“=”),①,⑦等体积混合后pH_______ 7(填“>”“<”或“=”)
(1)溶液③的pH=
(2)④、⑤、⑥、⑦四种溶液中
 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号)(3)①、②、③、⑦四种溶液pH由大到小的顺序是(填序号)
(4)已知t℃时,Kw=1×10-13,则t℃
(5)①,③等体积混合后pH
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】水溶液中存在多种平衡,请根据所学化学知识回答下列问题:
(1)在浓度均为0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH3.H2O ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为(填序号)___ 。
(2)浓度均为0.1mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵四种溶液中的H+浓度由大到小的顺序是(填序号)___ 。
(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=___ 。
(4)将FeCl3、NaHCO3、K2SO3溶液蒸干、灼烧后得到的固体物质分别是___ 。
(1)在浓度均为0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH3.H2O ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为(填序号)
(2)浓度均为0.1mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵四种溶液中的H+浓度由大到小的顺序是(填序号)
(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=
(4)将FeCl3、NaHCO3、K2SO3溶液蒸干、灼烧后得到的固体物质分别是
您最近一年使用:0次