下列有关水溶液中的离子问题的叙述中正确的是( )
| A.pH=12的氨水和pH=2的盐酸等体积混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.将pH=11的氨水溶液稀释后,恢复至原温度,pH和Kw均减小 |
| C.向一定量的醋酸溶液中逐滴加入物质的量浓度相同的氢氧化钠溶液,直至氢氧化钠过量,在实验过程中水的电离程度的变化趋势是先小后大 |
| D.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(CO32-)+c(HCO3-)+c(H2CO3) |
更新时间:2020-02-21 10:49:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,有关下列溶液的说法正确的是
A.加水稀释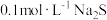 溶液时,溶液中各离子浓度均减小 溶液时,溶液中各离子浓度均减小 |
B. 相同的 相同的 和 和 溶液中水的电离程度相同 溶液中水的电离程度相同 |
C. 相同的① 相同的① ② ② ③ ③ 三种溶液的 三种溶液的 :③>②>① :③>②>① |
D.将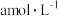 的氨水与 的氨水与 盐酸等体积混合,平衡时 盐酸等体积混合,平衡时 , , 的电离平衡常数可表示为 的电离平衡常数可表示为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】室温下向10 mL 0.1 mol/L 的氨水中加水稀释后,下列说法正确的是
| A.溶液中导电离子的数目减少 |
B.溶液中 不变 不变 |
| C.NH3·H2O的电离程度增大,c(OH-)亦增大 |
| D.Kw随氨水浓度减小而减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,将11.65 g BaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中不正确的是


| A.相同温度时,Ksp(BaSO4)<Ksp(BaCO3) |
| B.若使0.05 mol BaSO4全部转化为BaCO3,至少加入1.3 mol Na2CO3 |
| C.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(CO32-)>c(SO42-)>c(OH-)>c(Ba2+) |
| D.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,某小组做如下两组实验:
实验Ⅰ:分别往浓度均为 、
、 溶液中通入
溶液中通入 至
至 ;
;
实验Ⅱ:在1.0L、 溶液中加入
溶液中加入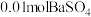 固体,充分反应。
固体,充分反应。
[已知:25℃, 的电离常数
的电离常数 、
、 ;
; 、
、 。混合后溶液体积变化忽略不计]。下列说法
。混合后溶液体积变化忽略不计]。下列说法不正确 的是
实验Ⅰ:分别往浓度均为
 、
、 溶液中通入
溶液中通入 至
至 ;
;实验Ⅱ:在1.0L、
 溶液中加入
溶液中加入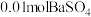 固体,充分反应。
固体,充分反应。[已知:25℃,
 的电离常数
的电离常数 、
、 ;
; 、
、 。混合后溶液体积变化忽略不计]。下列说法
。混合后溶液体积变化忽略不计]。下列说法A. 、 、 溶液中水的电离程度: 溶液中水的电离程度: |
B.实验Ⅰ结束后, 、 、 溶液中均有 溶液中均有 |
C.实验Ⅱ的转化存在平衡常数: |
D.实验Ⅱ中,改用饱和 溶液, 溶液, 的平衡转化率减小 的平衡转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】25℃时,由醋酸和醋酸钠按一定比例混合形成的溶液始终保持c(CH3COOH) +c(CH3COO-)= 0.1mol/L,该溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如下图所示,下列有关该溶液的叙述中正确的是


| A.pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.W点所表示的溶液中:c(Na+)=c(CH3COOH) |
| C.pH=3的溶液中:c(H+)+c(Na+)+c(CH3COOH)=0.1mol/L |
| D.据图象可求得该温度下CH3COOH的电离常数Ka=10-4.75 |
您最近一年使用:0次



