一氧化碳是一种重要的化工原料,被应用于很多化工生产中。
(1)高炉炼铁中发生的反应之一是:FeO(s)+CO(g) Fe(s)+CO2(g)+11kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将
Fe(s)+CO2(g)+11kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将_______ (填“增大”、“减小”或“不变”)。
(2)已知1100℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.263,现测得高炉中[CO2]=0.025mol/L,[CO]=0.1mol/L,此时该反应
Fe(s)+CO2(g)的平衡常数K=0.263,现测得高炉中[CO2]=0.025mol/L,[CO]=0.1mol/L,此时该反应_______ (填字母代号)。
A.向正反应方向进行 B.处于平衡状态 C.向逆反应方向进行
(3)合成氨工业中需将原料气中的CO变成CO2除去。在密闭容器中将等体积的CO和H2O混合加热到830℃,达到下列平衡:CO(g)+H2O(g) CO2(g)+H2(g);若平衡时[H2O]=[CO2],则CO转化成CO2的转化率是
CO2(g)+H2(g);若平衡时[H2O]=[CO2],则CO转化成CO2的转化率是_________ 。
(4)用CO和H2经如下两步反应反应制得甲酸甲酯:
①CO+2H2→CH3OH
②CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为0.8,反应②中两种反应物的转化率均为0.85,则2.52kg CO最多可制得甲酸甲酯___________ kg。
(1)高炉炼铁中发生的反应之一是:FeO(s)+CO(g)
 Fe(s)+CO2(g)+11kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将
Fe(s)+CO2(g)+11kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将(2)已知1100℃时,反应FeO(s)+CO(g)
 Fe(s)+CO2(g)的平衡常数K=0.263,现测得高炉中[CO2]=0.025mol/L,[CO]=0.1mol/L,此时该反应
Fe(s)+CO2(g)的平衡常数K=0.263,现测得高炉中[CO2]=0.025mol/L,[CO]=0.1mol/L,此时该反应A.向正反应方向进行 B.处于平衡状态 C.向逆反应方向进行
(3)合成氨工业中需将原料气中的CO变成CO2除去。在密闭容器中将等体积的CO和H2O混合加热到830℃,达到下列平衡:CO(g)+H2O(g)
 CO2(g)+H2(g);若平衡时[H2O]=[CO2],则CO转化成CO2的转化率是
CO2(g)+H2(g);若平衡时[H2O]=[CO2],则CO转化成CO2的转化率是(4)用CO和H2经如下两步反应反应制得甲酸甲酯:
①CO+2H2→CH3OH
②CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为0.8,反应②中两种反应物的转化率均为0.85,则2.52kg CO最多可制得甲酸甲酯
12-13高三上·上海金山·期末 查看更多[1]
(已下线)上海市金山区2012届高三上学期期末考试化学试题
更新时间:2020-03-31 09:22:47
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】工业烟气中的氮氧化物可用NH3催化还原,发生反应:4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH<0,研究表明不同氨氮比[m= ]条件下测得NO的残留率与温度关系如图所示。
]条件下测得NO的残留率与温度关系如图所示。

随着温度不断升高,NO的残留率趋近相同的可能原因是_____ 。
 ]条件下测得NO的残留率与温度关系如图所示。
]条件下测得NO的残留率与温度关系如图所示。
随着温度不断升高,NO的残留率趋近相同的可能原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国科学家研制出一种新型催化剂,实现了温和条件下“人工固氨”。在催化剂表面和常温常压下发生反应: 。
。
(1)改变下列一个条件,能提高活化分子百分数的是_______ (填字母)。
A.增大反应物浓度 B.加入高效催化剂 C.适当升温 D.增大压强
(2)在某恒温恒容密闭容器中充入足量液态水和N2,达到平衡后,再充入少量N2,N2的平衡转化率_______ (填“增大”“减小”或“不变”)。达到平衡后,液化分离NH3,其目的是_______ 。
(3)在总压强恒定为16 kPa和T K条件下,向某密闭容器中充入足量液态水,再充入N2(g)和Ar(g)的混合气体(Ar不参与反应),发生上述反应,起始时混合气体中N2的体积分数与N2的平衡转化率的关系如图所示。

①保持总压强和温度不变,充入Ar(g)与不充入相比,N2的平衡转化率增大的原因是_______ 。
②计算T K时上述反应的平衡常数Kp=_______ (kPa)5(只列计算式,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
 。
。(1)改变下列一个条件,能提高活化分子百分数的是
A.增大反应物浓度 B.加入高效催化剂 C.适当升温 D.增大压强
(2)在某恒温恒容密闭容器中充入足量液态水和N2,达到平衡后,再充入少量N2,N2的平衡转化率
(3)在总压强恒定为16 kPa和T K条件下,向某密闭容器中充入足量液态水,再充入N2(g)和Ar(g)的混合气体(Ar不参与反应),发生上述反应,起始时混合气体中N2的体积分数与N2的平衡转化率的关系如图所示。

①保持总压强和温度不变,充入Ar(g)与不充入相比,N2的平衡转化率增大的原因是
②计算T K时上述反应的平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Na2SO3是中学化学中常用的试剂。测定0.1 mol·L-1的Na2SO3溶液的pH与温度关系如下表所示(已知d>c>b>a)。
(1)水的离子积:Kw(a)___________ (填“>”“<”或“=”,下同)Kw(d);水解常数:Kh1(a)___________ Kh1(b)。
(2)分别取a、d时刻的溶液各10 mL,加入足量的用盐酸酸化的BaCl2溶液做对比实验,d时刻溶液产生的白色沉淀比a时刻的多。该白色沉淀的化学式是___________ ,d时刻沉淀比a时刻溶液多的原因是___________ 。
(3)数据显示:a→c的过程中,___________ (填“浓度”或“温度”)对水解平衡移动方向的影响程度更大。
(4)为了证明上述规律的普遍性,可以选择下列物质做类似实验,该物质是___________(填字母)。
| 时刻 | a | b | c | d |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
(1)水的离子积:Kw(a)
(2)分别取a、d时刻的溶液各10 mL,加入足量的用盐酸酸化的BaCl2溶液做对比实验,d时刻溶液产生的白色沉淀比a时刻的多。该白色沉淀的化学式是
(3)数据显示:a→c的过程中,
(4)为了证明上述规律的普遍性,可以选择下列物质做类似实验,该物质是___________(填字母)。
| A.Na2CO3 | B.NaHCO3 | C.Na2S | D.Na2SO4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐1】在温度t1和t2下,X2(g)和 H2反应生成HX的平衡常数如下表:
(1)已知t2>t1,HX的生成反应是_______ 反应(填“吸热”或“放热”)。
(2)HX的电子式是_______ 。
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是_______ 。
(4)X2都能与H2反应生成HX,用原子结构解释原因:_______ 。
(5)K的变化体现出X2化学性质的递变性,用原子结构解释原因:_______ ,原子半径逐渐增大,得电子能力逐渐减弱。
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,_______ (选填字母)
a. 在相同条件下,平衡时X2的转化率逐渐降低
b. X2与H2反应的剧烈程度逐渐减弱
c. HX的还原性逐渐
d. HX的稳定性逐渐减弱
| 化学方程式 | K (t1 ) | K (t2) |
F2+H2 2HF 2HF | 1.8×1036 | 1.9×1032 |
Cl2+H2 2HCl 2HCl | 9.7×1012 | 4.2×1011 |
Br2+H2 2HBr 2HBr | 5.6×107 | 9.3×106 |
I2+H2 2HI 2HI | 43 | 34 |
(1)已知t2>t1,HX的生成反应是
(2)HX的电子式是
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是
(4)X2都能与H2反应生成HX,用原子结构解释原因:
(5)K的变化体现出X2化学性质的递变性,用原子结构解释原因:
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,
a. 在相同条件下,平衡时X2的转化率逐渐降低
b. X2与H2反应的剧烈程度逐渐减弱
c. HX的还原性逐渐
d. HX的稳定性逐渐减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
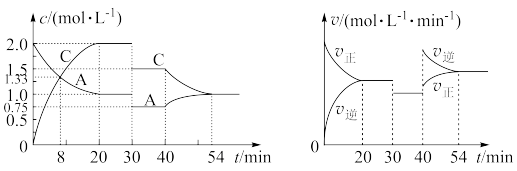
(1)0~20min,A的平均反应速率为__ mol/(L·min);8min时,v正__ v逆(填“>”“=”或“<”)。
(2)反应方程式中的x=__ ,30min时改变的反应条件是__ 。
(3)20~30min时反应的平衡常数__ (填“>”“=”或“<”)30〜40min时反应的平衡常数。
(4)该反应的正反应为__ (填“放热”或“吸热”)反应。
(5)反应过程中B的转化率最大的时间段是_ min。
 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
(1)0~20min,A的平均反应速率为
(2)反应方程式中的x=
(3)20~30min时反应的平衡常数
(4)该反应的正反应为
(5)反应过程中B的转化率最大的时间段是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐3】(1)元素M 的离子与NH4+所含电子数和质子数均相同,则M的原子结构示意图为_ 。
(2)硫酸铝溶液与过量氨水反应的离子方程式为 _。
(3)能证明Na2SO3溶液中存在SO32-+H2O HSO3-+OH-水解平衡的事实是 _(填序号)。
HSO3-+OH-水解平衡的事实是 _(填序号)。
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色退去
(4)元素X、Y 在周期表中位于向一主族,化合物Cu2X和Cu2Y 可发生如下转化(其中D 是纤维素水解的最终产物):

① 非金属性X Y(填“>”或“<”)
② Cu2Y与过量浓硝酸反应有红棕色气体生成,化学方程式为
(5)在恒容绝热(不与外界交换能量)条件下进行2A ( g ) + B ( g) 2C ( g ) + D ( s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:
2C ( g ) + D ( s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:
(2)硫酸铝溶液与过量氨水反应的离子方程式为 _。
(3)能证明Na2SO3溶液中存在SO32-+H2O
 HSO3-+OH-水解平衡的事实是 _(填序号)。
HSO3-+OH-水解平衡的事实是 _(填序号)。A.滴入酚酞溶液变红,再加入H2SO4溶液后红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色退去
(4)元素X、Y 在周期表中位于向一主族,化合物Cu2X和Cu2Y 可发生如下转化(其中D 是纤维素水解的最终产物):

① 非金属性X Y(填“>”或“<”)
② Cu2Y与过量浓硝酸反应有红棕色气体生成,化学方程式为
(5)在恒容绝热(不与外界交换能量)条件下进行2A ( g ) + B ( g)
 2C ( g ) + D ( s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:
2C ( g ) + D ( s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硫化氢 有臭鸡蛋气味,能溶于水。研究发现,
有臭鸡蛋气味,能溶于水。研究发现, 具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1) 与
与 在高温条件下发生反应:
在高温条件下发生反应: 。在610K时,将
。在610K时,将 与
与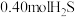 充入2.5L的空钢瓶中,反应平衡后测得水的物质的量分数为2%。
充入2.5L的空钢瓶中,反应平衡后测得水的物质的量分数为2%。
① 的平衡转化率
的平衡转化率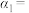
___________ %,反应平衡常数
___________ (保留两位有效数字)。
②在620K下重复试验,平衡后水的物质的量分数为3%, 的转化率
的转化率
___________  ,该反应的
,该反应的
___________ 0(填“>”“<”“=”,上同)。
③向反应器中再分别充入下列气体,能使 转化率增大的是
转化率增大的是___________ (填序号)。
A. B.
B. C.
C. D.
D.
(2)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
煤的气化过程中产生的 可用足量的
可用足量的 溶液吸收,该反应的离子方程式为
溶液吸收,该反应的离子方程式为___________ 。
(3)常温下,在某酸性溶液中通入 至饱和时,测得
至饱和时,测得 ,硫化氢的平衡浓度为
,硫化氢的平衡浓度为 ,计算此时溶液中
,计算此时溶液中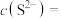
___________  (保留两位有效数字)。
(保留两位有效数字)。
 有臭鸡蛋气味,能溶于水。研究发现,
有臭鸡蛋气味,能溶于水。研究发现, 具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:(1)
 与
与 在高温条件下发生反应:
在高温条件下发生反应: 。在610K时,将
。在610K时,将 与
与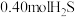 充入2.5L的空钢瓶中,反应平衡后测得水的物质的量分数为2%。
充入2.5L的空钢瓶中,反应平衡后测得水的物质的量分数为2%。①
 的平衡转化率
的平衡转化率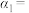

②在620K下重复试验,平衡后水的物质的量分数为3%,
 的转化率
的转化率
 ,该反应的
,该反应的
③向反应器中再分别充入下列气体,能使
 转化率增大的是
转化率增大的是A.
 B.
B. C.
C. D.
D.
(2)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
| 电离平衡常数 |  |  |
 |  | 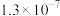 |
 | 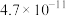 |  |
 可用足量的
可用足量的 溶液吸收,该反应的离子方程式为
溶液吸收,该反应的离子方程式为(3)常温下,在某酸性溶液中通入
 至饱和时,测得
至饱和时,测得 ,硫化氢的平衡浓度为
,硫化氢的平衡浓度为 ,计算此时溶液中
,计算此时溶液中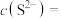
 (保留两位有效数字)。
(保留两位有效数字)。
您最近一年使用:0次
【推荐2】已知一个固定容积的密闭容器中,发生如下反应:M(g)+N(g)⇌P(g)+Q(g) ,△H>0 请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol/L,c(N)=2.4mol/L,达到平衡后,M的转化率为60%,此时N的转化率为__________ ;原混合气体与平衡混合气体的压强之比,p(始):p(平)=________
(2)若反应温度升高,M的转化率_____ (填“增大”“减小”或“不变”;)
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol/L, c(N)=a mol/L;达到平衡后,c(P)=2mol/L,a=________
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=bmol/L,达到平衡后,M的转化率为________ 。
(5)若反应温度不变,某一时刻测得容器内各物质的浓度分别为c(M)=0.5mol/L,c(Y)=0.2mol/L,c(P)=0.4mol/L,c(Q)=0.4mol/L,则下一时刻,反应向__________ (填“正向”或“逆向”)进行。
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol/L,c(N)=2.4mol/L,达到平衡后,M的转化率为60%,此时N的转化率为
(2)若反应温度升高,M的转化率
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol/L, c(N)=a mol/L;达到平衡后,c(P)=2mol/L,a=
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=bmol/L,达到平衡后,M的转化率为
(5)若反应温度不变,某一时刻测得容器内各物质的浓度分别为c(M)=0.5mol/L,c(Y)=0.2mol/L,c(P)=0.4mol/L,c(Q)=0.4mol/L,则下一时刻,反应向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在密闭容器中,使1 mol N2和3 mol H2混合发生下列反应:N2 (g) + 3H2 (g) 2NH3 (g) ΔH <0。
2NH3 (g) ΔH <0。
(1)达到平衡时, 充入N2并保持体积不变,平衡将______ 移动(填“正向”、“逆向”或“不”)。
(2)达到平衡时,充入氩气(Ar)并保持体积不变,平衡将______ 移动(同上)。
(3)达到平衡时,充入氩气(Ar),并保持压强不变,平衡将______ 移动(同上)。
(4)达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡______ 移动(同上)。
(5)保持体积不变,升高温度时,混和气体的平均相对分子质量______ ,密度_______ (填“变大”、“变小”或“不变”)。
(6)当反应达到平衡时,N2和H2的浓度比是______ ;N2和H2的转化率比是______ 。
 2NH3 (g) ΔH <0。
2NH3 (g) ΔH <0。(1)达到平衡时, 充入N2并保持体积不变,平衡将
(2)达到平衡时,充入氩气(Ar)并保持体积不变,平衡将
(3)达到平衡时,充入氩气(Ar),并保持压强不变,平衡将
(4)达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡
(5)保持体积不变,升高温度时,混和气体的平均相对分子质量
(6)当反应达到平衡时,N2和H2的浓度比是
您最近一年使用:0次



