某工业尾气中含有NO和NO2(通常表示为NOx),处理尾气常用以下方法。
方法一:氨气还原法:NH3+NOx→N2+H2O(未配平),
方法二:用碱液吸收:2NO2+2NaOH→NaNO2+NaNO3+H2O;NO+NO2+2NaOH→2NaNO2+H2O。
(1)另写一个氨气作还原剂的化学方程式:__ ;
(2)方法二中若使NOx完全被吸收。则n(NO2)__ n(NO)(填“≤”、“=”、“≥”);NOx中 =
=__ (用含“x”的代数式表示);
(3)若用方法一消除NOx,当x=1.75时,则应通入的氨气与NOx的体积比(同温同压下) ≥
≥__ ;
(4)若气体中除含NOx(NO和NO2)外,还含有体积分数为y的N2O4,用方法二处理1mol这种气体,气体完全被吸收。计算:
①若y=0.2,求生成NaNO3和NaNO2的质量___ ;
②满足气体完全被吸收的y和x的关系式___ 。
方法一:氨气还原法:NH3+NOx→N2+H2O(未配平),
方法二:用碱液吸收:2NO2+2NaOH→NaNO2+NaNO3+H2O;NO+NO2+2NaOH→2NaNO2+H2O。
(1)另写一个氨气作还原剂的化学方程式:
(2)方法二中若使NOx完全被吸收。则n(NO2)
 =
=(3)若用方法一消除NOx,当x=1.75时,则应通入的氨气与NOx的体积比(同温同压下)
 ≥
≥(4)若气体中除含NOx(NO和NO2)外,还含有体积分数为y的N2O4,用方法二处理1mol这种气体,气体完全被吸收。计算:
①若y=0.2,求生成NaNO3和NaNO2的质量
②满足气体完全被吸收的y和x的关系式
2010·上海松江·二模 查看更多[1]
(已下线)上海市松江区2010届高三第二次模拟考试化学试题
更新时间:2020-04-04 08:56:21
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)2molO3和3molO2的质量之比为____ ,分子数之比为____ ;同温同压下的密度之比为____ ,含氧原子数之比为_____ ,体积之比为____ 。
(2)气体化合物A的化学式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为____ ,推断的依据是____ 。
(3)标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞如图。已知甲室中气体的质量比乙室中气体的质量少33.8g。
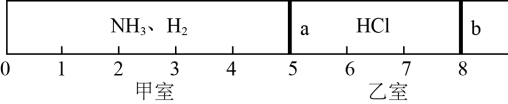
请回答下列问题:
①甲室中气体的物质的量为____ mol。
②甲室中气体的质量为____ g。
③甲室中NH3、H2的物质的量之比为___ ,质量之比为____ 。
④如果将活塞a去掉,当HCl与NH3完全反应后,活塞b将静止于刻度“____ ”(填数字)处。
(2)气体化合物A的化学式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为
(3)标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞如图。已知甲室中气体的质量比乙室中气体的质量少33.8g。

请回答下列问题:
①甲室中气体的物质的量为
②甲室中气体的质量为
③甲室中NH3、H2的物质的量之比为
④如果将活塞a去掉,当HCl与NH3完全反应后,活塞b将静止于刻度“
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】计算填空:
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为_______ 。
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为_______ 。
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为_______ 。
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为_______ g。(已知:2NaHCO3 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)
(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=______ mol/L。
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为
 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(Ⅰ)把15.6gNa2O2放入100mL水中,充分反应后,计算:
(1)生成O2在标准状况的体积___________ mL;
(2)反应后所得NaOH的物质的量浓度___________ 。(反应前后溶液体积变化忽略不计)。
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象____________ 。
(4)则原混合物中Fe2O3与Fe的物质的量之比为___________ 。
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为_______ L(标准状况)。
(1)生成O2在标准状况的体积
(2)反应后所得NaOH的物质的量浓度
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象
(4)则原混合物中Fe2O3与Fe的物质的量之比为
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】Zn与不同浓度的H2SO4反应,其还原产物不同,
(1)将13g锌粉投入足量的18.4mol/L的浓硫酸中,充分反应后,所得SO2气体其标况下体积为多少升?_____
(2)若将一定量的锌投入100mL14.5mol/L的浓硫酸中,反应后锌完全溶解,将反应后溶液稀释至1L,测得溶液中c(SO42﹣)=1.05mol/L、[H+]=0.1mol/L.反应产生SO2体积(标准状况下)V(SO2)=_____ L,V(H2)=_____ L。
(3)将(1)中产生的气体缓缓通入100MLamol/L NaOH溶液中,SO2、NaOH都完全消耗,则a的取值范围为_____ 。
(1)将13g锌粉投入足量的18.4mol/L的浓硫酸中,充分反应后,所得SO2气体其标况下体积为多少升?
(2)若将一定量的锌投入100mL14.5mol/L的浓硫酸中,反应后锌完全溶解,将反应后溶液稀释至1L,测得溶液中c(SO42﹣)=1.05mol/L、[H+]=0.1mol/L.反应产生SO2体积(标准状况下)V(SO2)=
(3)将(1)中产生的气体缓缓通入100MLamol/L NaOH溶液中,SO2、NaOH都完全消耗,则a的取值范围为
您最近一年使用:0次
【推荐2】硬铝(因其主要成分,在此仅看作Al-Cu合金)常用于建筑装潢。1.18 g某种硬铝恰好与10 mL某浓度的硝酸完全反应,生成的混合气体(其中NO2与NO的体积比为2:1)再与448 mL氧气(标准状况)混合,恰好能被水完全吸收,通过计算并确定此种硬铝的化学式______________
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】能基于物质的量认识物质的组成及其化学变化,是学生必备的学科素养。
(1)已知:①5.6LH2S(标准状况下)②1.204×1023个NH3分子③4.8gCH4④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为__ 。
(2)同浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO 浓度之比为
浓度之比为__ 。
(3)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为dg·cm-3,则形成溶液的物质的量浓度为__ mol·L-1。
(4)某工厂废液中含有K2Cr2O7,排放废液前要将废液中的Cr2O 还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为
还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为__ mol·L-1。
(5)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(N2H4),反应的化学方程式为__ 。
(6)用零价铁(Fe)去除水体中的硝酸盐(NO )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。
实验研究表明,将足量铁粉投入 =2.5的水体中,经24小时测得水体中NO
=2.5的水体中,经24小时测得水体中NO 去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH
去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH ,反应0.1molNO
,反应0.1molNO 恰好消耗16.8gFe,则反应的离子方程式为
恰好消耗16.8gFe,则反应的离子方程式为__ 。
(1)已知:①5.6LH2S(标准状况下)②1.204×1023个NH3分子③4.8gCH4④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为
(2)同浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO
 浓度之比为
浓度之比为(3)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为dg·cm-3,则形成溶液的物质的量浓度为
(4)某工厂废液中含有K2Cr2O7,排放废液前要将废液中的Cr2O
 还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为
还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为(5)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(N2H4),反应的化学方程式为
(6)用零价铁(Fe)去除水体中的硝酸盐(NO
 )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。实验研究表明,将足量铁粉投入
 =2.5的水体中,经24小时测得水体中NO
=2.5的水体中,经24小时测得水体中NO 去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH
去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH ,反应0.1molNO
,反应0.1molNO 恰好消耗16.8gFe,则反应的离子方程式为
恰好消耗16.8gFe,则反应的离子方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】一瓶久置的Na2SO3(杂质只有Na2SO4),为了测定其纯度,取样品5.0 g配成100 mL溶液,取其中25.00 mL于锥形瓶中,用0.10 mol•L-1酸性KMnO4溶液进行滴定,到终点时消耗KMnO4溶液20.00 mL,求此样品的纯度。_______________
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】人工固氮合成氨,并通过氨氧化法制取硝酸的流程如图所示。
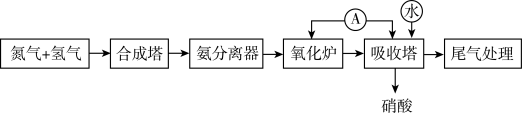
(1)“合成塔”内发生的化学反应中作氧化剂的是_______ (填化学式),金属镁在该氧化剂中燃烧的化学方程式为_______ ,其产物遇水生成的有刺激性气味气体的电子式为_______ ;“氧化炉”中氨气发生反应的化学方程式为_______ 。
(2)常温下,工业上选择铁或铝作盛装浓硝酸的罐体材料的主要原因是_______ 。
(3)为了避免生成硝酸的过程中氮的氧化物污染环境,可用氨气处理尾气,将其转化为大气中含有的无害气体,以处理NO2为例,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)取3.2 g铜与30 mL8 mol/L硝酸充分反应,硝酸的还原产物为NO2和NO,反应后溶液中含有a mol H+,则生成的NO2的物质的量为_______ (用含a的代数式表示,下同)mol,NO的物质的量为_______ mol。

(1)“合成塔”内发生的化学反应中作氧化剂的是
(2)常温下,工业上选择铁或铝作盛装浓硝酸的罐体材料的主要原因是
(3)为了避免生成硝酸的过程中氮的氧化物污染环境,可用氨气处理尾气,将其转化为大气中含有的无害气体,以处理NO2为例,该反应中氧化剂与还原剂的物质的量之比为
(4)取3.2 g铜与30 mL8 mol/L硝酸充分反应,硝酸的还原产物为NO2和NO,反应后溶液中含有a mol H+,则生成的NO2的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】工业上利用氨催化氧化法可制取硝酸,加入脱水剂后制得较高浓度的硝酸。现以17吨氨作为原料,假设NH3全部转化为HNO3。
(1)写出NH3完全转化为HNO3的总化学反应方程式___________________ ;
(2)生产过程中需加水吸收,如果加入脱水剂后脱去水的量相等,则所得硝酸溶液的质量分数为__________ ?
(3)如果生产中同时制得50%的硝酸m1吨和90%的硝酸m2吨(脱去的水可循环使用,制得较低浓度的稀硝酸),若共加入27吨水,则m1与m2的质量比为__________ ?
(1)写出NH3完全转化为HNO3的总化学反应方程式
(2)生产过程中需加水吸收,如果加入脱水剂后脱去水的量相等,则所得硝酸溶液的质量分数为
(3)如果生产中同时制得50%的硝酸m1吨和90%的硝酸m2吨(脱去的水可循环使用,制得较低浓度的稀硝酸),若共加入27吨水,则m1与m2的质量比为
您最近一年使用:0次

 由
由 与
与 组成的混合气体在催化剂作用下于
组成的混合气体在催化剂作用下于 左右可发生反应:
左右可发生反应: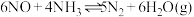 ,达到平衡时在相同条件下气体体积变为
,达到平衡时在相同条件下气体体积变为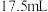 ,计算原混合气体中
,计算原混合气体中

