温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,发生反应:2C(s)+2NO2(g)⇌N2(g)+2CO2(g)反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。下列说法正确的是
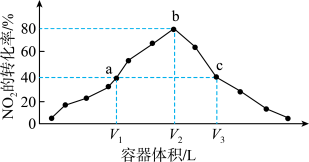

A.T℃时,该反应的化学平衡常数为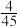 |
| B.图中c点所示条件下,v(正)>v(逆) |
| C.向a点平衡体系中充入一定量的NO2,达到平衡时,NO2的转化率比原平衡大 |
| D.容器内的压强:Pa:Pb>6:7 |
2020·江苏·二模 查看更多[5]
2020年浙江省温州市摇篮杯高一化学竞赛试卷(已下线)专题09 反应速率、化学平衡-2020年高考真题和模拟题化学分项汇编山东省泰安市肥城市2020届高三适应性训练(二)化学试题江苏省南通市2020届高三第二次调研测试化学试题江苏省七市(南通、泰州、扬州、徐州、淮安、连云港、宿迁)2020届高三第二次调研考试化学试题
更新时间:2020-04-04 09:00:39
|
相似题推荐
多选题
|
较难
(0.4)
【推荐1】甲、乙两个密闭容器中均发生反应:C(s)+2H2O(g) CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
下列说法正确的是( )
 CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 平衡 常数 | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2.0 | 4.0 | 3.2 | K1 |
| 乙 | 1 | T2 | 1.0 | 2.0 | 1.2 | K2 |
| A.K1=12.8 |
| B.T1<T2 |
| C.T1℃时向甲容器中再充入0.1 mol H2O(g),则平衡正向移动,CO2(g)的体积分数增大 |
| D.若在T2温度下,向2 L密闭容器中充入1.0 mol CO2和2.0 mol H2,达平衡时,CO2的转化率小于40% |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】温度T1和T2时,分别将1 mol CH4和1.2 mol CO2充入体积为1L的密闭容器中,发生反应:CH4(g)+CO2(g)  2CO(g)+2H2(g),测得有关数据如下表:
2CO(g)+2H2(g),测得有关数据如下表:
下列说法正确的是
 2CO(g)+2H2(g),测得有关数据如下表:
2CO(g)+2H2(g),测得有关数据如下表:| 温度 | 时间/min | 0 | 5 | 10 | 15 | 20 |
| T1 | n(CH4)/mol | 1 | 0.75 | 0.60 | 0.50 | 0.50 |
| T2 | n(CH4)/mol | 1 | 0.65 | 0.45 | …… | 0.40 |
| A.该反应∆H<0 |
| B.T1时0~10min的平均反应速率v(CO)=0.04mol·L-1·min-1 |
| C.保持其他条件不变,T1时向平衡体系中再充入0.5 mol CH4和1 mol H2,重新达平衡前,v(正)<v(逆) |
| D.T 1时,若起始向容器中充入2 mol CH4和2.4 mol CO2,平衡时n(CH4)>1 mol |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
【推荐3】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2 mol A和1 mol B,发生反应:2A(g) + B(g) 2D(g) △H=Q kJ·mol–1。相关条件和数据见下表:
2D(g) △H=Q kJ·mol–1。相关条件和数据见下表:
下列说法正确的是
 2D(g) △H=Q kJ·mol–1。相关条件和数据见下表:
2D(g) △H=Q kJ·mol–1。相关条件和数据见下表:实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/ mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K 2 | K 3 |
| A.K 3>K 2=K 1 |
| B.实验Ⅱ可能使用了催化剂 |
C.实验Ⅲ达平衡后容器内的压强是实验Ⅰ的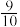 倍 倍 |
| D.实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,平衡不移动 |
您最近半年使用:0次
多选题
|
较难
(0.4)
【推荐1】汽车尾气净化器中发生的反应为2NO(g)+2CO(g) N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
下列说法正确的是
 N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:| 容器 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||||
| NO | CO | N2 | CO2 | N2 | CO2 | ||
| 甲 | 400 | 0.3 | 0.3 | 0 | 0 | 0.2 | |
| 乙 | 400 | 0.6 | 0.6 | 0 | 0 | ||
| 丙 | 500 | 0 | 0 | 0.15 | 0.3 | 0.08 | |
| A.该反应正反应为放热反应 |
| B.达到平衡时,转化率:α(NO,容器甲)+α(N2,容器丙)<1 |
| C.达到平衡时,体系中c(CO)关系:c(CO,容器乙)<2c(CO,容器甲) |
| D.400℃时,若起始时向容器中充入NO、CO、N2、CO2各0.2 mol,开始时v正<v逆 |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】温度T1和T2时,分别将1 mol CH4和1.2 mol CO2充入体积为1L的密闭容器中,发生反应:CH4(g)+CO2(g)  2CO(g)+2H2(g),测得有关数据如下表:
2CO(g)+2H2(g),测得有关数据如下表:
下列说法正确的是
 2CO(g)+2H2(g),测得有关数据如下表:
2CO(g)+2H2(g),测得有关数据如下表:| 温度 | 时间/min | 0 | 5 | 10 | 15 | 20 |
| T1 | n(CH4)/mol | 1 | 0.75 | 0.60 | 0.50 | 0.50 |
| T2 | n(CH4)/mol | 1 | 0.65 | 0.45 | …… | 0.40 |
| A.该反应∆H<0 |
| B.T1时0~10min的平均反应速率v(CO)=0.04mol·L-1·min-1 |
| C.保持其他条件不变,T1时向平衡体系中再充入0.5 mol CH4和1 mol H2,重新达平衡前,v(正)<v(逆) |
| D.T 1时,若起始向容器中充入2 mol CH4和2.4 mol CO2,平衡时n(CH4)>1 mol |
您最近半年使用:0次
多选题
|
较难
(0.4)
【推荐1】科学家发现过渡金属离子可催化消除大气中的N2O和CO污染物,反应原理为CO(g)+N2O(g) CO2(g)+N2(g) ∆H<0。在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1molN2O、0.4molCO和相同催化剂。实验测得A、B容器中N2O的转化率随时间的变化关系如图所示。下列说法正确的是
CO2(g)+N2(g) ∆H<0。在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1molN2O、0.4molCO和相同催化剂。实验测得A、B容器中N2O的转化率随时间的变化关系如图所示。下列说法正确的是

 CO2(g)+N2(g) ∆H<0。在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1molN2O、0.4molCO和相同催化剂。实验测得A、B容器中N2O的转化率随时间的变化关系如图所示。下列说法正确的是
CO2(g)+N2(g) ∆H<0。在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1molN2O、0.4molCO和相同催化剂。实验测得A、B容器中N2O的转化率随时间的变化关系如图所示。下列说法正确的是
| A.A容器中N2O的转化率随时间的变化关系是图中的a曲线 |
| B.要缩短b曲线对应容器达到平衡的时间,但不改变N2O的平衡转化率,可采取的措施为减小容器的体积 |
C.B容器达到化学平衡时,化学平衡常数 |
D.实验测定该反应的反应速率v正=k正·c(N2O)·c(CO),v逆=k逆·c(N2)·c(CO2),k正、k逆分别是正、逆反应速率常数,c为物质的量浓度,则M处的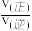 约为1.69 约为1.69 |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
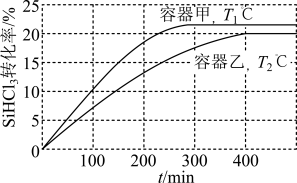
【推荐2】向甲、乙两个恒容密闭容器中分别充入一定量的SiHCl3,发生反应:2SiHCl3(g) SiH2Cl2(g)+SiCl4(g) ΔH=+48kJ·mol−1,维持容器的温度分别为T1℃和T2℃不变,反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
SiH2Cl2(g)+SiCl4(g) ΔH=+48kJ·mol−1,维持容器的温度分别为T1℃和T2℃不变,反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
 SiH2Cl2(g)+SiCl4(g) ΔH=+48kJ·mol−1,维持容器的温度分别为T1℃和T2℃不变,反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
SiH2Cl2(g)+SiCl4(g) ΔH=+48kJ·mol−1,维持容器的温度分别为T1℃和T2℃不变,反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
| A.T1>T2 |
| B.维持温度不变,向平衡后的乙容器中充入一定量的SiHCl3,平衡不移动 |
C.T2℃时,反应的平衡常数:K= |
| D.T1℃时,向甲容器中起始充入0.2molSiHCl3和0.02molSiH2Cl2,SiHCl3的平衡转化率小于10% |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐3】向体积为2 L的恒容密闭容器中充入1 mol SiHCl3发生如下反应: 2SiHCl3(g)  SiH2Cl2(g)+SiCl4(g)下图是不同温度下SiHCl3的物质的量分数随时间的变化:
SiH2Cl2(g)+SiCl4(g)下图是不同温度下SiHCl3的物质的量分数随时间的变化:
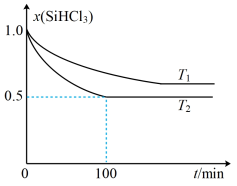
下列说法正确的是
 SiH2Cl2(g)+SiCl4(g)下图是不同温度下SiHCl3的物质的量分数随时间的变化:
SiH2Cl2(g)+SiCl4(g)下图是不同温度下SiHCl3的物质的量分数随时间的变化:
下列说法正确的是
| A.该反应正方向为吸热反应 |
| B.T2时,0~100min时,v(SiCl4)=0.0025 mol·L-1·min-1 |
| C.T2时向平衡体系中再充入1 mol SiHCl3,平衡不移动 |
| D.T1时,起始向容器中充入SiHCl3 、SiH2Cl2、SiCl4各0.3mol,达到平衡前v(正)<v(逆) |
您最近半年使用:0次




