10-11高三·浙江杭州·阶段练习
名校
解题方法
1 . 如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g) Z(g)+2W(g) △H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
Z(g)+2W(g) △H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
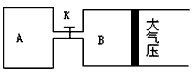
(1)B中X 的转化率α(X)B为_________________________
(2)A中W和B中Z的物质的量的比较: n(W)A_______________ n(Z)B (填<、>、或=)
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为__________________ 升 (用含a的代数式表示,连通管中气体体积不计)
(4)要使B容器恢复原来反应前的体积,可采取的措施是_______________________
 Z(g)+2W(g) △H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
Z(g)+2W(g) △H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
(1)B中X 的转化率α(X)B为
(2)A中W和B中Z的物质的量的比较: n(W)A
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为
(4)要使B容器恢复原来反应前的体积,可采取的措施是
您最近一年使用:0次
2016-12-08更新
|
653次组卷
|
7卷引用:2012届浙江省杭州高级中学高三第三次月考化学试卷
(已下线)2012届浙江省杭州高级中学高三第三次月考化学试卷(已下线)2012届福建省龙岩一中高三第一学段考试化学试卷2015-2016学年江西省九江一中高二上学期第一次月考化学试卷2016-2017学年江西省九江一中高二上第一次月考化学卷安徽师范大学附属中学2017-2018学年高二上学期10月月考化学试题(已下线)【南昌新东方】江西省九江一中2015-2016学年高二上学期第一次月考化学试卷甘肃省会宁县第一中学2020-2021学年高二上学期第一次月考化学试题
名校
2 . 将1 mol X、3 mol Y充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+3Y(g) ⇌ 2Z(g);ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是
| A.升高温度,X的体积分数减小 |
| B.缩小体积,Y的物质的量浓度不变 |
| C.保持容器体积不变,充入一定量的稀有气体,Z的浓度不变 |
| D.保持容器体积不变,充入一定量的Z,X的体积分数增大 |
您最近一年使用:0次
2016-12-08更新
|
205次组卷
|
4卷引用:2016-2017学年湖南省醴陵二中、醴陵四中高二上期中化学卷
名校
解题方法
3 . 一定条件下存在反应:H2(g) + I2(g)  2HI(g) ΔH<0,现有三个相同的体积均为 1 L 的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入 1 mol H2和 1 molI2(g),在Ⅱ中充入 2 molHI(g),在Ⅲ中充入 2 mol H2和2 mol I2 (g),700℃条件下开始反应。达到平衡时,下列说法正确的是
2HI(g) ΔH<0,现有三个相同的体积均为 1 L 的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入 1 mol H2和 1 molI2(g),在Ⅱ中充入 2 molHI(g),在Ⅲ中充入 2 mol H2和2 mol I2 (g),700℃条件下开始反应。达到平衡时,下列说法正确的是
 2HI(g) ΔH<0,现有三个相同的体积均为 1 L 的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入 1 mol H2和 1 molI2(g),在Ⅱ中充入 2 molHI(g),在Ⅲ中充入 2 mol H2和2 mol I2 (g),700℃条件下开始反应。达到平衡时,下列说法正确的是
2HI(g) ΔH<0,现有三个相同的体积均为 1 L 的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入 1 mol H2和 1 molI2(g),在Ⅱ中充入 2 molHI(g),在Ⅲ中充入 2 mol H2和2 mol I2 (g),700℃条件下开始反应。达到平衡时,下列说法正确的是| A.容器Ⅰ、Ⅱ中正反应速率相同 |
| B.容器Ⅰ中反应的平衡常数大于容器Ⅲ中反应的平衡常数 |
| C.容器Ⅱ中的气体颜色比容器Ⅰ中的气体颜色深 |
| D.容器Ⅰ中 H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
您最近一年使用:0次
2016-11-21更新
|
329次组卷
|
6卷引用:2016-2017学年河南省郑州一中高二上期中化学卷
名校
4 . 在密闭容器中发生反应:aX(g)+bY(g) cZ(g)+dW(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述不正确的是( )
cZ(g)+dW(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述不正确的是( )
 cZ(g)+dW(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述不正确的是( )
cZ(g)+dW(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述不正确的是( )| A.平衡向逆反应方向移动 | B.(a+b)< (c+d) |
| C.Z的物质的量浓度变小 | D.X的转化率变小 |
您最近一年使用:0次
2016-05-20更新
|
94次组卷
|
2卷引用:2015-2016学年河北省邢台一中高一下期中化学试卷
5 . 一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
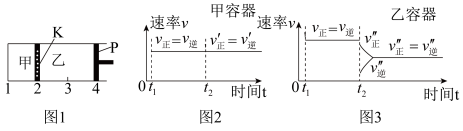
 2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
您最近一年使用:0次
2016-04-25更新
|
3311次组卷
|
12卷引用:2007年普通高等学校招生全国统一考试(江苏卷)化学试题
2007年普通高等学校招生全国统一考试(江苏卷)化学试题2016届浙江省温州市第八高级中学高三上学期期中测试理综化学试卷2015-2016学年河南省信阳高级中学高二12月月考化学卷2015-2016学年江西省抚州市南城一中高二下3月月考化学试卷浙江省宁波市效实中学2015-2016学年高一下期中化学卷2015-2016学年河北省定州中学高二6月月考化学试卷河南省商丘市第一高级中学2017-2018学年高二上学期期中考试化学试题陕西省西安市交通大学附属中学2017-2018学年高二第二次月考期末选修四测试化学试题【全国百强校】河南省信阳市高级中学2018-2019学年高二上学期10月月考化学试题2黑龙江省哈尔滨三中2021届高三上学期期中考试化学试题辽宁省鞍山市岫岩满族自治县高级中学2021-2022学年高三下学期期中质量检测化学试题河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学试题
11-12高三上·辽宁·期中
解题方法
6 . 在恒温、恒容下,发生如下反应:2A(g)+2B(g) C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1和6 mol·L—1,以下叙述正确的是
C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1和6 mol·L—1,以下叙述正确的是
 C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1和6 mol·L—1,以下叙述正确的是
C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1和6 mol·L—1,以下叙述正确的是| A.达到平衡时,途径I的反应速率等于途径Ⅱ的反应速率 |
| B.达到平衡时,途径I所得混合气体的压强等于途径Ⅱ所得混合气体的压强 |
| C.两途径最终达到平衡时,体系内各组分的百分含量相同 |
| D.两途径最终达到平衡时,体系内各组分的百分含量不相同 |
您最近一年使用:0次
2016-03-30更新
|
267次组卷
|
7卷引用:2012届辽宁省辽南协作体高三上学期期中考试化学试卷
14-15高三上·内蒙古赤峰·阶段练习
名校
解题方法
7 . 相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g) 2SO3(g)△H=-197kJ/mol。实验测得起始、平衡时的有关数据如下表:
2SO3(g)△H=-197kJ/mol。实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是
 2SO3(g)△H=-197kJ/mol。实验测得起始、平衡时的有关数据如下表:
2SO3(g)△H=-197kJ/mol。实验测得起始、平衡时的有关数据如下表: | 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A.若在上述条件下反应生成2molSO3(s)的反应热为△H1,则△H1>-197 kJ·mol-1 |
| B.Q1=Q2=Q3=197kJ |
| C.甲、乙、丙3个容器中反应的平衡常数不相等 |
| D.达到平衡时,丙容器中SO2的体积分数最小 |
您最近一年使用:0次
2016-01-16更新
|
124次组卷
|
7卷引用:2015届内蒙古赤峰市宁城县高三上学期摸底统一考试化学试卷
8 . 一定温度下,在三个体积均为1.0 L的恒容密闭容器中发生反应:
下列说法正确的是

| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是
| A.该反应的逆反应为放热反应 |
| B.达到平衡时,容器Ⅰ中的CH3OH体积分数比容器Ⅱ中的小 |
| C.达到平衡时,容器Ⅰ中的压强与容器Ⅲ中的压强相同 |
| D.若起始时向容器Ⅰ中充入CH3OH 0.15 mol、CH3OCH30.15 mol 和H2O 0.10 mol,则反应将向正反应方向进行 |
您最近一年使用:0次
13-14高一下·黑龙江鹤岗·期末
解题方法
9 . 在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通如图所示。容器中发生以下反应:N2+3H2 2NH3(正反应为放热反应)。若反应达平衡后,测得混合气体的体积为7体积,据此回答下列问题:
2NH3(正反应为放热反应)。若反应达平衡后,测得混合气体的体积为7体积,据此回答下列问题:
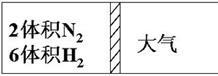
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的体积仍与上述平衡时完全相同,那么:
①若a=1,c=2,则b=____ 。在此情况下,反应起始时将向______ (填“正”或“逆”)反应方向进行。
②若需规定起始时反应向逆反应方向进行,则c的范围是______ 。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是______ ,原因是_____ 。
 2NH3(正反应为放热反应)。若反应达平衡后,测得混合气体的体积为7体积,据此回答下列问题:
2NH3(正反应为放热反应)。若反应达平衡后,测得混合气体的体积为7体积,据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的体积仍与上述平衡时完全相同,那么:
①若a=1,c=2,则b=
②若需规定起始时反应向逆反应方向进行,则c的范围是
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是
您最近一年使用:0次
2015-09-16更新
|
487次组卷
|
4卷引用:2013-2014黑龙江省鹤岗一中高一下学期期末考试化学试卷
(已下线)2013-2014黑龙江省鹤岗一中高一下学期期末考试化学试卷2014-2015学年江西省高安中学高一下学期期末化学试卷2020届福建高三化学总复习——--速率与平衡简答题2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷
名校
10 . 臭氧是理想的烟气脱硝剂,其脱硝反应为2NO2(g)+O3(g) N2O5(g)十O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O5(g)十O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
下列有关说法正确的是
 N2O5(g)十O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O5(g)十O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:| t/s | 0 | 3 | 6 | 12 | 24 |
| n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 |
下列有关说法正确的是
| A.反应在0~3s内的平均速率v(NO2)=0.24 mol·L-1·s-1 |
| B.24 s后,若保持其他条件不变,降低温度,达到新平衡时测得c(O2)=0.44 mol·L-1,则反应的ΔH<0 |
| C.在T温度下,起始时向容器中充入1.0 mol NO2、0.5 mol O3和0.50 mol N2O5、0.50 mol O2,反应达到平衡时,压强为起始时的0.88倍 |
| D.在T温度下,起始时向容器中充入2.0 mol N2O5和2.0 mol O2,达到平衡时,N2O5的转化率大于20% |
您最近一年使用:0次
2015-05-25更新
|
569次组卷
|
5卷引用:2015届江苏省泰州市高三第二次模拟考试化学试卷



