名校
1 . 常温下,用0.1000mol•L﹣1 NaOH溶液滴定20.00mL 0.1000mol•L﹣1 CH3COOH溶液所得滴定曲线如图,下列说法不正确的是
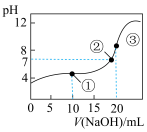

| A.点③溶液显碱性的原因是CH3COO﹣+H2O=CH3COOH+OH﹣ |
| B.点②时溶液中c(Na+)大于c(CH3COO﹣) |
| C.点①溶液中 c(CH3COOH)+c(H+)>c(CH3COO﹣)+c(OH﹣) |
| D.在逐滴加入NaOH溶液至40mL的过程中,水的电离程度先增大后减小 |
您最近一年使用:0次
名校
解题方法
2 . 在科研和工农业生产中,氮、氯、砷(As)、铁、铜等元素形成的单质及其化合物有着广泛的应用。请回答下列问题:
(1)As和N同族,基态砷原子的价层电子排布式为___________ 。
(2) 的空间结构名称为
的空间结构名称为___________ 。
(3)氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,反应原理为:5 +2
+2 +H+=2Mn2++3H2O+5
+H+=2Mn2++3H2O+5 。请回答下列问题:
。请回答下列问题:
①用KMnO4进行滴定时,判断滴定终点的现象是___________ 。
②下列操作会导致测定结果偏低的是___________ (填序号)。
A.酸式滴定管水洗后未用待测液润洗
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定管尖嘴部分有气泡,滴定后消失
D.观察读数时,滴定前仰视,滴定后俯视
③根据下表中测定的实验数据,计算NaHSO3溶液的物质的量浓度__________ (写出计算过程,结果保留4位有效数字)。
(1)As和N同族,基态砷原子的价层电子排布式为
(2)
 的空间结构名称为
的空间结构名称为(3)氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,反应原理为:5
 +2
+2 +H+=2Mn2++3H2O+5
+H+=2Mn2++3H2O+5 。请回答下列问题:
。请回答下列问题:①用KMnO4进行滴定时,判断滴定终点的现象是
②下列操作会导致测定结果偏低的是
A.酸式滴定管水洗后未用待测液润洗
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定管尖嘴部分有气泡,滴定后消失
D.观察读数时,滴定前仰视,滴定后俯视
③根据下表中测定的实验数据,计算NaHSO3溶液的物质的量浓度
| 实验编号 | 待测NaHSO3溶液的体积/mL | KMnO4溶液的体积/mL |
| 1 | 20.00 | 15.98 |
| 2 | 20.00 | 17.00 |
| 3 | 20.00 | 16.02 |
您最近一年使用:0次
名校
解题方法
3 . 某课外兴趣小组用 的NaOH标准溶液滴定未知浓度的盐酸,实验操作如下,请完成以下问题。
的NaOH标准溶液滴定未知浓度的盐酸,实验操作如下,请完成以下问题。
I.首先配制 的氢氧化钠溶液。
的氢氧化钠溶液。
(1)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、______ 、______ 。需要称量NaOH固体的质量为_______ g。
(2)若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”“偏低”或“无影响”)
①容量瓶中原有少量蒸馏水:___________ 。
②转移溶液时,没有洗涤玻璃棒和溶解用的烧杯:___________ 。
③定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线:___________ 。
④定容时,俯视观察液面:___________ 。
Ⅱ.用上述 的NaOH标准溶液滴定未知浓度的盐酸。
的NaOH标准溶液滴定未知浓度的盐酸。
(3)正确操作步骤为A→______ 。
A.分别检查酸式滴定管、碱式滴定管,可以使用,并用水清洗滴定管
B.另取锥形瓶,再重复操作一次
C.分别用蒸馏水洗干净酸式滴定管和碱式滴定管
D.用待测定的盐酸润洗酸式滴定管
E.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
F.碱式滴定管用标准 溶液润洗后,将标准液注入碱式滴定管“0”刻度以上
溶液润洗后,将标准液注入碱式滴定管“0”刻度以上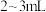 处,再把碱式滴定管固定好,排尽尖嘴部分的气泡,并调节液面至“0”刻度或“0”刻度以下
处,再把碱式滴定管固定好,排尽尖嘴部分的气泡,并调节液面至“0”刻度或“0”刻度以下
G.用酸式滴定管量取盐酸 ,注入事先洗干净的锥形瓶中,加入指示剂
,注入事先洗干净的锥形瓶中,加入指示剂
(4)滴定实验所需的玻璃仪器有______ (填字母)。
A.酸式滴定管 B.碱式滴定管 C.量筒 D.锥形瓶 E.铁架台 F.滴定管夹 G.烧杯 H.白纸
(5)该小组同学选用酚酞作为指示剂,滴定终点的现象为______ 。
(6)有学生在滴定过程中出现下列操作,会导致测定结果偏小的是_______ 。
①酸式滴定管用蒸馏水洗净后未用待装液润洗
②锥形瓶用蒸馏水洗净后再用待测液润洗
③滴定时摇晃锥形瓶将液体溅出瓶外
④读取标准溶液体积时,滴定前俯视,滴定后仰视
(7)该小组学生某3次实验的有关数据分别记录如表:
依据表中数据计算该盐酸的物质的量浓度为_____ 。
 的NaOH标准溶液滴定未知浓度的盐酸,实验操作如下,请完成以下问题。
的NaOH标准溶液滴定未知浓度的盐酸,实验操作如下,请完成以下问题。I.首先配制
 的氢氧化钠溶液。
的氢氧化钠溶液。(1)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、
(2)若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”“偏低”或“无影响”)
①容量瓶中原有少量蒸馏水:
②转移溶液时,没有洗涤玻璃棒和溶解用的烧杯:
③定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线:
④定容时,俯视观察液面:
Ⅱ.用上述
 的NaOH标准溶液滴定未知浓度的盐酸。
的NaOH标准溶液滴定未知浓度的盐酸。(3)正确操作步骤为A→
A.分别检查酸式滴定管、碱式滴定管,可以使用,并用水清洗滴定管
B.另取锥形瓶,再重复操作一次
C.分别用蒸馏水洗干净酸式滴定管和碱式滴定管
D.用待测定的盐酸润洗酸式滴定管
E.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
F.碱式滴定管用标准
 溶液润洗后,将标准液注入碱式滴定管“0”刻度以上
溶液润洗后,将标准液注入碱式滴定管“0”刻度以上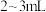 处,再把碱式滴定管固定好,排尽尖嘴部分的气泡,并调节液面至“0”刻度或“0”刻度以下
处,再把碱式滴定管固定好,排尽尖嘴部分的气泡,并调节液面至“0”刻度或“0”刻度以下G.用酸式滴定管量取盐酸
 ,注入事先洗干净的锥形瓶中,加入指示剂
,注入事先洗干净的锥形瓶中,加入指示剂(4)滴定实验所需的玻璃仪器有
A.酸式滴定管 B.碱式滴定管 C.量筒 D.锥形瓶 E.铁架台 F.滴定管夹 G.烧杯 H.白纸
(5)该小组同学选用酚酞作为指示剂,滴定终点的现象为
(6)有学生在滴定过程中出现下列操作,会导致测定结果偏小的是
①酸式滴定管用蒸馏水洗净后未用待装液润洗
②锥形瓶用蒸馏水洗净后再用待测液润洗
③滴定时摇晃锥形瓶将液体溅出瓶外
④读取标准溶液体积时,滴定前俯视,滴定后仰视
(7)该小组学生某3次实验的有关数据分别记录如表:
| 滴定次数 | 待测盐酸的体积/mL |  NaOH溶液的体积/mL NaOH溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 2.00 | 27.91 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
您最近一年使用:0次
名校
解题方法
4 . 室温下,向 的溶液中滴加几滴甲基橙,此时溶液呈
的溶液中滴加几滴甲基橙,此时溶液呈
 的溶液中滴加几滴甲基橙,此时溶液呈
的溶液中滴加几滴甲基橙,此时溶液呈| A.红色 | B.黄色 | C.橙色 | D.紫色 |
您最近一年使用:0次
名校
解题方法
5 . 某学生用0.1000mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.调节液面至“0”或“0”以下某一刻度,记下读数
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.用标准溶液润洗滴定管2~3次
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)A→___________ →F;
(2)若无上述E步骤操作,则测定结果会_______ (填“偏高”、“偏低”或“无影响”,下同);
(3)上述A步骤之前,若先用待测液润洗锥形瓶,则对滴定结果的影响是_______ 。
(4)判断到达滴定终点的现象是________ 。
(5)若甲学生在实验过程中,记录滴定前滴定管内液面读数为2.60ml,滴定后液面如图,则此时消耗标准溶液的体积为______ mL。

(6)乙学生做了三组平行实验,数据记录如下:选取下述合理数据,计算出待测溶液的物质的量浓度为________ ; 保留四位有效数字
保留四位有效数字
A.移取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.调节液面至“0”或“0”以下某一刻度,记下读数
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.用标准溶液润洗滴定管2~3次
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)A→
(2)若无上述E步骤操作,则测定结果会
(3)上述A步骤之前,若先用待测液润洗锥形瓶,则对滴定结果的影响是
(4)判断到达滴定终点的现象是
(5)若甲学生在实验过程中,记录滴定前滴定管内液面读数为2.60ml,滴定后液面如图,则此时消耗标准溶液的体积为

(6)乙学生做了三组平行实验,数据记录如下:选取下述合理数据,计算出待测溶液的物质的量浓度为
 保留四位有效数字
保留四位有效数字
| 实验序号 | 待测HCl溶液的体积 | 0.1000mol·L-1的KOH溶液的体积 | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 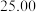 |  | 25.33 |
| 2 | 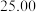 | 0.00 | 30.00 |
| 3 | 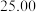 |  | 25.67 |
您最近一年使用:0次
解题方法
6 . 氯碱厂质检人员用滴定法测定某NaOH溶液的浓度。
(1)洗涤滴定管前必须首先________ 。
(2)选用盐酸作为标准溶液进行测定实验。将盐酸装入______ ,NaOH溶液装入______ ,滴加______ 作指示剂。滴定时,眼睛注视________ ,当锥形瓶内______ 即达滴定终点。记录此时滴定管内液面读数V(末)。
(3)实验数据记录及处理:标准盐酸浓度:0.1054mol/L
若NaOH溶液的准确浓度为 0.1005mol/L,实验误差是_______ %。
(4)若测定结果偏低,原因可能是________。
(1)洗涤滴定管前必须首先
(2)选用盐酸作为标准溶液进行测定实验。将盐酸装入
(3)实验数据记录及处理:标准盐酸浓度:0.1054mol/L
| 实验次数 | 待测氢氧化钠溶液体积(mL) | 标准盐酸体积(mL) | NaOH溶液浓度(mol/L) | ||
| 初读数 | 末读数 | 体积 | |||
| 1 | 20.00 | 0.50 | 20.70 | | |
| 2 | 20.00 | 6.00 | 26.00 | | |
(4)若测定结果偏低,原因可能是________。
| A.见到指示剂的颜色有变化就停止滴定 |
| B.锥形瓶用蒸馏水清洗后,未用待装液润洗 |
| C.读数时,若滴定前视线偏低,滴定后视线偏高 |
| D.滴定前滴定管的尖嘴部分充满液体,滴定终点时尖嘴部分有气泡 |
您最近一年使用:0次
解题方法
7 . 用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列操作会导致测定结果偏低的是
| A.酸式滴定管未润洗就装标准液滴定 |
| B.锥形瓶未用待测液润洗 |
| C.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失 |
| D.读取标准液读数时,滴前仰视,滴定到终点后俯视 |
您最近一年使用:0次
名校
解题方法
8 . 如图是用 的盐酸滴定某未知浓度的NaOH溶液的示意图。
的盐酸滴定某未知浓度的NaOH溶液的示意图。

请回答下列问题:
(1)仪器A的名称是___________ 。
(2)某学生的操作步骤如下:
A.移取20.00mL待测NaOH溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的酸式滴定管固定好,调节滴定管使尖嘴部分充满溶液;调节液面至“0”或“0”以下刻度,记下读数;
D.取标准盐酸溶液注入酸式滴定管至“0”刻度以上23mL;
E.把锥形瓶放在滴定管的下面,用标准盐酸溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是___________ (用字母序号填写)。上述B步骤操作的目的是___________ 。判断到达滴定终点的实验现象是___________ 。
(3)如图为某次滴定前、后盛放盐酸的滴定管中液面的位置。
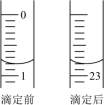
盐酸的体积读数:滴定前读数为___________ mL,滴定后读数为___________ mL。
(4)某实验小组同学的三次实验的实验数据如下表所示,根据表中数据计算出的待测NaOH溶液的平均浓度是___________  。
。
(5)对下列几种假定情况进行讨论:
①盛标准溶液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失,对测定结果的影响是___________ (填“偏高”“偏低”或“无影响”,下同);
②若滴定前锥形瓶未用待测液润洗,对测定结果的影响是___________ ;
③标准液读数时,若滴定前俯视,滴定后仰视,对测定结果的影响是___________ 。
 的盐酸滴定某未知浓度的NaOH溶液的示意图。
的盐酸滴定某未知浓度的NaOH溶液的示意图。
请回答下列问题:
(1)仪器A的名称是
(2)某学生的操作步骤如下:
A.移取20.00mL待测NaOH溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的酸式滴定管固定好,调节滴定管使尖嘴部分充满溶液;调节液面至“0”或“0”以下刻度,记下读数;
D.取标准盐酸溶液注入酸式滴定管至“0”刻度以上23mL;
E.把锥形瓶放在滴定管的下面,用标准盐酸溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是
(3)如图为某次滴定前、后盛放盐酸的滴定管中液面的位置。

盐酸的体积读数:滴定前读数为
(4)某实验小组同学的三次实验的实验数据如下表所示,根据表中数据计算出的待测NaOH溶液的平均浓度是
 。
。| 实验编号 | 待测NaOH溶液的体积/mL | 滴定前盐酸的体积读数/mL | 滴定后盐酸的体积读数/mL |
| 1 | 20.00 | 1.20 | 23.22 |
| 2 | 20.00 | 1.21 | 29.21 |
| 3 | 20.00 | 1.50 | 23.48 |
①盛标准溶液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失,对测定结果的影响是
②若滴定前锥形瓶未用待测液润洗,对测定结果的影响是
③标准液读数时,若滴定前俯视,滴定后仰视,对测定结果的影响是
您最近一年使用:0次
名校
解题方法
9 . I.某学生用0.1mol/L的盐酸标准溶液测未知浓度的NaOH,其操作分解为如下几步:
A.移取20mL待测NaOH溶液注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准盐酸溶液注入酸式滴定管至0刻度以上2~3cm
E.调节液面至0或0以下刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准盐酸溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是_________ (用序号字母填写);
B→___________→C→E→___________→F
(2)用0.1mol/L盐酸的标准溶液测未知浓度的NaOH,滴定时左手控制活塞,两眼注视___________ 内溶液颜色的变化,直到滴定终点。
(3)判断到达滴定终点的实验现象是:滴加最后一滴标准液,溶液由___________ ,且半分钟内不变色。
II.室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol/LHA溶液中逐滴加入0.1000mol/L的标准KOH溶液,其pH变化曲线如图所示 忽略温度变化
忽略温度变化 。请回答下列有关问题:
。请回答下列有关问题:

(4)a、b、c、d四点中水的电离程度最大的是___________ 点。
(5)滴定过程中部分操作如下,下列各操作使测量结果偏高的是___________ 填字母序号
填字母序号 。
。
(6)若重复三次滴定实验的数据如表所示,计算滴定所测HA溶液的物质的量浓度为___________ mol/L。(保留4位有效数字)
A.移取20mL待测NaOH溶液注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准盐酸溶液注入酸式滴定管至0刻度以上2~3cm
E.调节液面至0或0以下刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准盐酸溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是
B→___________→C→E→___________→F
(2)用0.1mol/L盐酸的标准溶液测未知浓度的NaOH,滴定时左手控制活塞,两眼注视
(3)判断到达滴定终点的实验现象是:滴加最后一滴标准液,溶液由
II.室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol/LHA溶液中逐滴加入0.1000mol/L的标准KOH溶液,其pH变化曲线如图所示
 忽略温度变化
忽略温度变化 。请回答下列有关问题:
。请回答下列有关问题:
(4)a、b、c、d四点中水的电离程度最大的是
(5)滴定过程中部分操作如下,下列各操作使测量结果偏高的是___________
 填字母序号
填字母序号 。
。| A.滴定前碱式滴定管未用标准KOH溶液润洗 |
| B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定 |
| C.滴定过程中,溶液刚出现变色,立即停止滴定 |
| D.滴定结束后,仰视液面,读取KOH溶液体积 |
(6)若重复三次滴定实验的数据如表所示,计算滴定所测HA溶液的物质的量浓度为
| 实验序号 | KOH溶液体积/mL | 待测HA溶液体积/mL |
| 1 | 21.01 | 20.00 |
| 2 | 20.99 | 20.00 |
| 3 | 21.60 | 20.00 |
您最近一年使用:0次
名校
解题方法
10 . 如图是用0.1000mol⋅L−1的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前后盛放盐酸的滴定管中液面的位置。
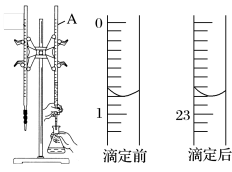
请回答下列问题:
(1)仪器A的名称是___________ 。
(2)盐酸的体积读数:滴定前读数为___________ mL,滴定后读数___________ mL
(3)某实验小组同学的三次实验的实验数据如下表所示。根据表中数据计算出待测NaOH溶液的平均浓度是___________ mol⋅L−1(保留四位有效数字)
(4)对下列几种假定情况进行讨论(填“无影响”“偏高”或“偏低”):
①量取待测液的滴定管,放出溶液前滴定管尖端有气泡,放出溶液后气泡消失,对测定结果的影响是___________ ;
②若滴定前锥形瓶未用待测液润洗,对测定结果的影响是___________ ;
③用湿润的pH试纸测稀硫酸溶液的pH,对测定结果的影响是___________ 。

请回答下列问题:
(1)仪器A的名称是
(2)盐酸的体积读数:滴定前读数为
(3)某实验小组同学的三次实验的实验数据如下表所示。根据表中数据计算出待测NaOH溶液的平均浓度是
| 实验编号 | 待测NaOH溶液的体积/mL | 滴定前盐酸的体积读数/mL | 滴定后盐酸的体积读数/mL |
| 1 | 20.00 | 1.20 | 23.22 |
| 2 | 20.00 | 1.21 | 29.21 |
| 3 | 20.00 | 1.50 | 23.48 |
(4)对下列几种假定情况进行讨论(填“无影响”“偏高”或“偏低”):
①量取待测液的滴定管,放出溶液前滴定管尖端有气泡,放出溶液后气泡消失,对测定结果的影响是
②若滴定前锥形瓶未用待测液润洗,对测定结果的影响是
③用湿润的pH试纸测稀硫酸溶液的pH,对测定结果的影响是
您最近一年使用:0次



