解题方法
1 . 电解质的水溶液中存在电离平衡。
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为_______ 。
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)________ 。
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。_______ 。
②滴定醋酸的曲线是_______ (填“I”或“Ⅱ”),则V1______ V2(填“>”、 “<”“或“=”)。
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为_____ mL。 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①该滴定过程应选择______ (填“甲基橙”或“酚酞”)为指示剂,根据上述数据,可计算出该醋酸的浓度约为_____  。
。
②在上述实验中,下列操作会造成测定结果偏大的有______ 。(填字母序号)。
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为
 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。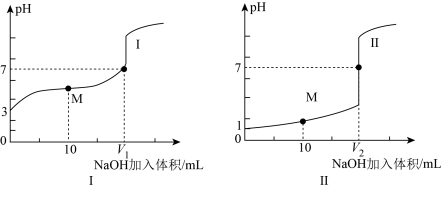
②滴定醋酸的曲线是
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为

 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。| 实验编号 | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测醋酸的体积(mL) |
| 1 | 0.1000 | 22.48 | 20.00 |
| 2 | 0.1000 | 25.72 | 20.00 |
| 3 | 0.1000 | 22.52 | 20.00 |
 。
。②在上述实验中,下列操作会造成测定结果偏大的有
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近半年使用:0次
解题方法
2 . 用0.1000mol/L的CH3COOH溶液滴定20.00mL某浓度的NaOH溶液,重复3次的实验数据如下表所示,下列说法正确的是
| 实验编号 | 待测NaOH溶液的体积/mL | 滴定前醋酸的体积读数/mL | 滴定后醋酸的体积读数/mL |
| 1 | 20.00 | 0.36 | 24.26 |
| 2 | 20.00 | 0.25 | 29.69 |
| 3 | 20.00 | 0.48 | 24.58 |
| A.将酸式滴定管用蒸馏水洗净后,立即向其中注入CH3COOH溶液 |
| B.滴定过程中不小心将CH3COOH溶液滴到锥形瓶外,会导致测定结果偏低 |
| C.为了尽可能减小误差,应选择酚䣭作为指示剂 |
| D.待测NaOH溶液的浓度为0.1300mol/L |
您最近半年使用:0次
解题方法
3 . 关于下列各实验或装置的叙述中,不正确的是


| A.①可用于测溶液pH |
| B.②是用酸性KMnO4溶液滴定Na2SO3溶液 |
| C.③是滴定操作时手的操作 |
| D.④中滴入最后半滴NaOH标准液使溶液由无色变为红色,即达到滴定终点 |
您最近半年使用:0次
名校
解题方法
4 . 滴定法是一种常见的定量实验分析方法,常见的有酸碱中和滴定法、氧化还原滴定法、沉淀滴定法等。常温下,用 的NaOH溶液滴定20.00mL
的NaOH溶液滴定20.00mL 醋酸
醋酸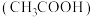 ,滴定曲线如图1所示。
,滴定曲线如图1所示。

1.在上述滴定过程中,不需要使用的玻璃仪器是 。
2.滴定过程中眼睛应注视_____ 。该实验使用的指示剂为_____ ,滴定终点的现象为_____ 。某次实验滴定终点时滴定管中液面位置如图2所示,则此时的读数为_____ mL。
3.如图1所示,c点的纵坐标为7,d点的横坐标为20.00mL,a、b、c、d四个点对应溶液中,_____ 点对应水的电离程度最大,c点溶液中,
_____  (填“>”“<”或“=”)
(填“>”“<”或“=”)
 的NaOH溶液滴定20.00mL
的NaOH溶液滴定20.00mL 醋酸
醋酸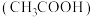 ,滴定曲线如图1所示。
,滴定曲线如图1所示。
1.在上述滴定过程中,不需要使用的玻璃仪器是 。
| A.移液管 | B.滴定管 | C.锥形瓶 | D.胶头滴管 |
3.如图1所示,c点的纵坐标为7,d点的横坐标为20.00mL,a、b、c、d四个点对应溶液中,

 (填“>”“<”或“=”)
(填“>”“<”或“=”)
您最近半年使用:0次
5 . 下列实验操作或装置能达到实验目的的是
| 选项 | A | B | D | |
| 实验操作与装置 | 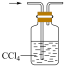 | 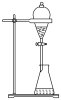 | 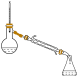 | 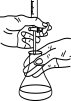 |
| 实验目的 | 除去HCl气体中的Cl2 | 苯萃取溴水中溴并从下口放出溴的苯溶液 | 实验室纯化工业乙酸乙酯 | 用标准高锰酸钾溶液测定盐酸酸化的FeCl2溶液中Fe2+的含量 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 用标准盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是
| A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 |
| B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定 |
| C.用蒸馏水洗净锥形瓶后,装入20.00mLNaOH溶液,加入少量的蒸馏水再进行滴定 |
| D.用酚酞作指示剂滴至红色刚变无色时,立即停止加盐酸并读数 |
您最近半年使用:0次
解题方法
7 . 某学生用碱式滴定管量取0.1mol/l的NaOH溶液,开始时仰视液面读数为2.10mL,取出部分溶液后,俯视液面,读数为12.10mL,该同学在操作中实际取出的液体体积为
| A.大于10.00mL | B.小于10.00mL | C.等于10.00mL | D.等于11.00mL |
您最近半年使用:0次
解题方法
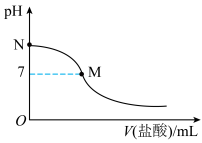
8 . 常温下,向25.00mL0.10mol·L-1氨水中滴入 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知 氨水的电离度为1.32%,下列有关叙述正确的是
氨水的电离度为1.32%,下列有关叙述正确的是
 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知 氨水的电离度为1.32%,下列有关叙述正确的是
氨水的电离度为1.32%,下列有关叙述正确的是
| A.用量筒量取25.00mL0.10mol·L-1 氨水 |
| B.可根据该反应过程中放出的热量计算中和反应反应热 |
C.M点对应的盐酸体积为 |
D.N点处的溶液中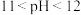 |
您最近半年使用:0次
名校
解题方法
9 . 用标准盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是
| A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 |
| B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定 |
| C.将NaOH溶液放入用蒸馏水洗净的锥形瓶中,加入少量的蒸馏水后进行滴定 |
| D.用酚酞作指示剂滴至红色刚变无色时即停止加盐酸 |
您最近半年使用:0次
10 . 回答下列问题。
(1)醋酸是常见的弱酸。
 醋酸在水溶液中的电离方程式为
醋酸在水溶液中的电离方程式为 ___________ 。
 下列方法中,可以使醋酸稀溶液中
下列方法中,可以使醋酸稀溶液中 电离程度增大的是
电离程度增大的是___________  填字母序号
填字母序号 。
。
a.滴加少量浓盐酸 b.微热溶液 c.加水稀释 d.加入少量醋酸钠晶体
(2)用 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。

 滴定醋酸的曲线是
滴定醋酸的曲线是___________  填“
填“ ”或“Ⅱ”
”或“Ⅱ” 。
。
 滴定开始前,三种溶液中由水电离出的
滴定开始前,三种溶液中由水电离出的 最大的是
最大的是___________ 。
 上述用
上述用 的
的 溶液滴定
溶液滴定 的盐酸,下列操作不正确的是
的盐酸,下列操作不正确的是___________ 。
A.用标准 溶液润洗碱式滴定管后,再装入标准碱溶液
溶液润洗碱式滴定管后,再装入标准碱溶液
B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
(1)醋酸是常见的弱酸。
 醋酸在水溶液中的电离方程式为
醋酸在水溶液中的电离方程式为  下列方法中,可以使醋酸稀溶液中
下列方法中,可以使醋酸稀溶液中 电离程度增大的是
电离程度增大的是 填字母序号
填字母序号 。
。a.滴加少量浓盐酸 b.微热溶液 c.加水稀释 d.加入少量醋酸钠晶体
(2)用
 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。
 滴定醋酸的曲线是
滴定醋酸的曲线是 填“
填“ ”或“Ⅱ”
”或“Ⅱ” 。
。 滴定开始前,三种溶液中由水电离出的
滴定开始前,三种溶液中由水电离出的 最大的是
最大的是 上述用
上述用 的
的 溶液滴定
溶液滴定 的盐酸,下列操作不正确的是
的盐酸,下列操作不正确的是A.用标准
 溶液润洗碱式滴定管后,再装入标准碱溶液
溶液润洗碱式滴定管后,再装入标准碱溶液B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
您最近半年使用:0次



