名校
解题方法
1 .  的盐酸溶液能吸收CO生成配合物氯化羰基亚铜
的盐酸溶液能吸收CO生成配合物氯化羰基亚铜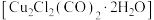 ,其结构如图:
,其结构如图:

下列有关氯化羰基亚铜的说法不正确 的是
 的盐酸溶液能吸收CO生成配合物氯化羰基亚铜
的盐酸溶液能吸收CO生成配合物氯化羰基亚铜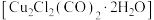 ,其结构如图:
,其结构如图:
下列有关氯化羰基亚铜的说法
A.该配合物中Cl离子的杂化方式为 杂化 杂化 |
B.该配合物的配体有CO、 、 、 ,其中CO提供孤电子对的为O原子 ,其中CO提供孤电子对的为O原子 |
C.该配合物中, 提供空轨道接受孤电子对形成配位键 提供空轨道接受孤电子对形成配位键 |
| D.该配合物中,中心离子的配位数为4 |
您最近半年使用:0次
名校
解题方法
2 . 下列有关原子结构和元素性质的叙述中,正确的是
| A.邻羟基苯甲醛的熔点高于对羟基苯甲醛的熔点 |
| B.第四周期元素中,基态锰原子价电子层中未成对电子数最多 |
| C.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 |
D.价层电子对互斥理论中, 键电子对数不计入中心原子的价层电子对数 键电子对数不计入中心原子的价层电子对数 |
您最近半年使用:0次
2023-09-15更新
|
143次组卷
|
2卷引用:四川省南充高级中学2022-2023学年高二上学期1月期末考试化学试题
解题方法
3 . 下列关于C,Si及其化合物结构与性质的论述错误的是
A.自然界中的14C来自宇宙射线(中子)撞击14N,其过程可表示为 |
| B.SiH4中Si的化合价为+4,CH4中C的化合价为-4,因此SiH4还原性小于CH4 |
| C.高压下制得的CO2共价晶体结构与SiO2晶体相似,其硬度和熔沸点均高于SiO2晶体 |
| D.Si原子问难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成p-pπ键 |
您最近半年使用:0次
4 . 纳米TiO2是一种重要的光催化剂,其催化苯甲胺(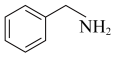 )生成苯甲亚胺(
)生成苯甲亚胺(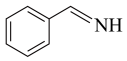 )的机理如图所示。下列说法不正确的是
)的机理如图所示。下列说法不正确的是
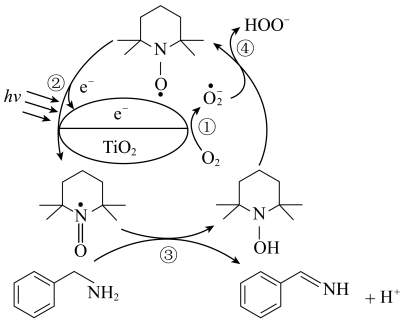
 )生成苯甲亚胺(
)生成苯甲亚胺( )的机理如图所示。下列说法不正确的是
)的机理如图所示。下列说法不正确的是
| A.HOO-具有氧化性 |
| B.O2在TiO2表面捕获电子 |
| C.反应③涉及π键的断裂和生成 |
D.总反应为2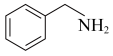 +O2→2 +O2→2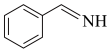 +2H2O +2H2O |
您最近半年使用:0次
2023-09-14更新
|
175次组卷
|
2卷引用:广东省广州市2024届高三上学期9月阶段训练化学试题
解题方法
5 . 陈述I和II均正确,且具有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | 电负性:F>Cl | 酸性:CF3COOH<CCl3COOH |
| B | 离子半径:r(Mg2+)<r(Ca2+) | 熔点:MgO>CaO |
| C | 分子极性:CO>N2 | 范德华力:CO<N2 |
| D | 分子间作用力:H2O>H2S | 稳定性:H2O>H2S |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示。该反应能够有效脱除烟气中的NO。下列说法正确的是
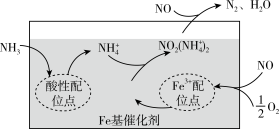

A.在酸性配位点上,NH3与H+通过离子键形成 |
| B.增大压强有利于NO与O2吸附在Fe3+配位点上形成NO2 |
| C.反应物NH3和生成物H2O的杂化类型分别为sp3、sp2 |
| D.催化剂表面发生的总反应为4NH3+6NO=5N2+6H2O |
您最近半年使用:0次
7 . 由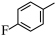 经两步反应合成
经两步反应合成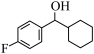 的步骤如下:
的步骤如下:
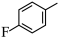
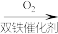
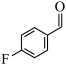
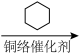
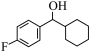
完成下列问题:
(1)上述有机物涉及的3种第二周期元素,其电负性由小到大排序依次是___________ 。
(2)用“*”标记出下图分子中的手性碳原子________ 。
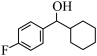
(3)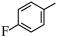 的分子式是
的分子式是___________ ,其中碳原子的杂化类型是___________ ,分子中有___________ 个原子参与形成离域键。
(4)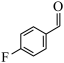 转化为
转化为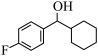 的过程中,C=O键中的
的过程中,C=O键中的___________ (填“σ”或“π”)键断裂,所属的有机反应基本类型是___________ 反应。
 经两步反应合成
经两步反应合成 的步骤如下:
的步骤如下:
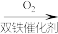



完成下列问题:
(1)上述有机物涉及的3种第二周期元素,其电负性由小到大排序依次是
(2)用“*”标记出下图分子中的手性碳原子

(3)
 的分子式是
的分子式是(4)
 转化为
转化为 的过程中,C=O键中的
的过程中,C=O键中的
您最近半年使用:0次
2023-09-10更新
|
241次组卷
|
2卷引用:上海市格致中学2023-2024学年高三上学期9月(等级考)化学试题
解题方法
8 . 我国某科学团队利用二维氮化硼陶瓷片在特定方向上具有超高热导的性质造出一款新型热界面材料。以天然硼砂为起始物,可制备得到 和
和 ,如图所示。下列叙述错误的是
,如图所示。下列叙述错误的是
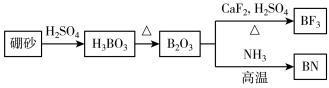
 和
和 ,如图所示。下列叙述错误的是
,如图所示。下列叙述错误的是
| A.硼酸分子间存在氢键 |
B. 与 与 都具有极性键,但前者为极性分子后者为非极性分子 都具有极性键,但前者为极性分子后者为非极性分子 |
C.平面二维氮化硼 中, 中,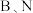 都为 都为 杂化 杂化 |
D. 分子与 分子与 分子的键角,后者大于前者 分子的键角,后者大于前者 |
您最近半年使用:0次
名校
解题方法
9 . 金粉溶于过氧化氢-浓盐酸可以安全环保的制备氯金酸(H[AuCl4]),其化学方程式为: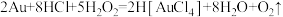 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
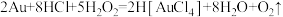 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.消耗1 mol Au,反应转移的电子数为4NA |
| B.100 mL质量分数为36.5%、密度为1.19 g/cm3的盐酸中所含HCl的分子数为1.19NA |
| C.消耗85 g H2O2,产物中形成的配位键数目为2NA |
| D.2 mol液态水中含有的氢键数目为4NA |
您最近半年使用:0次
解题方法
10 . 某抗癌药物的分子结构如图所示,其中W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y同主族、Y、Z的最外层电子数之和是X的最外层电子数的2倍。下列叙述正确的是
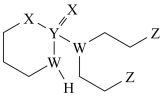

A.电负性: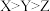 | B.简单氢化物的沸点: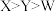 |
C.简单氢化物分子的键角: | D.氧化物对应的水化物的酸性: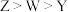 |
您最近半年使用:0次



