名校
解题方法
1 . CH4、NH3和N2H4均可作为燃料电池的燃料。下列说法错误的是
| A.CH4、NH3和 N2H4中C、N杂化方式均相同 |
| B.CH4、NH3和N2H4均为极性分子 |
| C.CH4和 NH3的空间结构分别为正四面体形、三角锥形 |
D.沸点: 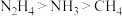 |
您最近半年使用:0次
解题方法
2 . 随着科学技术的发展,锂电池已经成为了主流。某电解质阴离子(如下图)在锂电工业中广泛应用,其组成元素X、Y、Z、R、W均为短周期主族元素,原子序数依次增大且X、Y、Z、R位于同周期。下列叙述不正确的是
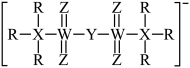
| A.简单氢化物的沸点:Z>Y>X |
| B.气态氢化物稳定性:R>Z>W |
| C.WF4、WF6分子中每个原子都达到8电子结构 |
| D.最高价氧化物对应的水化物酸性:Y>X |
您最近半年使用:0次
解题方法
3 . 锂离子电池是新能源重要组成部分,锂离子电池的回收利用日渐成为化学工作者的重要研究课题。某研究组利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺流程如下:
进行氯化处理以回收Li、Co等金属,工艺流程如下: ,
,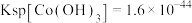 。
。
回答下列问题:
(1)基态Co原子的价层电子排布式是___________ 。
(2)“烧渣”是LiCl、 和
和 的混合物,请写出“500℃焙烧”的化学方程式
的混合物,请写出“500℃焙烧”的化学方程式___________ 。
(3)“500℃焙烧”后剩余的 应先除去,否则水浸时会因其水解产生大量烟雾。试从物质结构的角度解释
应先除去,否则水浸时会因其水解产生大量烟雾。试从物质结构的角度解释 比
比 易水解的原因
易水解的原因___________ 。
(4)若“滤液2”中 浓度为:
浓度为: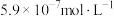 ,“沉钴”时应控制pH为
,“沉钴”时应控制pH为___________ 。
(5)“沉锂”步骤的“试剂A”的化学式为___________ 。
(6)将“滤饼2”在通入充足空气后,进行850℃煅烧才能得到 。写出该过程的化学方程式
。写出该过程的化学方程式___________ 。
(7)钴酸锂(LiCoO2)的一种晶胞如图所示(仅标出Li,Co与O未标出),晶胞中含有 的个数为
的个数为___________ 。
 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺流程如下:
进行氯化处理以回收Li、Co等金属,工艺流程如下: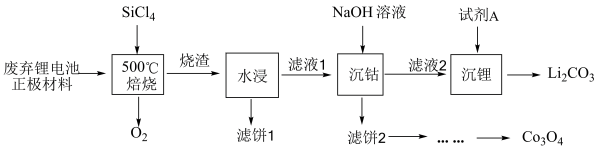
 ,
,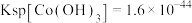 。
。回答下列问题:
(1)基态Co原子的价层电子排布式是
(2)“烧渣”是LiCl、
 和
和 的混合物,请写出“500℃焙烧”的化学方程式
的混合物,请写出“500℃焙烧”的化学方程式(3)“500℃焙烧”后剩余的
 应先除去,否则水浸时会因其水解产生大量烟雾。试从物质结构的角度解释
应先除去,否则水浸时会因其水解产生大量烟雾。试从物质结构的角度解释 比
比 易水解的原因
易水解的原因(4)若“滤液2”中
 浓度为:
浓度为: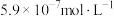 ,“沉钴”时应控制pH为
,“沉钴”时应控制pH为(5)“沉锂”步骤的“试剂A”的化学式为
(6)将“滤饼2”在通入充足空气后,进行850℃煅烧才能得到
 。写出该过程的化学方程式
。写出该过程的化学方程式(7)钴酸锂(LiCoO2)的一种晶胞如图所示(仅标出Li,Co与O未标出),晶胞中含有
 的个数为
的个数为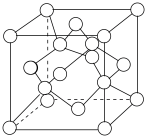
您最近半年使用:0次
4 . I.按构成晶体的粒子和粒子间作用力的不同,将以下晶体进行分类:
①氯化钡、②石英、③金刚砂、④水、⑤乙醇、⑥铜、⑦氯酸钾、⑧高锰酸钾、⑨稀有气体的晶体、⑩干冰
(1)属于共价晶体的有:___________ ;属于分子晶体的有:___________ ;属于离子晶体的有:___________ ;属于金属晶体的有:___________ 。
Ⅱ.比较:
(2)熔点:金刚石___________ 干冰(填“>”或“<”),原因是___________ 。
(3)键角:CH4___________ H2O(填“>”或“<”),原因是___________ 。
Ⅲ.请回答:
(4)黄铜合金采取面心立方堆积,其晶胞结构如图所示:___________ 。
②与Cu原子等距离且最近的Cu原子有___________ 个。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:___________ 。
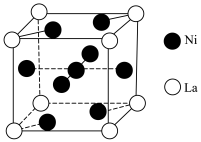
(6)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如图。___________ 。
①氯化钡、②石英、③金刚砂、④水、⑤乙醇、⑥铜、⑦氯酸钾、⑧高锰酸钾、⑨稀有气体的晶体、⑩干冰
(1)属于共价晶体的有:
Ⅱ.比较:
(2)熔点:金刚石
(3)键角:CH4
Ⅲ.请回答:
(4)黄铜合金采取面心立方堆积,其晶胞结构如图所示:

②与Cu原子等距离且最近的Cu原子有
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:
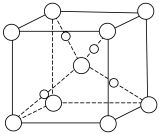
(6)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如图。
您最近半年使用:0次
解题方法
5 . 生产生活中处处有化学,结合物质与结构的相关知识,回答下列问题:
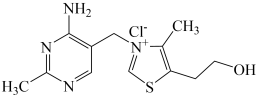
(1)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用,该物质的结构简式如图所示:___________ 。
a.离子键、共价键 b.离子键、氢键、共价键
c.氢键、范德华力 d.离子键、氢键、范德华力
②维生素B1燃烧可生成N2、NH3、CO2、SO2、H2O、HCl等物质,这些物质中属于非极性分子的化合物有___________ 。
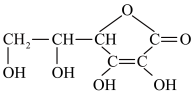
(2)维生素C的结构简式如下,它能防治坏血病,该分子中有___________ 个手性碳原子。___________ (填标号)。
a.原子轨道电子排布半充满时体系能量最低,电子排布式为[Ne]3s13p3
b.3p轨道的电子总是比3s轨道的电子在离核更远的区域运动
c.电负性比Al高,原子对键合电子的吸引力比Al大
(4)近年来美国为了遏制中国发展,对我国发起了以封锁“芯片”为核心的全方位打压,此举激发了中国科技人员自研的决心。2022年10月宁波南大光电ArF光刻胶生产线正式投产,国内7 nm芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:___________ 。
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有___________ 。
(5)金属钛密度小、强度高、抗腐蚀性能好,是应用广泛的金属。含钛的矿石主要有金红石和钛铁矿。将1 mol TiCl3∙4H2O溶于水,加入足量AgNO3溶液,得到1 mol AgCl沉淀,已知Ti3+的配位数为6,TiCl3∙4H2O的化学式用配合物的形式表示为___________ 。
(1)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用,该物质的结构简式如图所示:
a.离子键、共价键 b.离子键、氢键、共价键
c.氢键、范德华力 d.离子键、氢键、范德华力
②维生素B1燃烧可生成N2、NH3、CO2、SO2、H2O、HCl等物质,这些物质中属于非极性分子的化合物有
(2)维生素C的结构简式如下,它能防治坏血病,该分子中有
a.原子轨道电子排布半充满时体系能量最低,电子排布式为[Ne]3s13p3
b.3p轨道的电子总是比3s轨道的电子在离核更远的区域运动
c.电负性比Al高,原子对键合电子的吸引力比Al大
(4)近年来美国为了遏制中国发展,对我国发起了以封锁“芯片”为核心的全方位打压,此举激发了中国科技人员自研的决心。2022年10月宁波南大光电ArF光刻胶生产线正式投产,国内7 nm芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
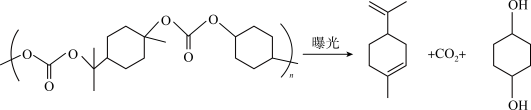
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有
(5)金属钛密度小、强度高、抗腐蚀性能好,是应用广泛的金属。含钛的矿石主要有金红石和钛铁矿。将1 mol TiCl3∙4H2O溶于水,加入足量AgNO3溶液,得到1 mol AgCl沉淀,已知Ti3+的配位数为6,TiCl3∙4H2O的化学式用配合物的形式表示为
您最近半年使用:0次
6 . 下列叙述正确的是
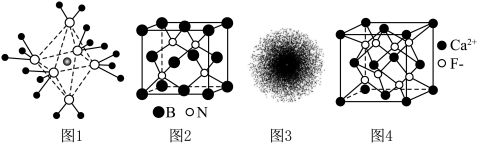
| A.图1为[Cu(NH3)4(H2O)2]2+结构示意图,该离子内存在极性键、配位键、离子键 |
| B.图2为BN晶体的晶胞示意图,由N和B原子围成的最小六元环为平面结构 |
| C.图3为H原子的电子云图,一个黑点表示一个电子 |
| D.图4为CaF2晶体的晶胞示意图,与Ca2+周围紧邻且距离相等的F-共有8个 |
您最近半年使用:0次
7 . 下列说法正确的是
| A.CO2、HClO、P4分子中所有原子均满足最外层8电子稳定结构 |
| B.离子晶体中可能存在共价键,而分子晶体中一定存在共价键 |
| C.氨气很稳定(很高温度才会部分分解),并不是氨气中含有大量的氢键所致 |
| D.金刚石、石英和C60均为空间网状结构的共价晶体,加热熔化时需破坏共价键 |
您最近半年使用:0次
解题方法
8 . 下列说法不正确的是
①N2H4分子中既含极性键又含非极性键
②若R2-、M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④NCl3、PCl3、CO2、CS2分子中各原子均达到 稳定结构
稳定结构
⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦Na2O2固体中的阴离子和阳离子个数比是1∶2
⑧第一电离能介于B和N之间的第二周期元素有2种
①N2H4分子中既含极性键又含非极性键
②若R2-、M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④NCl3、PCl3、CO2、CS2分子中各原子均达到
 稳定结构
稳定结构⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦Na2O2固体中的阴离子和阳离子个数比是1∶2
⑧第一电离能介于B和N之间的第二周期元素有2种
| A.②⑤⑥⑧ | B.①③④⑤ | C.②④⑤⑦ | D.③⑤⑦⑧ |
您最近半年使用:0次
解题方法
9 . 下列说法中,错误的是
| A.H-Cl键的键能为431.8 kJ/mol,H-Br键的键能为366 kJ/mol,这可以说明HCl比HBr分子稳定 |
| B.共价键都具有方向性 |
| C.H2O2中只有σ键没有π键 |
| D.N2中有1个σ键和2个π键 |
您最近半年使用:0次
名校
解题方法
10 . 下列有机物中,由于分子之间易形成氢键,沸点较高的是
| A.乙烷 | B.乙醇 | C.乙酸乙酯 | D.甲苯 |
您最近半年使用:0次



