名校
1 . 下列关于物质的性质、用途等描述错误的是
| A.工业上,用氯气和热的石灰乳制备漂白粉、漂粉精 |
| B.在葡萄酒中添加适量的SO2能杀灭微生物并防止葡萄酒的氧化变质 |
| C.储氢合金是一类能大量吸收H2,并与H2结合成金属氢化物的材料 |
| D.高铁酸钾(K2FeO4)在水处理过程中涉及的变化过程有:氧化还原反应、蛋白质变性、盐类水解、胶体聚沉等 |
您最近一年使用:0次
2 . 便携式消毒除菌卡主要活性成分为亚氯酸钠(NaClO2);一种制备NaClO2粗产品的工艺流程如图。已知纯ClO2易分解爆炸,一般用空气稀释到10%以下。
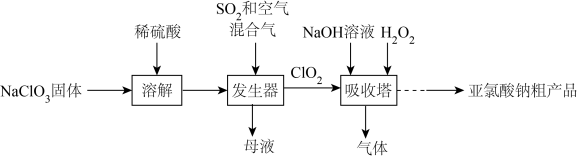
| A.溶解过程中可以用盐酸代替稀硫酸 |
| B.流程中H2O2做氧化剂 |
| C.发生器中鼓入空气的主要目的是提供氧化剂 |
| D.吸收塔中温度不宜过高,否则会导致NaClO2产率下降 |
您最近一年使用:0次
名校
解题方法
3 .  是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物
是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物 可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。
可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。
已知:①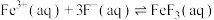
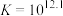
②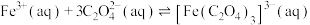

I.制备高铁酸盐
(1)在碱性条件下以多孔的磁铁矿作阳极电解制备高铁酸盐的电极反应式是___________ 。
Ⅱ.高铁酸盐稳定性的研究
(2)碱性环境下,久置的 溶液中除了产生红褐色
溶液中除了产生红褐色 外,同时还会产生绿色的
外,同时还会产生绿色的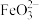 ,此过程的反应为
,此过程的反应为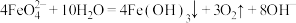 、
、___________ 。
为研究使稳定的方法,分别做以下4个实验:
资料:吸光度大小与溶液中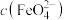 成正比。
成正比。___________ ,但吸光度结果图显示甲同学预测并不正确,原因可能是d试管加入的 与
与 发生配位反应的速率
发生配位反应的速率___________ (填“快”或“慢”),且进行程度大,导致催化剂 量减少,
量减少, 的分解速率
的分解速率___________ (填“快”或“慢”)。
(4)乙同学推测“ ”曲线为试管c的实验结果,依据是
”曲线为试管c的实验结果,依据是___________ 。
(5)综合以上分析,为增强高铁酸盐的稳定性,可向其中加入___________ (填化学式)。
Ⅲ.高铁酸盐产品纯度的测定
称取mg高铁酸钾粗品,配成250mL溶液,准确量取25.00mL放入锥形瓶,加入足量 和NaOH溶液,振荡,再加入稀硫酸酸化后得到
和NaOH溶液,振荡,再加入稀硫酸酸化后得到 和
和 ,滴入几滴二苯胺磺酸钠作指示剂,用
,滴入几滴二苯胺磺酸钠作指示剂,用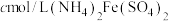 标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗
标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗 标准溶液VmL。
标准溶液VmL。
(6)粗品中 的质量分数为
的质量分数为___________ 。[已知: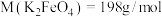 ]
]
 是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物
是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物 可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。
可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。已知:①
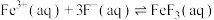
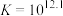
②
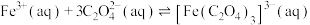

I.制备高铁酸盐
(1)在碱性条件下以多孔的磁铁矿作阳极电解制备高铁酸盐的电极反应式是
Ⅱ.高铁酸盐稳定性的研究
(2)碱性环境下,久置的
 溶液中除了产生红褐色
溶液中除了产生红褐色 外,同时还会产生绿色的
外,同时还会产生绿色的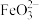 ,此过程的反应为
,此过程的反应为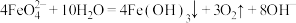 、
、为研究使稳定的方法,分别做以下4个实验:
| 序号 |  | 现象 | |
| a | 2滴0.01mol/LKI溶液 | 紫色迅速褪去 |
| b | 2滴蒸馏水 | 分别用紫外可见分光光度计测三支试管内溶液的吸光度,结果如下图所示。 | |
| c | 2滴0.01mol/LNaF溶液 | ||
| d | 2滴 溶液 溶液 |
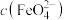 成正比。
成正比。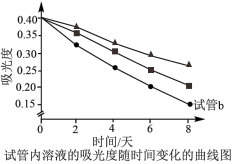
 与
与 发生配位反应的速率
发生配位反应的速率 量减少,
量减少, 的分解速率
的分解速率(4)乙同学推测“
 ”曲线为试管c的实验结果,依据是
”曲线为试管c的实验结果,依据是(5)综合以上分析,为增强高铁酸盐的稳定性,可向其中加入
Ⅲ.高铁酸盐产品纯度的测定
称取mg高铁酸钾粗品,配成250mL溶液,准确量取25.00mL放入锥形瓶,加入足量
 和NaOH溶液,振荡,再加入稀硫酸酸化后得到
和NaOH溶液,振荡,再加入稀硫酸酸化后得到 和
和 ,滴入几滴二苯胺磺酸钠作指示剂,用
,滴入几滴二苯胺磺酸钠作指示剂,用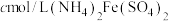 标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗
标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗 标准溶液VmL。
标准溶液VmL。(6)粗品中
 的质量分数为
的质量分数为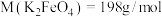 ]
]
您最近一年使用:0次
2024-06-05更新
|
261次组卷
|
4卷引用:辽宁省协作校2023-2024学年高三下学期三模化学试题
4 . Cu与KCN溶液反应的化学方程式为: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.基态Cu原子中含有2个未成对电子 |
B.每生成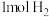 转移电子数为 转移电子数为 |
C.常温下, 中心原子上含有的孤电子对数是 中心原子上含有的孤电子对数是 |
D. 中含有 中含有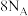 个 个 键 键 |
您最近一年使用:0次
名校
解题方法
5 . 亚硝酸钙 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。 溶液能将NO氧化为
溶液能将NO氧化为 。
。
回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通 ,其目的是
,其目的是________ 。通 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是________ 。
(2)仪器a的名称为________ ,装置D中盛装的试剂是________ (填名称),装置E的作用是________ 。
(3)制备的产品 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为________ ,样品中 的纯度为
的纯度为________ (用含m、V的式子表示)。
 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。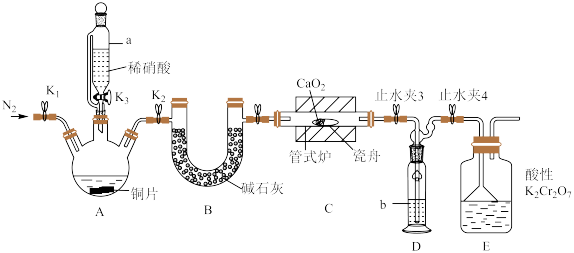
 溶液能将NO氧化为
溶液能将NO氧化为 。
。回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通
 ,其目的是
,其目的是 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是(2)仪器a的名称为
(3)制备的产品
 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: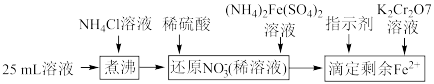
 ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为 的纯度为
的纯度为
您最近一年使用:0次
2024-06-01更新
|
292次组卷
|
7卷引用:辽宁省部分高中2024届高三下学期二轮复习联考(二)化学试题
名校
解题方法
6 . 某同学利用W形管和V形管安装了下面微型实验装置,进行 的制备及探究
的制备及探究 的漂白性实验。下列说法正确的是
的漂白性实验。下列说法正确的是
 的制备及探究
的制备及探究 的漂白性实验。下列说法正确的是
的漂白性实验。下列说法正确的是
| A.固体粉末甲为二氧化锰 |
B.鲜花花瓣褪色说明 具有漂白性 具有漂白性 |
| C.W形管和V形管的玻璃泡能防止倒吸 |
D.溶液乙为碱液,与安全气球共同防止 逸出 逸出 |
您最近一年使用:0次
2024-05-31更新
|
255次组卷
|
5卷引用:辽宁省部分高中2024届高三下学期二轮复习联考(二)化学试题
名校
解题方法
7 .  和
和 在工业生产中有广泛应用。下列离子方程式正确且符合题意的是
在工业生产中有广泛应用。下列离子方程式正确且符合题意的是
 和
和 在工业生产中有广泛应用。下列离子方程式正确且符合题意的是
在工业生产中有广泛应用。下列离子方程式正确且符合题意的是A.硫酸铁溶液用于腐蚀铜质电路板;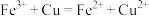 |
B.将 溶液与氨水 溶液与氨水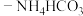 混合溶液反应,生成 混合溶液反应,生成 沉淀: 沉淀: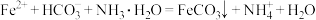 |
C.在硫酸铁溶液中滴加 溶液,产生红褐色沉淀: 溶液,产生红褐色沉淀: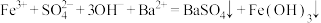 |
D.在NaClO溶液中滴加少量 溶液: 溶液: |
您最近一年使用:0次
2024-05-27更新
|
373次组卷
|
3卷引用:2024届辽宁省沈阳市第二中学高三下学期三模化学试题
解题方法
8 . 150mL某无色溶液中可能含有 中的若干种,现将此溶液分成三等份,进行如下实验:
中的若干种,现将此溶液分成三等份,进行如下实验:
①向第一份中加入足量的 稀盐酸,生成0.448L气体(已换算成标准状况下);
稀盐酸,生成0.448L气体(已换算成标准状况下);
②向第二份中加入足量NaOH溶液并加热,收集到0.04mol气体;
③向第三份中加入足量BaCl2溶液,得到沉淀6.27g,加入足量 稀盐酸充分反应后,剩余沉淀2.33g。
稀盐酸充分反应后,剩余沉淀2.33g。
根据上述实验,回答下列问题:
(1)用12mol·L-1的浓盐酸配制240mL0.5mol·L-1稀盐酸,需要用量筒量取___________ mL浓盐酸,若在量取浓盐酸时俯视刻度线,则会导致配制的稀盐酸的浓度___________ (填“偏高”、“偏低”或“不变”)。
(2)实验②中生成气体的离子方程式为___________ 。
(3)实验③中沉淀部分溶解的化学方程式为___________ ,剩余沉淀的化学式为___________ 。
(4)原溶液中
___________ 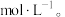
(5)经分析,溶液中一定存在Na+,理由是___________ 。
 中的若干种,现将此溶液分成三等份,进行如下实验:
中的若干种,现将此溶液分成三等份,进行如下实验:①向第一份中加入足量的
 稀盐酸,生成0.448L气体(已换算成标准状况下);
稀盐酸,生成0.448L气体(已换算成标准状况下);②向第二份中加入足量NaOH溶液并加热,收集到0.04mol气体;
③向第三份中加入足量BaCl2溶液,得到沉淀6.27g,加入足量
 稀盐酸充分反应后,剩余沉淀2.33g。
稀盐酸充分反应后,剩余沉淀2.33g。根据上述实验,回答下列问题:
(1)用12mol·L-1的浓盐酸配制240mL0.5mol·L-1稀盐酸,需要用量筒量取
(2)实验②中生成气体的离子方程式为
(3)实验③中沉淀部分溶解的化学方程式为
(4)原溶液中

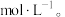
(5)经分析,溶液中一定存在Na+,理由是
您最近一年使用:0次
名校
9 . 下列物质的鉴别或检验能达到目的的是
A.用澄清石灰水鉴别 和 和 气体 气体 | B.用溴的四氯化碳溶液鉴别苯和己烷 |
| C.用金属钠检验乙醇中是否含有乙醛 | D.用红色石蕊试纸检验苏打溶液的酸碱性 |
您最近一年使用:0次
解题方法
10 . 根据所学知识,回答下列问题:
(1)K2FeO4是常见的水处理剂,净水原理如图所示。请回答下列问题:___________ 。
②过程a中K2FeO4体现___________ (填“氧化”或“还原”)性,反应过程中转移5.418×1022个电子,需要___________ mol K2FeO4。
(2)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:___________ 。
___________Fe(OH)3+___________KOH+___________KClO=___________K2FeO4+___________KCl+___________H2O
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是___________ ,生产1mol的高铁酸钠,需要转移电子的物质的量是___________ mol。
(4)将铝箔放入NaOH稀溶液中,开始时无气体生成,写出反应的离子方程式:___________ ;反应片刻后,可观察到有气体产生。
(1)K2FeO4是常见的水处理剂,净水原理如图所示。请回答下列问题:
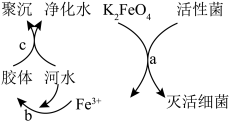
②过程a中K2FeO4体现
(2)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
___________Fe(OH)3+___________KOH+___________KClO=___________K2FeO4+___________KCl+___________H2O
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是
(4)将铝箔放入NaOH稀溶液中,开始时无气体生成,写出反应的离子方程式:
您最近一年使用:0次




