名校
解题方法
1 . FeCl2是中学化学常用试剂。请根据题意填空:
往FeCl2溶液中加入KSCN溶液,溶液___ (填“变”或“不变”)色,再往其中通入氯气,溶液呈___ (填“红”或“蓝”)色。除去FeCl2溶液中少量的FeCl3应加(通)入的试剂为___ (填“Fe”或“Cl2”)。
往FeCl2溶液中加入KSCN溶液,溶液
您最近一年使用:0次
2020-05-26更新
|
382次组卷
|
2卷引用:湖南省2020年普通高中学业水平合格性考试模拟卷一 化学
名校
解题方法
2 . 下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题;
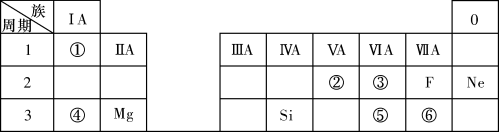
(1)④表示的元素是___ (填元素符号);
(2)②、③两种元素相比较,原子半径较大的是___ (填元素符号);
(3)写出①与⑥两种元素所形成化合物的化学式___ ;
(4)③和⑤两种元素的非金属性强弱顺序是③____ ⑤(填“<”或“>”)。

(1)④表示的元素是
(2)②、③两种元素相比较,原子半径较大的是
(3)写出①与⑥两种元素所形成化合物的化学式
(4)③和⑤两种元素的非金属性强弱顺序是③
您最近一年使用:0次
2020-05-13更新
|
646次组卷
|
3卷引用:湖南省2019-2020学年高二学业水平考试信息模拟(五) 化学
3 . 钠、铝和钙是中学化学常见的三种重要金属。请回答下列问题:
(1)常盛放在呼吸面具中作为供氧剂的物质为____________ (填“ ”或“
”或“ ”)。
”)。
(2) 能溶于酸或强碱溶液生成盐和水,则
能溶于酸或强碱溶液生成盐和水,则 是一种
是一种____________ (填“酸性”“碱性”或“两性”)氧化物。
(3)漂白粉的有效成分为____________ (填“ ”或“
”或“ ”)。
”)。
(1)常盛放在呼吸面具中作为供氧剂的物质为
 ”或“
”或“ ”)。
”)。(2)
 能溶于酸或强碱溶液生成盐和水,则
能溶于酸或强碱溶液生成盐和水,则 是一种
是一种(3)漂白粉的有效成分为
 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
名校
4 . 回答下列问题:
(1)工业上常用铝土矿冶炼金属铝。
①铝土矿的主要成分为 和
和 ,其中
,其中 属于
属于____________ (填“酸性”“碱性”或“两性”)氧化物;
②冶炼过程中需要用到氨,氨溶于水所得溶液呈____________ (填“酸性”或“碱性”);
③利用金属活动性的不同,可以采用不同的冶炼方法,制取单质铝应采取_____________ (填“热还原法”或“电解法”)。
(2)工业上合成氨的反应为: ,一定条件下,将
,一定条件下,将 和
和 置于
置于 的密闭容器中,
的密闭容器中,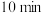 后测得
后测得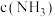 为
为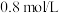 。
。
①用 表示该反应的速率为
表示该反应的速率为___________ ;
②其他条件不变时,再通入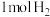 ,该反应的速率将
,该反应的速率将_____________ (填“增大”或“减小”)。
(1)工业上常用铝土矿冶炼金属铝。
①铝土矿的主要成分为
 和
和 ,其中
,其中 属于
属于②冶炼过程中需要用到氨,氨溶于水所得溶液呈
③利用金属活动性的不同,可以采用不同的冶炼方法,制取单质铝应采取
(2)工业上合成氨的反应为:
 ,一定条件下,将
,一定条件下,将 和
和 置于
置于 的密闭容器中,
的密闭容器中,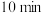 后测得
后测得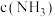 为
为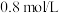 。
。①用
 表示该反应的速率为
表示该反应的速率为②其他条件不变时,再通入
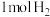 ,该反应的速率将
,该反应的速率将
您最近一年使用:0次
2020-05-12更新
|
408次组卷
|
2卷引用:湖南省2020年普通高中学业水平考试第一次模拟试卷化学试题
5 . 往FeCl3溶液中加入KSCN溶液,溶液呈现_______ 色、再往其中加入铁粉,发生的离子反应为________________ 。
您最近一年使用:0次
解题方法
6 . 化学是门实用性很强的科学。请根据题意填空:
(1)铝制易拉罐的表面有一层氧化膜,主要成分是Al2O3。它与盐酸和氢氧化钠溶液反应都生成盐和水,则Al2O3属于___ 氧化物(填“酸性”、“碱性” 或“两性”)
(2)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式: 2Na2O2 + 2__ = 2Na2 CO3 +O2 ↑;
(3)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是__ (填“食盐”或“纯碱”).
(1)铝制易拉罐的表面有一层氧化膜,主要成分是Al2O3。它与盐酸和氢氧化钠溶液反应都生成盐和水,则Al2O3属于
(2)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式: 2Na2O2 + 2
(3)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是
您最近一年使用:0次
7 . 目前,从海水提取的溴占世界溴年产量的三分之一左右,空气吹出法是工业规模海水提溴的常用方法。其中一种工艺流程为:①海水浓缩,酸化;②通入Cl2,使Br— 转化为Br2;③通入空气、水蒸气,将Br2吹入吸收塔,与吸收剂SO2反应转化为HBr;④通入Cl2,再经过一系列处理得到产品Br2。请回答下列问题:
(1)步骤②、③操作的目的是_____ (填“富集溴”或“萃取溴”);
(2)在步骤③中,生成HBr的化学方程式是___________ ;
(3)在步骤②中,若通入22.4LCl2(标准状况),理论上可得Br2__________ g。
(1)步骤②、③操作的目的是
(2)在步骤③中,生成HBr的化学方程式是
(3)在步骤②中,若通入22.4LCl2(标准状况),理论上可得Br2
您最近一年使用:0次
2014高二·湖南·学业考试
8 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
(1)①的元素符号是__________
(2)②和⑥两种元素的原子半径大小关系:_________ (填“>”或“<”);
(3)③和⑤两种元素的金属性强弱关系:________ (填“>”或“<”);
(4)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:__________ 。
| ⅠA | 0 | ||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | B | ① | ② | Ne | |||||
| 3 | ③ | ④ | ⑤ | Si | ⑥ | ||||
(1)①的元素符号是
(2)②和⑥两种元素的原子半径大小关系:
(3)③和⑤两种元素的金属性强弱关系:
(4)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次
解题方法
9 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
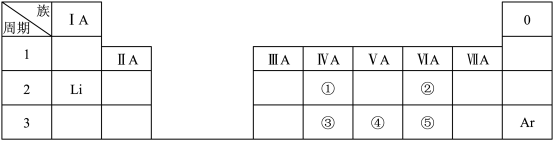
(1)①的元素符号是_________ ;
(2)②的原子结构示意图是_________ ;
(3)①和③的原子半径大小关系是:①____ ③(填“>”、“<”或“=”);
(4)③、④和⑤中,最高价氧化物对应的水化物酸性最强的酸的化学式是____________ 。

(1)①的元素符号是
(2)②的原子结构示意图是
(3)①和③的原子半径大小关系是:①
(4)③、④和⑤中,最高价氧化物对应的水化物酸性最强的酸的化学式是
您最近一年使用:0次
解题方法
10 . 请根据物质在生产中的应用填空:
(1)自来水厂对水消毒,常使用的物质是__________ (填“液氯”或“明矾”)
(2)制造光导纤维的基本原料是__________ (填“硅”或“二氧化硅”)
(3)铁在冷的浓硫酸或浓硝酸中,表面被氧化生成致密氧化物膜而保护内层金属,常温下盛装浓硫酸或浓硝酸可以使用容器是________ (填“铁罐”或“铜罐”)
(1)自来水厂对水消毒,常使用的物质是
(2)制造光导纤维的基本原料是
(3)铁在冷的浓硫酸或浓硝酸中,表面被氧化生成致密氧化物膜而保护内层金属,常温下盛装浓硫酸或浓硝酸可以使用容器是
您最近一年使用:0次



