名校
解题方法
1 . 短周期元素W、X、Y、Z的原子序数依次增大,W、Z位于同主族,四种元素组成的一种化合物的结构式为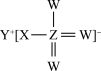 ,下列说法错误的是
,下列说法错误的是
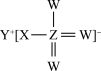 ,下列说法错误的是
,下列说法错误的是| A.X的最简单氢化物的稳定性比W的强 |
| B.X与Y形成的是离子化合物 |
| C.W与Y形成的化合物中可能含有共价键 |
D.简单离子半径: |
您最近一年使用:0次
2023-10-18更新
|
148次组卷
|
2卷引用:广东广雅中学2023-2024学年高二上学期开学考化学试题
解题方法
2 . 铅(Pb)及其化合物广泛用于冶金、蓄电池、印刷、颜料、油漆等领域,常见铅的化合物主要以+2价和+4价的形态存在。经查阅资料:
已知:①Pb与酸反应都得到+2价的化合物。
②PbCl4不稳定,易分解为PbCl2和Cl2。
回答下列问题:
(1)Pb是较活泼金属,但在实验室或化工厂常用Pb作为某些酸(如稀硫酸)的耐酸反应器的衬里和贮存、输送的管道设备。请解释其原因___________ 。
(2)PbSO4可用于制造蓄电池、白色颜料等。写出用钠盐制备PbSO4的化学方程式___________ 。
(3)PbO2在强酸性条件下能与Mn2+反应生成Pb2+和 ,反应的离子方程式为
,反应的离子方程式为 ___________ ,该反应说明PbO2具有 ___________ (填“氧化性”或“还原性”)。
(4)经查阅,PbO2是两性氧化物,设计实验并验证
| 物质 | PbO | PbO2 | PbCl2 | PbCl+4 |
| 在水中的溶解性(常温) | 难溶于水的黄色固体 | 难溶于水的棕黑色固体 | 微溶于水的白色固体 | 易溶于水的黄色油状液体 |
| 物质 | PbSO4 | Pb(NO3)2 | Na2PbO2 | Na2PbO3 |
| 在水中的溶解性(常温) | 难溶于水的白色固体 | 易溶于水形成无色溶液 | 易溶于水形成无色溶液 | 易溶于水形成无色溶液 |
②PbCl4不稳定,易分解为PbCl2和Cl2。
回答下列问题:
(1)Pb是较活泼金属,但在实验室或化工厂常用Pb作为某些酸(如稀硫酸)的耐酸反应器的衬里和贮存、输送的管道设备。请解释其原因
(2)PbSO4可用于制造蓄电池、白色颜料等。写出用钠盐制备PbSO4的化学方程式
(3)PbO2在强酸性条件下能与Mn2+反应生成Pb2+和
 ,反应的离子方程式为
,反应的离子方程式为 (4)经查阅,PbO2是两性氧化物,设计实验并验证
| 实验步骤 | 实验现象 | 反应的化学方程式 |
| ①向盛有PbO2固体的试管中滴加NaOH溶液 | 棕黑色固体逐渐溶解 | |
| ②向盛有PbO2固体的试管中滴加稀盐酸 |
您最近一年使用:0次
名校
解题方法
3 . 已知浓盐酸与高锰酸钾固体混合反应能生成Cl2、KCl和MnCl2等,实验小组在实验室设计如图装置制备纯净、干燥的Cl2并检验其性质,请回答:
Ⅰ.制备氯气和金属氯化物
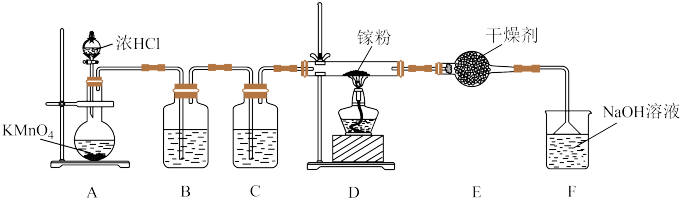
(1)装置A中发生反应的离子方程式为___________ 。
(2)已知镓(Ga)是一种“类铝”金属,能与氯气反应___________ (填化学式),该生成物具有很强的吸湿性,在空气中易吸收水蒸气而冒烟。为保证实验顺利进行___________ 、___________ 。装置E的作用是 ___________ 。
Ⅱ.检验氯气的性质:
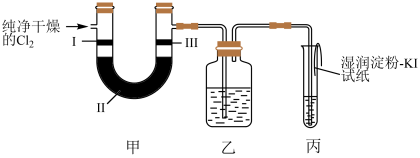
(3)装置甲的实验目的是验证氯气是否具有漂白性,则甲中Ⅰ、Ⅱ、Ⅲ应依次放___________ (填字母)。
(4)装置乙中盛有NaBr溶液,观察到的实验现象是 ___________ 。该现象说明 ___________ 。
(5)装置丙中盛有NaOH溶液,试管口内部放置湿润淀粉﹣KI试纸的主要目的是___________ 。
Ⅰ.制备氯气和金属氯化物

(1)装置A中发生反应的离子方程式为
(2)已知镓(Ga)是一种“类铝”金属,能与氯气反应
Ⅱ.检验氯气的性质:

(3)装置甲的实验目的是验证氯气是否具有漂白性,则甲中Ⅰ、Ⅱ、Ⅲ应依次放
| 选项 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 生石灰 | 湿润的有色布条 |
| b | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
(5)装置丙中盛有NaOH溶液,试管口内部放置湿润淀粉﹣KI试纸的主要目的是
您最近一年使用:0次
解题方法
4 . 工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质)制取绿矾(FeSO4•7H2O,相对分子质量278),流程如图:
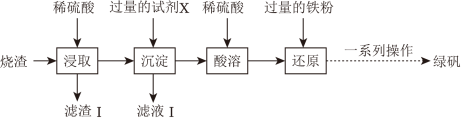
已知:SiO2是酸性氧化物,不溶于稀硫酸。
(1)滤渣Ⅰ的主要成分是___________ (填化学式)。
(2)“试剂X”的化学式是___________ ,滤液Ⅰ中的阴离子有 ___________ (填离子符号)。
(3)“还原”后,经“一系列操作”可得绿矾,则“一系列操作”为___________ 、蒸发浓缩、___________ 、过滤、洗涤、干燥。操作过程中需尽量减少与空气接触的目的是 ___________ 。
(4)已知m1kg该烧渣(含Fe28%,假设生产过程无损耗),某同学通过理论计算可得到绿矾的质量m2= kg,该计算式
kg,该计算式__ (填“正确”或“不正确”),理由是 ___________ 。

已知:SiO2是酸性氧化物,不溶于稀硫酸。
(1)滤渣Ⅰ的主要成分是
(2)“试剂X”的化学式是
(3)“还原”后,经“一系列操作”可得绿矾,则“一系列操作”为
(4)已知m1kg该烧渣(含Fe28%,假设生产过程无损耗),某同学通过理论计算可得到绿矾的质量m2=
 kg,该计算式
kg,该计算式
您最近一年使用:0次
解题方法
5 . 联合国大会将2019年定为“化学元素周期表国际年”,表明了元素周期律的重要性。如表列出了元素周期表中短周期的一部分,a~i代表9种短周期元素。
请用化学用语回答下列问题:
(1)a和b形成的化合物可用作催化剂,其化学式为___________ 。
(2)元素c、d形成的简单离子半径大小关系为___________ >___________ (填离子符号)。
(3)9种元素中非金属性最强的是___________ (填元素符号)。
(4)若单质c与水反应得到3.36L的气体(标准状况),则消耗单质c的质量为___________ g。
(5)写出实验室制备g的最高价氧化物对应的水化物的离子方程式___________ 。
(6)预测将i的单质通入h的氢化物的水溶液中___________ (填“能”或“不能”)发生反应,请简述预测的依据:___________ 。
| 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA |  | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | a | b | c | d | |||||
| 3 | c | f | g | h | i | ||||
(1)a和b形成的化合物可用作催化剂,其化学式为
(2)元素c、d形成的简单离子半径大小关系为
(3)9种元素中非金属性最强的是
(4)若单质c与水反应得到3.36L的气体(标准状况),则消耗单质c的质量为
(5)写出实验室制备g的最高价氧化物对应的水化物的离子方程式
(6)预测将i的单质通入h的氢化物的水溶液中
您最近一年使用:0次
名校
解题方法
6 . 下列装置或操作一定能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 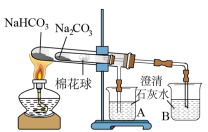 | 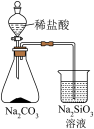 | 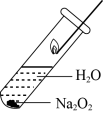 | 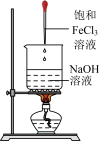 |
| 实验目的 | 验证热稳定性:Na2CO3>NaHCO3 | 验证非金属性强弱:Cl>C>Si | 验证Na2O2与水反应生成O2 | 制备Fe(OH)3胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-12更新
|
210次组卷
|
2卷引用:广东省广州市荔湾区2022-2023学年高一下学期开学考试化学试题
解题方法
7 . 高铁般的(Na2FeO4)是一种新型绿色消毒剂。工业上制备高铁酸钠的一种方法为:3ClO﹣+2Fe3++10OH﹣=2FeO +3Cl﹣+5H2O。下列说法不正确的是
+3Cl﹣+5H2O。下列说法不正确的是
 +3Cl﹣+5H2O。下列说法不正确的是
+3Cl﹣+5H2O。下列说法不正确的是A.FeO 中Fe元素的化合价为+6价 中Fe元素的化合价为+6价 |
| B.该反应中ClO﹣是氧化剂,H2O是还原产物 |
C.反应中每生成1molFeO ,转移电子为3mol ,转移电子为3mol |
| D.反应中氧化剂与还原剂的物质的量之比为3:2 |
您最近一年使用:0次
解题方法
8 . 设NA表示阿代加德罗常数,下列叙述中正确的是
A.1molD3 O+中含有的中子数为10NA O+中含有的中子数为10NA |
| B.常温常压下,11.2L氧气所含的原子数为NA |
| C.1mol/LNa2CO3溶液中,含存Na+的数目为2NA |
D.62g的P4( )分子中含有P﹣P键数为3NA )分子中含有P﹣P键数为3NA |
您最近一年使用:0次
名校
解题方法
9 . 已知Fe2+、I-、Br-、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序I->H2O2>Fe2+>Br->Cl-,则下列反应不可能发生的是
| A.2Fe2++I2=2Fe3++2I﹣ |
| B.Br2+2Fe2+=2Fe3++2Br﹣ |
| C.H2O2+2Fe3+=2Fe2++O2↑+2H+ |
| D.Cl2+2Fe2+=2Fe3++2Cl﹣ |
您最近一年使用:0次
2023-08-12更新
|
496次组卷
|
3卷引用:广东省广州市荔湾区2022-2023学年高一下学期开学考试化学试题
解题方法
10 . 下列说法正确的是
| A.Na2O和NaOH均为离子化合物,因此都只含有离子键 |
| B.Na2CO3固体和NaHCO3固体分别溶于少量水时,均伴随着放热现象 |
| C.Fe在高温下与水蒸气反应的产物为Fe3O4,FeO在空气中受热得到的产物也为Fe3O4 |
| D.Fe与硫酸铜溶液反应可置换出Cu,将Na投入硫酸铜溶液中也可置换出Cu |
您最近一年使用:0次



