名校
解题方法
1 . 氮、磷、砷、锑为元素周期表中原子序数依次增大的同族元素。
(1)锑在元素周期表中的位置_______ 。
(2)除 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
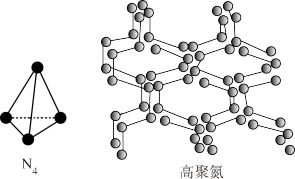
① 分子是一种
分子是一种_______ (填“极性”或“非极性”)分子。
② 的沸点
的沸点_______ (填“>”、“<”或“=”)高聚氮的沸点,原因是_______ 。
(3)热稳定性:
_______  (填“>”“<”),判断依据是
(填“>”“<”),判断依据是_______ 。
(4) 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为_______ ,C原子的杂化类型为_______ 。
(1)锑在元素周期表中的位置
(2)除
 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
①
 分子是一种
分子是一种②
 的沸点
的沸点(3)热稳定性:

 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(4)
 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为
您最近一年使用:0次
21-22高三下·上海浦东新·阶段练习
名校
2 . 寻找合适的催化剂,用于光催化CO2转化有助于解决世界能源短缺和环境问题。以CO2为碳源光催化转化为CH4、HCOOH、HCHO等能源物质,称为人工光合作用。C3N4,Ag3PO4等化合物均可以作为转化的催化剂。回答下列问题:
(1)CO2的电子式为_______ ,H、C、N、O原子的半径大小为_______ ,C3N4具有很高的熔沸点,比较它与金刚石熔点高低,说明理由_______ 。
(2)尿素在550℃下热解4h可得到氮化碳:3CO(NH2)2(g)⇌C3N4(s)+3H2O(g)+2NH3(g),反应平衡常数表达式为_______ ,下列能够说明尿素热解反应达到平衡状态的是(不考虑副反应)_______ :
a.气体的密度不再发生变化
b.H2O和NH3的物质的量之比不再变化
c.体系的压强不再发生变化
d.消耗CO(NH2)2的速率等于生成H2O的速率
(3)下面为某人工光合作用反应(CO2+2H2O→CH4+2O2)的能量转化图,正确的是_______
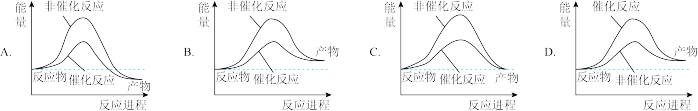
(4)CO2在催化转化的过程中被还原的元素为_______ ,某课题组研究CO2在甲醇中的催化转化,检测到一种有含两个碳原子,具有香味的物质生成,其结构简式为_______ 。
(5)磷酸银是一种优良的光催化材料,容易被光腐蚀而失活。研究人员用H2O2使其恢复活性,配平下列方程式:_______ 。
_______H2O2+_______Ag+_______ →_______Ag3PO4+_______OH-+_______H2O
→_______Ag3PO4+_______OH-+_______H2O
(1)CO2的电子式为
(2)尿素在550℃下热解4h可得到氮化碳:3CO(NH2)2(g)⇌C3N4(s)+3H2O(g)+2NH3(g),反应平衡常数表达式为
a.气体的密度不再发生变化
b.H2O和NH3的物质的量之比不再变化
c.体系的压强不再发生变化
d.消耗CO(NH2)2的速率等于生成H2O的速率
(3)下面为某人工光合作用反应(CO2+2H2O→CH4+2O2)的能量转化图,正确的是
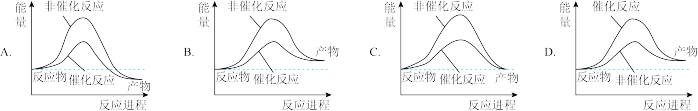
(4)CO2在催化转化的过程中被还原的元素为
(5)磷酸银是一种优良的光催化材料,容易被光腐蚀而失活。研究人员用H2O2使其恢复活性,配平下列方程式:
_______H2O2+_______Ag+_______
 →_______Ag3PO4+_______OH-+_______H2O
→_______Ag3PO4+_______OH-+_______H2O
您最近一年使用:0次
名校
解题方法
3 . 下列有关比较正确的是
| A.沸点:NH3>PH3>AsH3 | B.熔点:NaBr>NaCl>MgO |
| C.熔点:金刚石>硅>碳化硅 | D.热稳定性:HF>H2O>NH3 |
您最近一年使用:0次
名校
解题方法
4 . 下列关于晶体结构或性质的描述正确的是
| A.原子晶体中共价键越强,熔点越高 |
| B.金属晶体的熔点都比分子晶体的熔点高 |
| C.金属阳离子只能存在于离子晶体中 |
| D.分子晶体的熔、沸点低,常温下均呈液态或气态 |
您最近一年使用:0次
5 . GaAs晶体被业内称为“半导体贵族”,2001年7月31日,我国科学家宣布掌握其生产技术,中国称为继日本个德国之后第三个拥有此项技术的国家。他的熔点很高,硬度很大。其原子间以共价键(配位键)相连,密度为 ,Ga和As的摩尔质量分别为
,Ga和As的摩尔质量分别为 、
、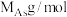 ,原子半径分别为
,原子半径分别为 、
、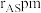 ,阿伏加德罗常数值为
,阿伏加德罗常数值为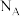 ,其晶胞结构如图所示。
,其晶胞结构如图所示。
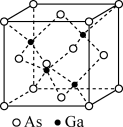
下列说法错误的是
 ,Ga和As的摩尔质量分别为
,Ga和As的摩尔质量分别为 、
、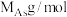 ,原子半径分别为
,原子半径分别为 、
、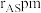 ,阿伏加德罗常数值为
,阿伏加德罗常数值为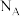 ,其晶胞结构如图所示。
,其晶胞结构如图所示。
下列说法错误的是
| A.该晶体为共价晶体 |
| B.在该晶体中Ga和As的配位数均为4 |
| C.不是所有原子均满足8电子稳定结构 |
D.原子的体积占晶胞体积的百分率为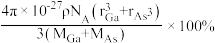 |
您最近一年使用:0次
名校
6 . 下列物质的性质不能 用化学键解释的是
| A.金属铜具有导电性 | B.氮气化学性质稳定 |
| C.金刚石硬度大 | D.碘单质常温为固体 |
您最近一年使用:0次
2022-03-25更新
|
457次组卷
|
3卷引用:北京市丰台区2022届高三一模化学试题
解题方法
7 . 下列有关比较正确的是
A.熔点: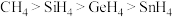 | B.熔点:NaBr>NaCl>MgO |
C.键的极性: 键> 键> 键> 键> 键 键 | D.热稳定性: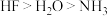 |
您最近一年使用:0次
2022-03-24更新
|
303次组卷
|
3卷引用:浙江省“南太湖”联盟2021-2022学年高二下学期第一次联考化学试题
名校
解题方法
8 . 在节能减排的大背景下,2022年北京冬奥会首次大规模采用了清洁低碳的二氧化碳跨临界直冷制冰技术,倾力呈现“更快、更美、更环保的冰”。
(1)二氧化碳易升华,其分子堆积方式为___ ,可以像氟利昂或_____ (10电子微粒,写名称)一样作为制冷剂。
(2)研究发现,在40GPa的高压下,用激光加热到1800K,会得到二氧化碳的立体网状结构,硬度大、熔沸点高,即该条件下变成____ (晶体类型)。
(3)CO2作制冷剂,能将液态水转化为固态冰,请解释这一变化过程中水的密度变小的原因____ 。
(4)已知H2O、H2S、NH3、CH4的VSEPR模型相同,其键角由小到大的顺序___ ,影响该条件下键角大小的因素主要有两方面:___ 、___ 。
(1)二氧化碳易升华,其分子堆积方式为
(2)研究发现,在40GPa的高压下,用激光加热到1800K,会得到二氧化碳的立体网状结构,硬度大、熔沸点高,即该条件下变成
(3)CO2作制冷剂,能将液态水转化为固态冰,请解释这一变化过程中水的密度变小的原因
(4)已知H2O、H2S、NH3、CH4的VSEPR模型相同,其键角由小到大的顺序
您最近一年使用:0次
9 . GaAs的熔点为1238℃,其晶胞结构如图所示,下列说法错误的是


| A.该晶体中普通共价键与配位键的个数比为3:1 |
| B.GaAs晶体属于共价晶体 |
| C.该晶胞中在面对角线方向上三个As原子相切 |
| D.该晶体固态和熔融状态都不导电 |
您最近一年使用:0次
2022-03-16更新
|
244次组卷
|
2卷引用:河北省石家庄市第二中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
10 . 据美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,制得具有高熔点、高硬度的二氧化碳晶体。下列关于该晶体的说法正确的是
| A.该晶体属于分子晶体 |
| B.该晶体易汽化,可用作制冷材料 |
| C.该晶体的熔沸点低于二氧化硅晶体 |
| D.一定条件下,该晶体可跟氢氧化钠反应 |
您最近一年使用:0次



