1 . 锰的化合物用途与性质的探究,有关物质及颜色: (白色)、
(白色)、 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。回答问题:
(紫色)。回答问题:
Ⅰ.用 溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
(1)操作Ⅰ为______ ,操作Ⅱ为______ 。
(2)无色液体A是______ ,.定性检验A的试剂是______ ,现象是____________ 。
(3)该同学推测白色固体B是苯甲酸与少量KCl的混合物,简述提纯过程____________ 。
Ⅱ.探究 在一定条件下被
在一定条件下被 或
或 氧化成的产物,实验装置如图(夹持装置略):
氧化成的产物,实验装置如图(夹持装置略): 前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入
前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入 后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
实验ⅱ:物质a为40% KOH溶液,C中通入 前后与实验ⅰ现象一样。
前后与实验ⅰ现象一样。
(4)通入 前,C中沉淀由白色变为黑色的化学方程式为
前,C中沉淀由白色变为黑色的化学方程式为____________ 。
(5) 的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是
的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是____________ 。
(6)浓碱条件下, 可被
可被 还原为
还原为 。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为
。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为____________ 。
(7)从反应速率的角度,分析实验ⅱ未得到绿色溶液的可能原因____________ 。
 (白色)、
(白色)、 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。回答问题:
(紫色)。回答问题:Ⅰ.用
 溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。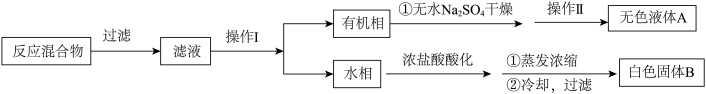
(1)操作Ⅰ为
(2)无色液体A是
(3)该同学推测白色固体B是苯甲酸与少量KCl的混合物,简述提纯过程
Ⅱ.探究
 在一定条件下被
在一定条件下被 或
或 氧化成的产物,实验装置如图(夹持装置略):
氧化成的产物,实验装置如图(夹持装置略):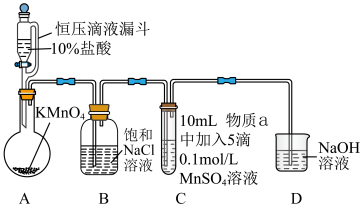
 前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入
前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入 后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。实验ⅱ:物质a为40% KOH溶液,C中通入
 前后与实验ⅰ现象一样。
前后与实验ⅰ现象一样。(4)通入
 前,C中沉淀由白色变为黑色的化学方程式为
前,C中沉淀由白色变为黑色的化学方程式为(5)
 的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是
的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是(6)浓碱条件下,
 可被
可被 还原为
还原为 。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为
。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为(7)从反应速率的角度,分析实验ⅱ未得到绿色溶液的可能原因
您最近一年使用:0次
2 . (Ⅰ)某温度时,在一个 的密闭容器中,
的密闭容器中, 三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白:
三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白:_______  时,到达反应最大限度;
时,到达反应最大限度;
(2)从开始到反应最大限度时间内, 的平均反应速率为
的平均反应速率为_______ ;
(3)该反应的化学方程式为_______ ;
(4)该反应达到平衡时, 的转化率为
的转化率为_______ ;
(5)该反应达到平衡时, 的体积分数为
的体积分数为_______ ;
(Ⅱ)在一固定容积的密闭容器中,进行反应:
(6)若容器容积为 ,反应
,反应 氢气质量增加
氢气质量增加 ,则该时间内一氧化碳的反应速率为
,则该时间内一氧化碳的反应速率为_______ 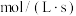 ;
;
(7)若增加碳的量,则正反应速率_______ ;(选填“增大”、“减小”、“不变”)
(8)该反应达到平衡状态的标志是_______ 。
a.混合气体的总压强不再变化
b.
c.混合气体的密度不再变化
d.
 的密闭容器中,
的密闭容器中, 三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白:
三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白: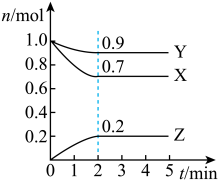
 时,到达反应最大限度;
时,到达反应最大限度;(2)从开始到反应最大限度时间内,
 的平均反应速率为
的平均反应速率为(3)该反应的化学方程式为
(4)该反应达到平衡时,
 的转化率为
的转化率为(5)该反应达到平衡时,
 的体积分数为
的体积分数为(Ⅱ)在一固定容积的密闭容器中,进行反应:

(6)若容器容积为
 ,反应
,反应 氢气质量增加
氢气质量增加 ,则该时间内一氧化碳的反应速率为
,则该时间内一氧化碳的反应速率为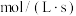 ;
;(7)若增加碳的量,则正反应速率
(8)该反应达到平衡状态的标志是
a.混合气体的总压强不再变化
b.

c.混合气体的密度不再变化
d.

您最近一年使用:0次
3 . (Ⅰ)氢氧燃料电池以 溶液作电解质溶液时,
溶液作电解质溶液时,
(1)负极反应式为_______ 。
(2)正极反应式为_______ 。
(Ⅱ)按要求回完成以下化学反应:
(3)氯乙烯发生加聚反应的化学方程式_______ 。
(4)乙烯通入溴水的化学方程式为_______ 。
(5)乙酸和乙醇的酯化反应的化学方程式_______ 。
(Ⅲ)t℃时,将 气体A和1mol气体B充入容积为
气体A和1mol气体B充入容积为 的恒容密闭容器中,发生如下反应:
的恒容密闭容器中,发生如下反应: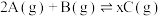 ,2min时化学反应达到限度(温度仍为t℃),此时B还有
,2min时化学反应达到限度(温度仍为t℃),此时B还有 ,并测得C的浓度为
,并测得C的浓度为 ,请回答下列问题:
,请回答下列问题:
(6)判断该反应达到限度的标志是_______ 。
a.容器中的压强保持不变
b.A的生成速率与B的消耗速率之比为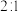
c.容器内混合气体的密度保持不变
d.A的百分含量保持不变
e.B和C的物质的量浓度之比为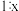
(7)保持温度不变增大容器体积,则正反应速率_______ (填“增大”、“减小”或“不变”)。
(8)化学反应达到限度时,A的转化率为_______ 。
 溶液作电解质溶液时,
溶液作电解质溶液时,(1)负极反应式为
(2)正极反应式为
(Ⅱ)按要求回完成以下化学反应:
(3)氯乙烯发生加聚反应的化学方程式
(4)乙烯通入溴水的化学方程式为
(5)乙酸和乙醇的酯化反应的化学方程式
(Ⅲ)t℃时,将
 气体A和1mol气体B充入容积为
气体A和1mol气体B充入容积为 的恒容密闭容器中,发生如下反应:
的恒容密闭容器中,发生如下反应: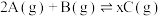 ,2min时化学反应达到限度(温度仍为t℃),此时B还有
,2min时化学反应达到限度(温度仍为t℃),此时B还有 ,并测得C的浓度为
,并测得C的浓度为 ,请回答下列问题:
,请回答下列问题:(6)判断该反应达到限度的标志是
a.容器中的压强保持不变
b.A的生成速率与B的消耗速率之比为
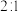
c.容器内混合气体的密度保持不变
d.A的百分含量保持不变
e.B和C的物质的量浓度之比为
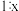
(7)保持温度不变增大容器体积,则正反应速率
(8)化学反应达到限度时,A的转化率为
您最近一年使用:0次
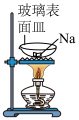
4 . 如图实验仪器或装置能达到实验目的的是
|
|
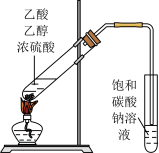
| A.钠的燃烧 | B.制备乙酸乙酯 |
|
|
C.制备 | D.收集 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列有关有机化合物的说法不正确的是
| A.用酸性高锰酸钾溶液可以区分烷烃和烯烃 | B.乙烷与乙烯可用溴水鉴别 |
| C.除去乙烷中的乙烯可通入酸性高锰酸钾溶液 | D. 有4种同分异构体 有4种同分异构体 |
您最近一年使用:0次
6 . 下列物质在光照条件下,可以和 发生取代反应的是
发生取代反应的是
 发生取代反应的是
发生取代反应的是| A.液溴 | B.氯水 | C.氧气 | D.酸性 溶液 溶液 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法中不正确 的是
| A.硫难溶于水,微溶于酒精,易溶于CS2,说明分子极性:H2O>C2H5OH>CS2 |
| B.热稳定性:H2O>H2S说明水分子间存在氢键作用 |
| C.CCl2F2无同分异构体,说明其中碳原子采取sp3杂化 |
| D.由于甲基(-CH3)是推电子基团,甲酸的pKa小于乙酸的pKa。 |
您最近一年使用:0次
昨日更新
|
54次组卷
|
2卷引用:天津市滨海新区塘沽第一中学2023-2024学年高二下学期期中考试化学试卷
名校
解题方法
8 . 一定条件下, 与
与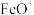 反应合成
反应合成 的反应历程如图所示。已知其他条件不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。说明:过渡态中“- -”表示化学键未完全断裂或形成。下列说法正确的是
的反应历程如图所示。已知其他条件不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。说明:过渡态中“- -”表示化学键未完全断裂或形成。下列说法正确的是
 与
与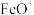 反应合成
反应合成 的反应历程如图所示。已知其他条件不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。说明:过渡态中“- -”表示化学键未完全断裂或形成。下列说法正确的是
的反应历程如图所示。已知其他条件不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。说明:过渡态中“- -”表示化学键未完全断裂或形成。下列说法正确的是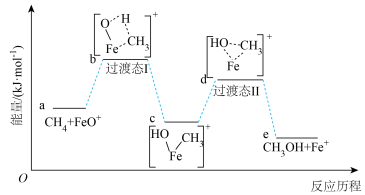
| A.反应历程中的两个反应均涉及氢原子的成键 |
B.相同条件下, 与 与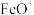 发生上述反应,则其过渡态 发生上述反应,则其过渡态 的能量比 的能量比 高 高 |
C.该反应的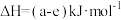 |
D.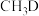 与 与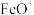 发生上述反应,只能获得1种相对分子质量的有机产物 发生上述反应,只能获得1种相对分子质量的有机产物 |
您最近一年使用:0次
7日内更新
|
61次组卷
|
4卷引用:化学(天津卷02)-2024年高考化学押题预测卷
(已下线)化学(天津卷02)-2024年高考化学押题预测卷广东省2024届高三下学期二模考试化学试题贵州省贵阳市清华中学2024届高三下5月模拟预测考前考(二)化学试题江苏省无锡市锡东高级中学2023-2024学年高二下学期5月月考化学试题
名校
9 . 下列方程式不能准确解释相应实验现象的是
A.MnO2和浓盐酸共热产生黄绿色气体:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| B.二氧化硫通入硝酸钡溶液中,产生白色沉淀:SO2+Ba2++H2O=BaSO3↓+2H+ |
| C.用FeCl3溶液清洗银镜:Fe3++Ag+Cl-=Fe2++AgCl |
D.[Cu(H2O)4]2+(aq)(蓝色)+4Cl-(ag)=[CuCl4]2-(ag)(黄色)+4H2O(l)  H>0,升温,溶液变为黄绿色 H>0,升温,溶液变为黄绿色 |
您最近一年使用:0次
7日内更新
|
89次组卷
|
2卷引用:天津市新华中学2024届高三下学期统练11化学 试题
10 . 一定温度时,在 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:___________ , 时刻N的转化率为
时刻N的转化率为___________ 。
(2)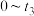 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为___________  。
。
(3)下列能表示上述反应达到化学平衡状态的是___________(填编号)。
(4)已知:H—H的键能为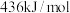 ,N—H的键能为
,N—H的键能为 ,生成
,生成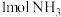 过程中放出
过程中放出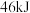 的热量。则
的热量。则 的键能为
的键能为___________  。
。
(5)化学反应速率受到很多因素的影响,例如:实验室制取氢气时一般用粗锌(含铁)代替纯锌和稀硫酸反应,这是利用___________ 原理加快了氢气生成的速率。
 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示: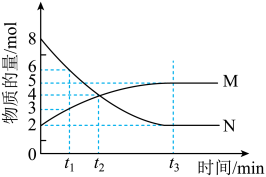
 时刻N的转化率为
时刻N的转化率为(2)
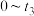 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为 。
。(3)下列能表示上述反应达到化学平衡状态的是___________(填编号)。
A. | B.M与N的物质的量之比保持不变 |
| C.各物质浓度保持不变 | D.每消耗 ,同时生成 ,同时生成 |
(4)已知:H—H的键能为
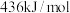 ,N—H的键能为
,N—H的键能为 ,生成
,生成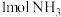 过程中放出
过程中放出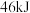 的热量。则
的热量。则 的键能为
的键能为 。
。(5)化学反应速率受到很多因素的影响,例如:实验室制取氢气时一般用粗锌(含铁)代替纯锌和稀硫酸反应,这是利用
您最近一年使用:0次