1 .  俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备
俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备 并测定摩尔盐中
并测定摩尔盐中 的含量。已知:
的含量。已知:
三种盐的溶解度(单位为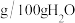 )
)
回答下列问题:
(1)制备硫酸亚铁(装置如图所示):称取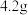 洗净的铁粉(含
洗净的铁粉(含 质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入
质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入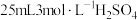 溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入
溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入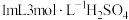 溶液,趁热过滤得
溶液,趁热过滤得 溶液。
溶液。______________________ ;装置b中所盛试剂的作用是______________________ 。
②若不及时向锥形瓶中补加水,导致硫酸浓度过大,可能造成的不良后果为______________________ 。
(2)在 的条件下,称取
的条件下,称取 晶体
晶体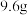 ,将其溶于
,将其溶于___________________  (结果保留一位小数,此温度下的水的密度近似为
(结果保留一位小数,此温度下的水的密度近似为 )水中,配成饱和溶液。
)水中,配成饱和溶液。
(3)将(2)中所配的 饱和溶液加入(1)所得
饱和溶液加入(1)所得 溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到
溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到 晶体,抽滤、洗涤得产品.洗涤的具体操作为
晶体,抽滤、洗涤得产品.洗涤的具体操作为_____________ 。
(4)测定产品中 的含量:称取
的含量:称取 产品,溶于水配成溶液并加入稀硫酸,用
产品,溶于水配成溶液并加入稀硫酸,用 的
的 标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗
标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗 标准溶液的体积为
标准溶液的体积为 。
。
①滴定反应的离子方程式为___________________ 。
②产品中 的质量分数为
的质量分数为____________________ 。
③若滴定终点时俯视读数,会使测定结果_____________ (填“偏低”或“偏高”)。
 俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备
俗称摩尔盐,是一种蓝绿色的无机复盐,不溶于酒精。在实验室以铁粉、稀硫酸、硫酸铵为原料制备 并测定摩尔盐中
并测定摩尔盐中 的含量。已知:
的含量。已知:三种盐的溶解度(单位为
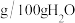 )
)温度/℃ |
|
|
|
10 | 20.0 | 73 | 17.2 |
20 | 26.5 | 75.4 | 21.6 |
30 | 32.9 | 78 | 28.1 |
(1)制备硫酸亚铁(装置如图所示):称取
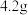 洗净的铁粉(含
洗净的铁粉(含 质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入
质量分数为2.3%)加入锥形瓶中。向锥形瓶中加入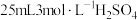 溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入
溶液,开始反应,加热,振荡,反应过程中适当补充水,防止硫酸浓度变大。然后再向锥形瓶中加入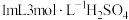 溶液,趁热过滤得
溶液,趁热过滤得 溶液。
溶液。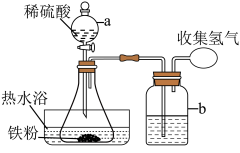
②若不及时向锥形瓶中补加水,导致硫酸浓度过大,可能造成的不良后果为
(2)在
 的条件下,称取
的条件下,称取 晶体
晶体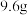 ,将其溶于
,将其溶于 (结果保留一位小数,此温度下的水的密度近似为
(结果保留一位小数,此温度下的水的密度近似为 )水中,配成饱和溶液。
)水中,配成饱和溶液。(3)将(2)中所配的
 饱和溶液加入(1)所得
饱和溶液加入(1)所得 溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到
溶液中,搅拌,小火加热,在蒸发皿中蒸发浓缩得到 晶体,抽滤、洗涤得产品.洗涤的具体操作为
晶体,抽滤、洗涤得产品.洗涤的具体操作为(4)测定产品中
 的含量:称取
的含量:称取 产品,溶于水配成溶液并加入稀硫酸,用
产品,溶于水配成溶液并加入稀硫酸,用 的
的 标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗
标准溶液进行滴定(杂质不参加反应),达到滴定终点时,消耗 标准溶液的体积为
标准溶液的体积为 。
。①滴定反应的离子方程式为
②产品中
 的质量分数为
的质量分数为③若滴定终点时俯视读数,会使测定结果
您最近一年使用:0次
名校
2 . 某铜合金中 的质量分数为80%~90%,还含有
的质量分数为80%~90%,还含有 等。通常用间接碘量法测定其中
等。通常用间接碘量法测定其中 的含量,步骤如下:
的含量,步骤如下:
1.称取 样品,加入稀
样品,加入稀 和
和 溶液使其溶解,煮沸除去过量的
溶液使其溶解,煮沸除去过量的 ,冷却后过滤,将滤液配制成
,冷却后过滤,将滤液配制成 溶液;
溶液;
Ⅱ.取 滤液于锥形瓶中,加入
滤液于锥形瓶中,加入 溶液,将溶液中的
溶液,将溶液中的 转化为无色稳定的
转化为无色稳定的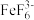 ,充分反应后,加入过量的
,充分反应后,加入过量的 溶液,生成白色沉淀,加入淀粉做指示剂;
溶液,生成白色沉淀,加入淀粉做指示剂;
Ⅲ.向Ⅱ的锥形瓶中加入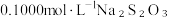 溶液滴定,发生反应:
溶液滴定,发生反应:
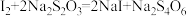 (无色);
(无色);
Ⅳ.平行测定四次,四次滴定实验消耗 标准溶液体积读数如下表所示:
标准溶液体积读数如下表所示:
V.计算铜的质量分数。
已知: 为白色难溶于水的难溶物。
为白色难溶于水的难溶物。
(1)盛装 溶液,应选择下图中的
溶液,应选择下图中的_____________ (填“a”或“b”)。

(2)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):_______
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.烘干 B.装入滴定液至零刻度以上 C.调整滴定液液面至零刻度或零刻度以下 D.用量筒量取一定体积的溶液倒入锥形瓶中 E.排除气泡 F.用滴定液润洗2至3次G记录起始读数
(3)Ⅱ中 和
和 反应生成
反应生成 白色沉淀和
白色沉淀和 。
。 和
和 反应的离子方程式是
反应的离子方程式是_____________ 。
(4)滴定终点的现象_____________ 。
(5)Ⅳ所消耗的 标准溶液平均体积为
标准溶液平均体积为_____________  ,V计算得到样品中
,V计算得到样品中 的质量分数为
的质量分数为_____________ (结果保留两位小数)。
(6)以下操作造成铜的含量偏高的是_____________ 。
A.滴定管未用标准溶液润洗
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
F.步骤Ⅱ中未加入 溶液
溶液
 的质量分数为80%~90%,还含有
的质量分数为80%~90%,还含有 等。通常用间接碘量法测定其中
等。通常用间接碘量法测定其中 的含量,步骤如下:
的含量,步骤如下:1.称取
 样品,加入稀
样品,加入稀 和
和 溶液使其溶解,煮沸除去过量的
溶液使其溶解,煮沸除去过量的 ,冷却后过滤,将滤液配制成
,冷却后过滤,将滤液配制成 溶液;
溶液;Ⅱ.取
 滤液于锥形瓶中,加入
滤液于锥形瓶中,加入 溶液,将溶液中的
溶液,将溶液中的 转化为无色稳定的
转化为无色稳定的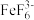 ,充分反应后,加入过量的
,充分反应后,加入过量的 溶液,生成白色沉淀,加入淀粉做指示剂;
溶液,生成白色沉淀,加入淀粉做指示剂;Ⅲ.向Ⅱ的锥形瓶中加入
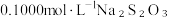 溶液滴定,发生反应:
溶液滴定,发生反应: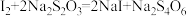 (无色);
(无色);Ⅳ.平行测定四次,四次滴定实验消耗
 标准溶液体积读数如下表所示:
标准溶液体积读数如下表所示:| 滴定次数 | 待测溶液的体积/ |  溶液的体积/ 溶液的体积/ | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 50.00 | 0.00 | 18.02 |
| 第二次 | 50.00 | 0.56 | 18.96 |
| 第三次 | 50.00 | 0.22 | 18.20 |
| 第四次 | 50.00 | 0.35 | 18.35 |
已知:
 为白色难溶于水的难溶物。
为白色难溶于水的难溶物。(1)盛装
 溶液,应选择下图中的
溶液,应选择下图中的
(2)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.烘干 B.装入滴定液至零刻度以上 C.调整滴定液液面至零刻度或零刻度以下 D.用量筒量取一定体积的溶液倒入锥形瓶中 E.排除气泡 F.用滴定液润洗2至3次G记录起始读数
(3)Ⅱ中
 和
和 反应生成
反应生成 白色沉淀和
白色沉淀和 。
。 和
和 反应的离子方程式是
反应的离子方程式是(4)滴定终点的现象
(5)Ⅳ所消耗的
 标准溶液平均体积为
标准溶液平均体积为 ,V计算得到样品中
,V计算得到样品中 的质量分数为
的质量分数为(6)以下操作造成铜的含量偏高的是
A.滴定管未用标准溶液润洗
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
F.步骤Ⅱ中未加入
 溶液
溶液
您最近一年使用:0次
名校
解题方法
3 . 工业上用粉碎的黄铁矿(主要成分可表示为 ,其中还有少量
,其中还有少量 等)为原料制备硫酸的流程如图:
等)为原料制备硫酸的流程如图:
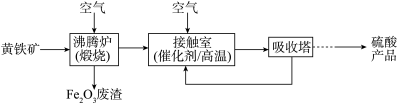
回答下列问题:
(1)硫酸厂沸腾炉排出的矿渣中含有 、CuO,请写出煅烧
、CuO,请写出煅烧 的化学方程式
的化学方程式___________ ,为提高生产效率,工业生产中我们会采用一定的办法加快反应速率,你认为上述流程中能加快速率的做法有___________ (至少写出两条)。
(2)在接触室中发生的是 的催化氧化反应,该反应属于
的催化氧化反应,该反应属于___________ (填字母)。
a.氧化还原反应 b.离子反应 c.化合反应 d.可逆反应
(3)为提高原料的转化率,并减少污染物的产生,落实绿色化学思想,上述流程中可循环利用的物质有___________ 。
(4)国家规定由吸收塔排出的尾气中 的最高含量不得超过
的最高含量不得超过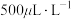 ,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物
,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物 可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:
可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:___________ ,___________ 。
(5)用含硫质量分数为a%的硫铁矿制硫酸,若高温煅烧时损失b%的硫元素,由 制
制 的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为
的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为___________ 吨(列出表达式即可,不必化简)。
 ,其中还有少量
,其中还有少量 等)为原料制备硫酸的流程如图:
等)为原料制备硫酸的流程如图:
回答下列问题:
(1)硫酸厂沸腾炉排出的矿渣中含有
 、CuO,请写出煅烧
、CuO,请写出煅烧 的化学方程式
的化学方程式(2)在接触室中发生的是
 的催化氧化反应,该反应属于
的催化氧化反应,该反应属于a.氧化还原反应 b.离子反应 c.化合反应 d.可逆反应
(3)为提高原料的转化率,并减少污染物的产生,落实绿色化学思想,上述流程中可循环利用的物质有
(4)国家规定由吸收塔排出的尾气中
 的最高含量不得超过
的最高含量不得超过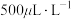 ,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物
,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物 可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:
可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:(5)用含硫质量分数为a%的硫铁矿制硫酸,若高温煅烧时损失b%的硫元素,由
 制
制 的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为
的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题
(1)下面列出了几组物质,请将物质的合适组号填写在表中。
①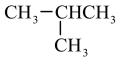 和
和 ;②
;② 和
和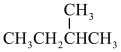 ;③
;③ 和
和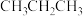 ;④金刚石与石墨;⑤氕、氘与氚;⑥
;④金刚石与石墨;⑤氕、氘与氚;⑥ 、
、 和
和 ;⑦乙醇(
;⑦乙醇( )和二甲醚(
)和二甲醚( ):③氧气(
):③氧气( )与臭氧(
)与臭氧( )。
)。
(2)写出下列有机化合物含有官能团的名称:
①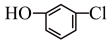
_______ 。
②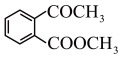
_______ 。
(3)下图是化学实验室浓盐酸试剂标签上的部分内容。
丁同学计划用该浓盐酸配制1mol/L的稀盐酸,现实验仅需要稀盐酸450mL,可供选用的仪器有:①胶头滴管;②烧瓶:③烧杯:④药匙:⑤玻璃棒;⑤量筒。
请回答下列问题:
①配制稀盐酸时,还缺少的仪器有_______ 。
②经计算,配制1mol/L的稀盐酸需要量取上述浓盐酸的体积为_______ mL(结果保留1位小数)。
③测定所配制的稀盐酸,发现其浓度大于1mol/L,引起误差的原因可能是_______ 。
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
B.定容时俯视容量瓶刻度线
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)铋酸钠( )在酸性溶液中具有很强的氧化性,可用于测定钢铁试样中锰的含量。完成并配平下列反应方程式,并用单线桥标出电子转移的方向和数目
)在酸性溶液中具有很强的氧化性,可用于测定钢铁试样中锰的含量。完成并配平下列反应方程式,并用单线桥标出电子转移的方向和数目_______ 。
_______ _______
_______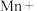 _______
_______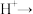 _______
_______ _______
_______ _______
_______
(5)同学检测到该溶液中含有大量的 、
、 、
、 ,若向1L该混合溶液中通入一定量的
,若向1L该混合溶液中通入一定量的 ,溶液中
,溶液中 、
、 、
、 的物质的量与通入
的物质的量与通入 的体积(标准状况)的关系如下表所示,分析后回答下列问题:
的体积(标准状况)的关系如下表所示,分析后回答下列问题:
原溶液中 、
、 、
、 的物质的量浓度之比为
的物质的量浓度之比为_______ 。
(1)下面列出了几组物质,请将物质的合适组号填写在表中。
①
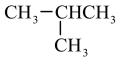 和
和 ;②
;② 和
和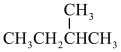 ;③
;③ 和
和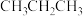 ;④金刚石与石墨;⑤氕、氘与氚;⑥
;④金刚石与石墨;⑤氕、氘与氚;⑥ 、
、 和
和 ;⑦乙醇(
;⑦乙醇( )和二甲醚(
)和二甲醚( ):③氧气(
):③氧气( )与臭氧(
)与臭氧( )。
)。| 类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 |
①

②

(3)下图是化学实验室浓盐酸试剂标签上的部分内容。
盐酸化学纯(CP) (500mL) 品名:盐酸 化学式:HCl 相对分子质量:36.5 密度:1.18g/cm3 质量分数:36.5% |
请回答下列问题:
①配制稀盐酸时,还缺少的仪器有
②经计算,配制1mol/L的稀盐酸需要量取上述浓盐酸的体积为
③测定所配制的稀盐酸,发现其浓度大于1mol/L,引起误差的原因可能是
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
B.定容时俯视容量瓶刻度线
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)铋酸钠(
 )在酸性溶液中具有很强的氧化性,可用于测定钢铁试样中锰的含量。完成并配平下列反应方程式,并用单线桥标出电子转移的方向和数目
)在酸性溶液中具有很强的氧化性,可用于测定钢铁试样中锰的含量。完成并配平下列反应方程式,并用单线桥标出电子转移的方向和数目_______
 _______
_______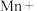 _______
_______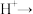 _______
_______ _______
_______ _______
_______(5)同学检测到该溶液中含有大量的
 、
、 、
、 ,若向1L该混合溶液中通入一定量的
,若向1L该混合溶液中通入一定量的 ,溶液中
,溶液中 、
、 、
、 的物质的量与通入
的物质的量与通入 的体积(标准状况)的关系如下表所示,分析后回答下列问题:
的体积(标准状况)的关系如下表所示,分析后回答下列问题: 的体积(标准状况) 的体积(标准状况) | 11.2L | 22.4L | 28.0L |
 | 2.5mol | 3.5mol | 4.0mol |
 | 3.0mol | 2.5mol | 2.0mol |
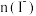 | xmol | 0 | 0 |
 、
、 、
、 的物质的量浓度之比为
的物质的量浓度之比为
您最近一年使用:0次
名校
5 . 三氧化二铬(Cr2O3)可用作着色剂、分析试剂、催化剂等。一种利用铬铁矿(主要成分为FeO、Cr2O3,还含有Al2O3、SiO2等杂质)清洁生产Cr2O3的工艺流程如下:

已知:①铬铁矿的成分及含量(以氧化物形式表示):
②金属离子开始沉淀与完全沉淀的pH如下:
③铬酸酐(CrO3)常用作氧化剂;
④铁铵矾的化学式为NH4Fe(SO4)2·12H2O,在pH =3时完全沉淀。回答下列问题:
(1)“氧化酸浸”前,常将铬铁矿粉碎,目的是___________ , 滤渣1的成分是___________ 。
(2)铬酸酐的作用是___________ ,“氧化酸浸”时FeO·Cr2O3反应的化学方程式是___________ 。
(3)“沉淀”时,应调节pH不低于___________ ,滤液1的成分主要是______ (填化学式)
(4)“除铝”一步的离子方程式是___________ 。
(5)若处理1kg铬铁矿,至少需要消耗铬酸酐的质量是___________ g。(保留一位小数)

已知:①铬铁矿的成分及含量(以氧化物形式表示):
| 成分 | Cr2O3 | FeO | SiO2 | Al2O3 | 其他 |
| 质量分数 | 45.0% | 32.5% | 11.5% | 10.8% | 0.2% |
| 金属离子 | Fe3+ | Al3+ | Cr3+ | Fe2+ |
| 开始沉淀的pH | 2.7 | 3.4 | 5.0 | 7.5 |
| 完全沉淀的pH | 3.7 | 4.9 | 5.9 | 9.7 |
④铁铵矾的化学式为NH4Fe(SO4)2·12H2O,在pH =3时完全沉淀。回答下列问题:
(1)“氧化酸浸”前,常将铬铁矿粉碎,目的是
(2)铬酸酐的作用是
(3)“沉淀”时,应调节pH不低于
(4)“除铝”一步的离子方程式是
(5)若处理1kg铬铁矿,至少需要消耗铬酸酐的质量是
您最近一年使用:0次
2022-06-05更新
|
402次组卷
|
3卷引用:黑龙江省双鸭山市第一中学2022-2023学年高三上学期开学考试化学试题
名校
6 . 碳酸钠是一种重要的无机化工原料,以“侯氏制碱法”为原理,实验室中用碳酸氢铵和粗盐(含有MgCl2、CaCl2)制备碳酸钠,并测定其含量。回答下列问题:
I.碳酸钠的制备
制备流程如图所示。
(1)滤渣的成分有____ 。
(2)写出灼烧碳酸氢钠的化学方程式____ 。
(3)根据相关物质的溶解度随温度的变化曲线(如图所示),制备NaHCO3时反应温度控制在30~35℃之间,温度过高或者过低都不利于反应进行,原因是____ 。____ 、____ 、洗涤、干燥。
II.碳酸钠含量分析
称取制备的碳酸钠2.00g,配制成250mL溶液,取25.00mL于锥形瓶中,加入2滴某指示剂,用0.1000mol/L盐酸滴定至第一滴定终点,消耗16.00mL盐酸。再加入2滴甲基橙,继续滴加盐酸,溶液由黄色变为橙色后,加热煮沸1~2min,冷却后溶液又变为黄色,继续用盐酸滴定,溶液重新变为橙色,直至加热不褪色即为第二滴定终点,最终共消耗34.00mL盐酸。
(5)第一滴定终点的现象为____ 。
(6)滴定过程中加热煮沸溶液的目的是____ ,若不煮沸,测得Na2CO3的质量分数____ (填“偏高”、“偏低”或“无影响”)
(7)产品中Na2CO3的质量分数为____ ,NaHCO3的质量分数为____ 。
I.碳酸钠的制备
制备流程如图所示。

(1)滤渣的成分有
(2)写出灼烧碳酸氢钠的化学方程式
(3)根据相关物质的溶解度随温度的变化曲线(如图所示),制备NaHCO3时反应温度控制在30~35℃之间,温度过高或者过低都不利于反应进行,原因是

II.碳酸钠含量分析
称取制备的碳酸钠2.00g,配制成250mL溶液,取25.00mL于锥形瓶中,加入2滴某指示剂,用0.1000mol/L盐酸滴定至第一滴定终点,消耗16.00mL盐酸。再加入2滴甲基橙,继续滴加盐酸,溶液由黄色变为橙色后,加热煮沸1~2min,冷却后溶液又变为黄色,继续用盐酸滴定,溶液重新变为橙色,直至加热不褪色即为第二滴定终点,最终共消耗34.00mL盐酸。
(5)第一滴定终点的现象为
(6)滴定过程中加热煮沸溶液的目的是
(7)产品中Na2CO3的质量分数为
您最近一年使用:0次
2022-05-29更新
|
306次组卷
|
2卷引用:黑龙江省哈尔滨市第三中学校2022届高三第五次模拟考试理科综合化学试题
名校
解题方法
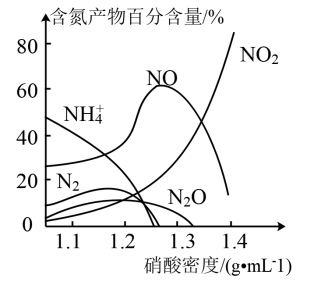
7 . 铁与不同密度的 溶液反应时产生的含氮产物的百分含量分布如图所示,硝酸的密度与其质量分数的对应关系见下表,下列有关说法错误的是
溶液反应时产生的含氮产物的百分含量分布如图所示,硝酸的密度与其质量分数的对应关系见下表,下列有关说法错误的是
 溶液反应时产生的含氮产物的百分含量分布如图所示,硝酸的密度与其质量分数的对应关系见下表,下列有关说法错误的是
溶液反应时产生的含氮产物的百分含量分布如图所示,硝酸的密度与其质量分数的对应关系见下表,下列有关说法错误的是
密度/ | 1.10 | 1.15 | 1.20 | 1.25 | 1.30 | 1.35 | 1.40 |
| 质量分数/% | 17.68 | 25.48 | 32.99 | 40.58 | 48.42 | 56.95 | 66.97 |
| A.上述反应中,铁为还原剂,硝酸为氧化剂 |
B. 、 、 、 、 、 、 都既有氧化性又有还原性 都既有氧化性又有还原性 |
C.随着硝酸的密度逐渐减小,产物中 的含量逐渐减小 的含量逐渐减小 |
D.当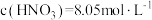 时,产物中 时,产物中 的含量最高 的含量最高 |
您最近一年使用:0次
2022-02-25更新
|
414次组卷
|
5卷引用:黑龙江省黑河市嫩江市高级中学等部分学校2021-2022学年高一下学期第一次月考化学试题
名校
解题方法
8 . 某实验小组利用下图装置模拟古法硫酸生产方法并进行SO2性质探究。

已知A中反应的化学方程式:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。
Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。
完成下列填空:
(1)C装置中覆盖食用油的目的是___________ ;D装置的作用___________ 。B中所得硫酸溶液的质量分数理论值为___________ (保留三位小数)。
为探究SO2与钡盐溶液的反应,在装置C中先后四次加入不同的溶液:
得到如下pH-t图:
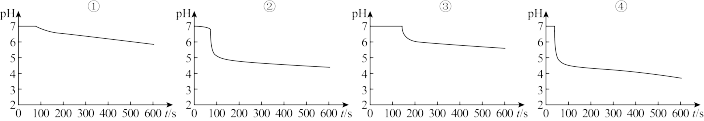
(2)曲线①呈缓慢下降趋势,这是因为___________ 。曲线②出现骤降,表明溶液中生成了___________ (填物质名称)。对比分析上述四组数据,可得出的结论是_________ (任写2条)。
(3)为对排气法收集到的SO2气体进行含量测定,将2240mL气体(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀21.436g。则SO2气体的体积分数为_______ 。若该实验数据较实际值偏大,则可能的原因是________ (选填编号)。
a.气体通入速率过快 b.沉淀未进行恒重操作
c.收集的气体中有CO2 d.未用食用油覆盖液面

已知A中反应的化学方程式:2FeSO4·7H2O
 Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。
Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。完成下列填空:
(1)C装置中覆盖食用油的目的是
为探究SO2与钡盐溶液的反应,在装置C中先后四次加入不同的溶液:
| ① | ② | ③ | ④ |
| 已煮沸的BaCl2溶液 | 未煮沸的BaCl2溶液 | 已煮沸的Ba(NO3)2溶液 | 未煮沸的Ba(NO3)2溶液 |
| 注:锥形瓶中溶液体积相同,钡盐溶液浓度相同;油层厚度一致,通入SO2流速一致。 | |||

(2)曲线①呈缓慢下降趋势,这是因为
(3)为对排气法收集到的SO2气体进行含量测定,将2240mL气体(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀21.436g。则SO2气体的体积分数为
a.气体通入速率过快 b.沉淀未进行恒重操作
c.收集的气体中有CO2 d.未用食用油覆盖液面
您最近一年使用:0次
2022-01-15更新
|
1078次组卷
|
3卷引用:黑龙江省哈尔滨市第九中学校2022届高考最后押题卷(一)化学试题
黑龙江省哈尔滨市第九中学校2022届高考最后押题卷(一)化学试题上海市浦东新区2022届高三一模化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)
名校
解题方法
9 . 山梨酸是国际上应用最广的防腐剂之一,实验室通过巴豆醛和丙酮缩合法制备山梨酸 反应原理:
反应原理:
③酸化反应
实验步骤:
①向三颈烧瓶中加入 丙酮、少量
丙酮、少量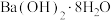 ,加热至丙酮出现回流时,在加热搅拌下缓慢滴入
,加热至丙酮出现回流时,在加热搅拌下缓慢滴入 巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。
巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。
②在室温下,将 溶液、20%
溶液、20% 溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用
溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用 处理水溶液中过量的
处理水溶液中过量的 。
。
③将质量分数为30%的稀 缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液
缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液 ,过滤、洗涤得山梨酸粗产品。
,过滤、洗涤得山梨酸粗产品。
④将适量蒸馏水加入粗产品中,加热溶解,冷却结晶,减压过滤,干燥后得到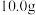 山梨酸。已知:
山梨酸。已知:
①山梨酸微溶于水,易溶于有机溶剂。易被强氧化剂HClO等氧化;
②部分有机物密度为:巴豆醛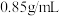 ,氯仿
,氯仿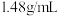 ,丙酮
,丙酮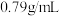 。
。
回答下列问题:
(1)步骤①分离出巴豆烯叉丙酮的装置如图1所示(加热及夹持装置省略),虚线框内连接的仪器为___________ (填名称),尾接管连接抽气泵的目的是___________ ,毛细管连通大气的主要作用是___________ 。___________ (填“a”或“b”)
(3)用 处理过量的
处理过量的 时反应的离子方程式为
时反应的离子方程式为___________ ;不可以在步骤③酸化后再加入 除去过量的
除去过量的 ,原因是
,原因是___________ 。
(4)步骤③中,检测洗涤是否完成的操作是___________ 。
(5)本实验中山梨酸的产率为___________ (保留3位有效数字)。
 反应原理:
反应原理:①缩合反应

③酸化反应

实验步骤:
①向三颈烧瓶中加入
 丙酮、少量
丙酮、少量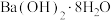 ,加热至丙酮出现回流时,在加热搅拌下缓慢滴入
,加热至丙酮出现回流时,在加热搅拌下缓慢滴入 巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。
巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。②在室温下,将
 溶液、20%
溶液、20% 溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用
溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用 处理水溶液中过量的
处理水溶液中过量的 。
。③将质量分数为30%的稀
 缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液
缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液 ,过滤、洗涤得山梨酸粗产品。
,过滤、洗涤得山梨酸粗产品。④将适量蒸馏水加入粗产品中,加热溶解,冷却结晶,减压过滤,干燥后得到
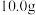 山梨酸。已知:
山梨酸。已知:①山梨酸微溶于水,易溶于有机溶剂。易被强氧化剂HClO等氧化;
②部分有机物密度为:巴豆醛
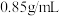 ,氯仿
,氯仿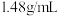 ,丙酮
,丙酮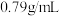 。
。回答下列问题:
(1)步骤①分离出巴豆烯叉丙酮的装置如图1所示(加热及夹持装置省略),虚线框内连接的仪器为

(3)用
 处理过量的
处理过量的 时反应的离子方程式为
时反应的离子方程式为 除去过量的
除去过量的 ,原因是
,原因是(4)步骤③中,检测洗涤是否完成的操作是
(5)本实验中山梨酸的产率为
您最近一年使用:0次
名校
解题方法
10 . 双氰胺( )为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮
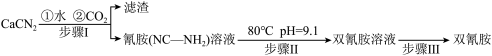
)为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮 为原料制备双氰胺的流程如下:
为原料制备双氰胺的流程如下:
已知氰胺二聚反应机理为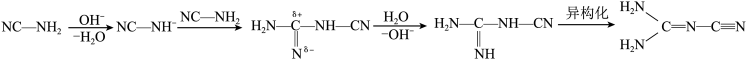
(1)已知:氰基是吸电子基团。氰氨
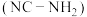 的碱性
的碱性(2)写出步骤Ⅰ的化学反应方程式:
(3)步骤Ⅱ中调节溶液pH为9.1,pH不能过低的原因:
(4)步骤Ⅲ中蒸发浓缩时,常采用真空蒸发浓缩,目的是
(5)凯氏定氮法是测定有机物中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐。
已知:
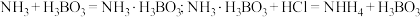

②仪器清洗后,g中加入硼酸
 和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭
和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭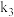 ,d中保留少量水。打开
,d中保留少量水。打开 ,加热b,使水蒸气进入e。
,加热b,使水蒸气进入e。d中保留少量水的目的是
③取双氰胺样品m克进行测定,滴定g中吸收液时消耗浓度为
 的盐酸VmL,则样品中氮的质量分数为
的盐酸VmL,则样品中氮的质量分数为
您最近一年使用:0次



