名校
1 . 下表为元素周期表的一部分,请参照元素在表中的位置,回答下列问题:
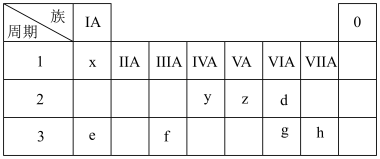
(1)比较d、e常见离子的半径大小(用化学式表示,下同):_______ >_______ ;
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:_______ >_______ 。
(3)用电子式表示e、g组成的简单化合物的形成过程:_______ 。
(4)下列说法不正确的是_______。
(5)由表中两种元素的原子按 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)_______ 。
(6)上述元素可组成盐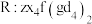 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
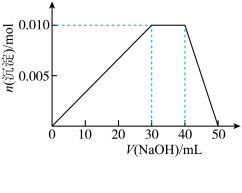
若向上述 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为_______  。
。

(1)比较d、e常见离子的半径大小(用化学式表示,下同):
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:
(3)用电子式表示e、g组成的简单化合物的形成过程:
(4)下列说法不正确的是_______。
A.最简单的氢化物的稳定性 |
B.最高价氧化物对应的水化物的碱性 |
| C.与y元素同主族的第四周期元素的单质是半导体材料 |
| D.y、h两元素组成的化合物中一定只含共价键 |
(5)由表中两种元素的原子按
 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)(6)上述元素可组成盐
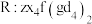 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
若向上述
 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为 。
。
您最近一年使用:0次
2 . 含氯、含钠化合物在生活、生产中随处可见。回答下列问题:
(1)某同学查询资料,发现用氯气消毒的自来水不能直接用于浇灌植物、养鱼等。
①不能直接用于浇灌植物、养鱼的原因是氯的水溶液具有较强的___________ (填“氧化性”或“还原性”)
②可以采取___________ 方式快速除水中的氯,再用于浇灌植物。
A.阳光下暴晒 B.烧开后冷却 C.加入过量 固体
固体
(2) 不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为
不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为___________ 。
(3)碱性条件下, 氧化
氧化 可制备绿色消毒剂
可制备绿色消毒剂 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(4)为了使以面粉为原料制作的面包松软可口,通常用碳酸氢钠作发泡剂,发泡时发生的化学方程式为___________ 。
(1)某同学查询资料,发现用氯气消毒的自来水不能直接用于浇灌植物、养鱼等。
①不能直接用于浇灌植物、养鱼的原因是氯的水溶液具有较强的
②可以采取
A.阳光下暴晒 B.烧开后冷却 C.加入过量
 固体
固体(2)
 不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为
不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为(3)碱性条件下,
 氧化
氧化 可制备绿色消毒剂
可制备绿色消毒剂 ,该反应的离子方程式为
,该反应的离子方程式为(4)为了使以面粉为原料制作的面包松软可口,通常用碳酸氢钠作发泡剂,发泡时发生的化学方程式为
您最近一年使用:0次
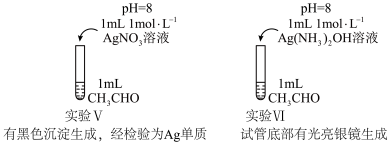
3 . 某实验小组进行如下关于银镜反应的实验探究。
Ⅰ.探究银镜反应中 的作用
的作用
已知:①银镜沉淀速率过快可影响其结构和形貌,从而影响其光泽;
② 开始沉淀时
开始沉淀时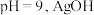 不稳定,易不可逆分解为黑色
不稳定,易不可逆分解为黑色 ;
;
③在实验Ⅰ、Ⅱ、Ⅲ中的 溶液可视作中性溶液。
溶液可视作中性溶液。 的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:
的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:
<猜想1> 的氧化性随溶液
的氧化性随溶液 的增大而增大
的增大而增大
<猜想2>_______ 。
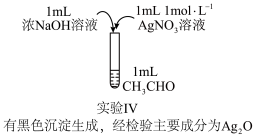
(2)该实验小组为进一步探究而设计实验Ⅲ,实验装置如图所示,最终得到结论:“猜想1不合理,猜想2合理”。简述实验Ⅲ的实验过程:_______ 。 相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是
相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是_______ 。
Ⅱ.该小组在一次制银镜时误将无标签的 溶液当成稀氨水,使得
溶液当成稀氨水,使得 转化为淡黄色
转化为淡黄色 沉淀。查阅资料知只有极浓的氨水可以将
沉淀。查阅资料知只有极浓的氨水可以将 溶解,而实验室并无浓氨水,故不能利用
溶解,而实验室并无浓氨水,故不能利用 制备银氨溶液。实验小组决定采用肼还原
制备银氨溶液。实验小组决定采用肼还原 制银镜,实验报告如下。
制银镜,实验报告如下。
请将实验报告的空缺部分填充完整。
Ⅰ.探究银镜反应中
 的作用
的作用已知:①银镜沉淀速率过快可影响其结构和形貌,从而影响其光泽;
②
 开始沉淀时
开始沉淀时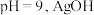 不稳定,易不可逆分解为黑色
不稳定,易不可逆分解为黑色 ;
;③在实验Ⅰ、Ⅱ、Ⅲ中的
 溶液可视作中性溶液。
溶液可视作中性溶液。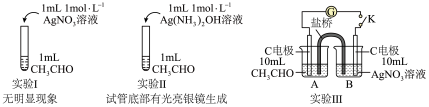
 的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:
的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:<猜想1>
 的氧化性随溶液
的氧化性随溶液 的增大而增大
的增大而增大<猜想2>
(2)该实验小组为进一步探究而设计实验Ⅲ,实验装置如图所示,最终得到结论:“猜想1不合理,猜想2合理”。简述实验Ⅲ的实验过程:
 相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是
相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是Ⅱ.该小组在一次制银镜时误将无标签的
 溶液当成稀氨水,使得
溶液当成稀氨水,使得 转化为淡黄色
转化为淡黄色 沉淀。查阅资料知只有极浓的氨水可以将
沉淀。查阅资料知只有极浓的氨水可以将 溶解,而实验室并无浓氨水,故不能利用
溶解,而实验室并无浓氨水,故不能利用 制备银氨溶液。实验小组决定采用肼还原
制备银氨溶液。实验小组决定采用肼还原 制银镜,实验报告如下。
制银镜,实验报告如下。请将实验报告的空缺部分填充完整。
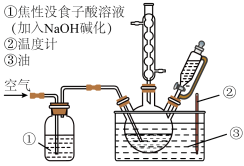
| 实验目的 | 采用肼还原 制得银镜并以此深入探究银镜反应中 制得银镜并以此深入探究银镜反应中 的作用 的作用 | |
| 实验原理 | ①肼 具有强还原性,易吸潮、易被氧化、易与 具有强还原性,易吸潮、易被氧化、易与 等酸性气体反应,常压下可与水形成共沸物(其中肼含量约69%); 等酸性气体反应,常压下可与水形成共沸物(其中肼含量约69%);② 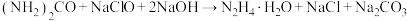 ; ;③  。 。 | |
| 实验药品 |  悬浊液、 悬浊液、 溶液(加 溶液(加 碱化, 碱化,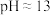 )、催化剂、焦性没食子酸(别名连苯三酚)溶液(加 )、催化剂、焦性没食子酸(别名连苯三酚)溶液(加 碱化, 碱化,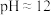 )、尿素、油、 )、尿素、油、 盐酸。 盐酸。 | |
| 实验仪器 | 制备肼的全套装置[具体仪器见装置图,需注意的几点:a.实验最好使用洗气瓶,但因实验室没有洗气瓶,故用 | |
| 实验操作 | ①依图组装仪器并检查气密性,装入药品; ②用 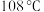 油浴加热,向三预烧瓶缓缓鼓入空气,同时缓缓将恒压滴液漏斗内药品滴入三颈烧瓶,加热约 油浴加热,向三预烧瓶缓缓鼓入空气,同时缓缓将恒压滴液漏斗内药品滴入三颈烧瓶,加热约 后停止加热; 后停止加热;③将三预烧瓶内的液体进行减压蒸馏,得到氨肼混合溶液,将其滴加入  悬浊液中。 悬浊液中。 |
|
| 实验结果 | 实验制得了银单质,但其并未附着在试管壁上形成银镜,而是松散的银粉。 | |
| 实验反思 | ①焦性没食子酸溶液(加 碱化)的作用是 碱化)的作用是②为深入研究为何该反应没有生成银镜,我们又做了如下实验:
| |
您最近一年使用:0次
名校
4 . I.实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。
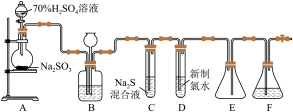
(1)盛装70% H2SO4溶液的仪器名称为___________ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择___________ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为___________ 。
(5)装置E的作用是___________ 。装置F中为___________ 溶液。
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量如下表
说明在严格控制用量的情况下,二氧化硫可被添加到食品中作为漂白剂、防腐剂和___________ (填“氧化剂”或“抗氧化剂”)。
II.利用下图所示装置进行铜与硝酸反应的实验,得到的实验现象如下表:
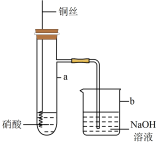
(7)组装好装置后进行实验之前需先进行___________ 。
(8)写出实验Ⅰ中产生的无色气体化学式___________ 。
(9)写出实验Ⅱ中铜与浓硝酸反应的离子方程式___________ 。
(10)装置中采用可拉动铜丝的优点是___________ (写一点)。
(11)针对Ⅰ中溶液呈蓝色,Ⅱ中溶液呈绿色。甲同学推测溶液的颜色与硝酸铜的质量分数有关,而乙同学推测Ⅱ中溶液呈绿色的原因是NO2在硝酸铜溶液中达到饱和所致。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是___________。

(1)盛装70% H2SO4溶液的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量如下表
| 食品名称 | 食糖 | 葡萄酒 | 水果干类 |
| SO2最大使用量 | 0.1g•kg-1 | 0.25g•kg-1 | 1g•kg-1 |
II.利用下图所示装置进行铜与硝酸反应的实验,得到的实验现象如下表:

| 序号 | 实验试剂(20℃) | 实验现象 |
| Ⅰ | 铜丝、2mL稀硝酸 | 铜丝逐渐变细,有气泡产生,a中先产生无色气体后略有红棕色,溶液变蓝 |
| Ⅱ | 铜丝、2mL浓硝酸 | 反应剧烈,铜丝逐渐变细,a中上方出现红棕色气体,溶液变绿 |
(8)写出实验Ⅰ中产生的无色气体化学式
(9)写出实验Ⅱ中铜与浓硝酸反应的离子方程式
(10)装置中采用可拉动铜丝的优点是
(11)针对Ⅰ中溶液呈蓝色,Ⅱ中溶液呈绿色。甲同学推测溶液的颜色与硝酸铜的质量分数有关,而乙同学推测Ⅱ中溶液呈绿色的原因是NO2在硝酸铜溶液中达到饱和所致。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是___________。
| A.加热绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
您最近一年使用:0次
5 . 某小组通过实验探究NO的某些性质。
(1)以Cu和HNO3为原料制备NO,反应的化学方程式为____ 。
(2)设计实验探究NO的氧化性。
实验I:用排水法收集一瓶NO,将其倒扣在盛有碱性Na2SO3溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:i.NO与碱性Na2SO3溶液会发生氧化还原反应NO被还原为N2O 。
。
ii.Ag+与N2O 反应生成黄色沉淀。
反应生成黄色沉淀。
检验SO 的氧化产物。取少量实验I反应后集气瓶中的溶液,
的氧化产物。取少量实验I反应后集气瓶中的溶液,____ (填操作和实验现象)。
(3)某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验II:取饱和Na2SO4溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,无明显变化。
实验III:取少量实验I反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,____ (填实验现象)。
上述实验证明NO有氧化性。
(4)①实验II的目的是____ 。
②写出NO与碱性Na2SO3溶液反应的离子方程式____ 。
③从电极反应角度分析NO与碱性Na2SO3溶液的反应。
还原反应:2NO+2e-=N2O
氧化反应:____ 。
(5)实验IV:用排水法收集两瓶NO,将其分别倒扣在饱和Na2SO3溶液和加有NaOH的饱和Na2SO3溶液中,后者集气瓶中液面上升更快。
根据上述实验所得结论:____ 。
(1)以Cu和HNO3为原料制备NO,反应的化学方程式为
(2)设计实验探究NO的氧化性。
实验I:用排水法收集一瓶NO,将其倒扣在盛有碱性Na2SO3溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:i.NO与碱性Na2SO3溶液会发生氧化还原反应NO被还原为N2O
 。
。ii.Ag+与N2O
 反应生成黄色沉淀。
反应生成黄色沉淀。检验SO
 的氧化产物。取少量实验I反应后集气瓶中的溶液,
的氧化产物。取少量实验I反应后集气瓶中的溶液,(3)某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验II:取饱和Na2SO4溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,无明显变化。
实验III:取少量实验I反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的AgNO3溶液,
上述实验证明NO有氧化性。
(4)①实验II的目的是
②写出NO与碱性Na2SO3溶液反应的离子方程式
③从电极反应角度分析NO与碱性Na2SO3溶液的反应。
还原反应:2NO+2e-=N2O

氧化反应:
(5)实验IV:用排水法收集两瓶NO,将其分别倒扣在饱和Na2SO3溶液和加有NaOH的饱和Na2SO3溶液中,后者集气瓶中液面上升更快。
根据上述实验所得结论:
您最近一年使用:0次
2022-07-10更新
|
534次组卷
|
4卷引用:浙江省宁波市九校2023-2024学年高一下学期6月期末考试化学试题
浙江省宁波市九校2023-2024学年高一下学期6月期末考试化学试题北京市清华附中2021-2022学年高一下学期期末考试化学试题(已下线)重难点04 硫和氮综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)北京市顺义区第一中学2023-2024学年高一下学期期末考试化学试题
名校
6 . 高铁酸钾(K2FeO4)是一种新型高效无毒的多功能水处理剂。K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
I.制备K2FeO4

(1)写出A中发生反应的化学方程式:___________ 。
(2)除杂装置B中的试剂为___________ 。
(3)请写出装置C中制备K2FeO4的离子方程式___________ 。
II.探究K2FeO4的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明K2FeO4能氧化Cl-而产生Cl2设计以下方案:
(4)方案1中溶液变红可知溶液a中含有Fe3+,该离子的产生___________ (填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的,理由是___________ 。
(5)方案2可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是排除ClO-的干扰。根据K2FeO4的制备实验得出:氧化性Cl2___________ FeO (填“>”或“<”),而方案2实验表明,Cl2和FeO
(填“>”或“<”),而方案2实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
(6)资料表明,酸性溶液中的氧化性FeO >MnO
>MnO ,验证实验如下:
,验证实验如下:
将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象___________ (填“能”或“不能”)证明氧化性FeO >MnO
>MnO 。请说明理由:
。请说明理由:___________ 。
I.制备K2FeO4

(1)写出A中发生反应的化学方程式:
(2)除杂装置B中的试剂为
(3)请写出装置C中制备K2FeO4的离子方程式
II.探究K2FeO4的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明K2FeO4能氧化Cl-而产生Cl2设计以下方案:
| 方案1 | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色 |
| 方案2 | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量溶液b,滴加盐酸,有Cl2产生 |
(4)方案1中溶液变红可知溶液a中含有Fe3+,该离子的产生
(5)方案2可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是排除ClO-的干扰。根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案2实验表明,Cl2和FeO
(填“>”或“<”),而方案2实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是(6)资料表明,酸性溶液中的氧化性FeO
 >MnO
>MnO ,验证实验如下:
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象
 >MnO
>MnO 。请说明理由:
。请说明理由:
您最近一年使用:0次
22-23高一上·浙江·期中
解题方法
7 . 高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。
[资料]K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持、加热仪器已略去)
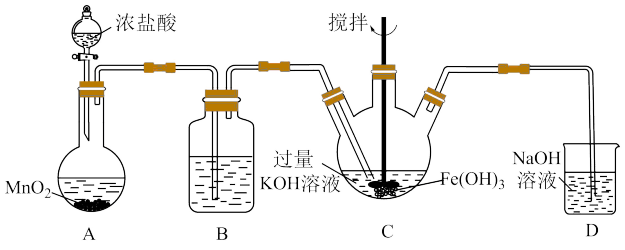
①A为氯气发生装置,A中反应的化学方程式为___________ 。
②B中所用试剂为___________ ,D的作用是___________ 。
③C为制备K2FeO4装置,写出次氯酸钾与氢氧化铁在碱性环境中反应的离子方程式___________ 。
(2)探究K2FeO4的性质。
取C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2.为证明是否是K2FeO4氧化C1-而产生Cl2,某同学设计了如下方案:取少量反应后溶液,滴加KSCN溶液至过量,溶液呈红色。该同学由此认为Cl2是K2FeO4氧化Cl—而产生,请分析他的判断是否准确,说明理由___________ 。
(3)测定高铁酸钾的纯度。已知:K2FeO4(式量为198)与硫酸溶液的反应如下:
4K2FeO4+10H2SO4=2Fe2(SO4)3+3O2↑+4K2SO4+10H2O
取C中洗涤并干燥后样品的质量10.0g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为___________ 计算结果保留到0.1%)。
[资料]K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持、加热仪器已略去)

①A为氯气发生装置,A中反应的化学方程式为
②B中所用试剂为
③C为制备K2FeO4装置,写出次氯酸钾与氢氧化铁在碱性环境中反应的离子方程式
(2)探究K2FeO4的性质。
取C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2.为证明是否是K2FeO4氧化C1-而产生Cl2,某同学设计了如下方案:取少量反应后溶液,滴加KSCN溶液至过量,溶液呈红色。该同学由此认为Cl2是K2FeO4氧化Cl—而产生,请分析他的判断是否准确,说明理由
(3)测定高铁酸钾的纯度。已知:K2FeO4(式量为198)与硫酸溶液的反应如下:
4K2FeO4+10H2SO4=2Fe2(SO4)3+3O2↑+4K2SO4+10H2O
取C中洗涤并干燥后样品的质量10.0g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近一年使用:0次
20-21高一下·浙江·阶段练习
8 . 在氮的化合物中,有一类盐叫亚硝酸盐,如亚硝酸钠(NaNO2)等。它们广泛用于印染、漂白等行业,在建筑行业用作防冻剂,在食品工业作防腐剂和增色剂;它是一种潜在致癌物质,过量或长期食用对人产生危害,由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生过被误当食盐食用的事件。某同学查阅有关资料,了解到亚硝酸及亚硝酸盐的资料相一关信息:(1)HNO2是一种弱酸(比醋酸略强),且不稳定,易分解生成NO和NO2。(2)NO 既有氧化性又有还原性,能被常见的强氧化剂氧化,在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2。(3)AgNO2是一种难溶于水、易溶于硝酸的化合物。下列有关说法不正确的是
既有氧化性又有还原性,能被常见的强氧化剂氧化,在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2。(3)AgNO2是一种难溶于水、易溶于硝酸的化合物。下列有关说法不正确的是
 既有氧化性又有还原性,能被常见的强氧化剂氧化,在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2。(3)AgNO2是一种难溶于水、易溶于硝酸的化合物。下列有关说法不正确的是
既有氧化性又有还原性,能被常见的强氧化剂氧化,在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2。(3)AgNO2是一种难溶于水、易溶于硝酸的化合物。下列有关说法不正确的是| A.可用AgNO3和HNO3两种试剂来鉴别NaNO2和NaCl |
B.亚硝酸钠可以使酸性KMnO4溶液褪色,发生反应的离子方程式可表示为:5NO +2 +2 +6H+=5NO +6H+=5NO +2Mn2++3H2O +2Mn2++3H2O |
| C.在冷冻的亚硝酸钠溶液中加入稀硫酸、通入CO2或SO2均能制得HNO2 |
| D.若误食亚硝酸盐(如NaNO2),会导致血红蛋白中Fe2+被转化为Fe3+而中毒,可服用维生素C解毒,这个过程体现了维生素C的还原性 |
您最近一年使用:0次
解题方法
9 . 利用铁元素“价–类”二维图可以从不同角度研究含铁物质的性质及其转化关系,请据此图回答问题: 属于
属于___________ (填“碱性”“酸性”或“两性”)氧化物。
(2)从物质类别和元素价态视角,下列说法中不正确的是___________。
(3) 通过置换反应可以转化成
通过置换反应可以转化成 ,请写出该化学方程式
,请写出该化学方程式___________ 。
(4)电子工业常用 的
的 溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式
溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式___________ 。某研究人员向上述印刷电路板的废液中加入一定量铁粉,充分反应后,准备过滤并收集滤渣。此时,滤渣的成分不可能是___________ 。
A.只有 B.有
B.有 和
和 C.只有
C.只有
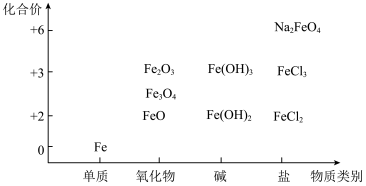
 属于
属于(2)从物质类别和元素价态视角,下列说法中不正确的是___________。
A. 具有强氧化性,可以用作水体消毒剂 具有强氧化性,可以用作水体消毒剂 |
B. 在空气中受热能迅速被氧化成 在空气中受热能迅速被氧化成 |
C.保存 溶液时加入少量还原性铁粉,以防止溶液变质 溶液时加入少量还原性铁粉,以防止溶液变质 |
D.过量的铁粉在氯气中燃烧可以实现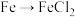 的转化 的转化 |
(3)
 通过置换反应可以转化成
通过置换反应可以转化成 ,请写出该化学方程式
,请写出该化学方程式(4)电子工业常用
 的
的 溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式
溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式A.只有
 B.有
B.有 和
和 C.只有
C.只有
您最近一年使用:0次
10 . 中秋节吃月饼的时候,月饼包装内有一小包标注了“脱氧剂”的物质,从标注可以看出该物质具有
| A.还原性 | B.氧化性 | C.碱性 | D.酸性 |
您最近一年使用:0次