1 . 由下列实验事实得出的结论中错误的是
| 选项 | 实验目的 | 实验事实 | 结论 |
| A | 验证牺牲阳极的阴极保护法 | 将锌片与铁片用导线相连,插入酸化的3%NaCl溶液,一段时间后在铁电极区滴入2滴K3[Fe(CN)6]溶液,出现蓝色沉淀 | 铁不一定被腐蚀 |
| B | 麦芽糖水解产物的检验 | 麦芽糖与稀硫酸共热后,加NaOH溶液调至碱性再加入新制Cu(OH)2并加热,有砖红色沉淀生成 | 麦芽糖水解生成葡萄糖 |
| C | 探究Mg和水反应 | 取一小段镁条,用砂纸除去表面氧化膜,放入试管中,加入2mL水,并滴入2滴酚酞溶液,无明显现象;再加热试管至液体沸腾,溶液变红 | Mg可以与热水反应 |
| D | 制备一水合硫酸四氨合铜 | 向[Cu(NH3)4]SO4溶液中加入无水乙醇,并用玻璃棒摩擦试管壁,有深蓝色晶体析出 | 乙醇极性小,降低了[Cu(NH3)4]SO4的溶解度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列实验设计可以达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 证明金属活动性: | 将金属钠投入 溶液中 溶液中 |
| B | 检验待测液中含有 | 用玻璃棒蘸取待测液在无色火焰上灼烧,观察现象 |
| C | 制备 胶体 胶体 | 将5~6滴饱和 溶液滴加到煮沸的蒸馏水中,继续煮沸至液体呈红褐色为止 溶液滴加到煮沸的蒸馏水中,继续煮沸至液体呈红褐色为止 |
| D | 探究钠在空气中燃烧产物为 | 将燃烧后的物质置于水中,滴入无色酚酞溶液,一段时间后,溶液为红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-20更新
|
451次组卷
|
4卷引用:安徽省安庆市第二中学2023-2024学年高一上学期11月期中考试化学试题
3 . 某校化学兴趣小组为探究锌粒与浓硫酸反应生成气体的成分,设计了如下图所示的实验装置。
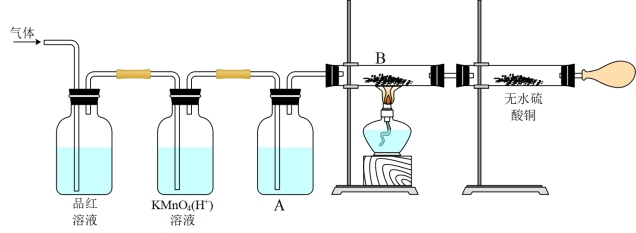
(1)判断气体中有 的实验现象为
的实验现象为___________ ,酸性 溶液的作用是
溶液的作用是___________ 。
(2)装置B中所装药品为___________ ,通过B中现象和无水硫酸铜变蓝说明气体中含有___________ 。
(3)有同学提出不用装置A也能达到实验目的。你是否同意此观点,说明理由:___________ 。
(4)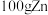 与
与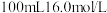 浓硫酸充分反应,锌剩余
浓硫酸充分反应,锌剩余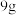 。
。
①写出此过程所发生的2个化学反应方程式:___________ ,___________ ;
②反应生成 体积(标准状况下)为
体积(标准状况下)为___________ L。

(1)判断气体中有
 的实验现象为
的实验现象为 溶液的作用是
溶液的作用是(2)装置B中所装药品为
(3)有同学提出不用装置A也能达到实验目的。你是否同意此观点,说明理由:
(4)
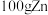 与
与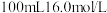 浓硫酸充分反应,锌剩余
浓硫酸充分反应,锌剩余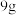 。
。①写出此过程所发生的2个化学反应方程式:
②反应生成
 体积(标准状况下)为
体积(标准状况下)为
您最近一年使用:0次
名校
4 . 利用如图所示装置和对应试剂能完成的实验是
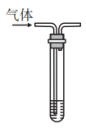

| 选项 | 实验目的 | 方法 | 现象或解释 |
| A | 检验某溶液中 | 在某溶液中先加入少量 溶液,溶液颜色无变化,再通入氯气 溶液,溶液颜色无变化,再通入氯气 | 通入氯气后溶液变红 |
| B | 除去 中少量 中少量 | 气体通过氢氧化钠溶液 |  可被氢氧化钠溶液吸收 可被氢氧化钠溶液吸收 |
| C | 检验 中是否含 中是否含 | 气体通入硝酸银溶液 | 溶液中出现浑浊 |
| D | 吸收实验尾气 | 气体通入水中 | 氨气能溶于水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-09-19更新
|
209次组卷
|
2卷引用:安徽省合肥艺术中学2020-2021学年高一下学期第一次调研考试化学试题
名校
5 . 下列有关制取和提纯乙酸乙酯实验原理和装置不能达到实验目的的是
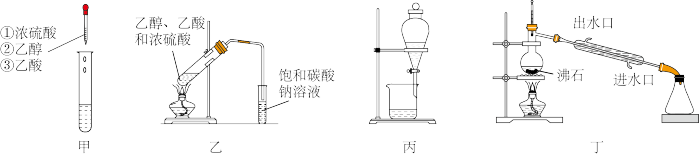

| A.向甲试管中按照乙醇、浓硫酸、乙酸的顺序加入反应物 |
| B.用装置乙制备乙酸乙酯 |
| C.用分液漏斗分离出来的碳酸钠溶液后,需换一个烧杯再从下口放出乙酸乙酯 |
| D.用装置丁通过蒸馏法收集纯净的乙酸乙酯 |
您最近一年使用:0次
2021-04-28更新
|
568次组卷
|
5卷引用:安徽省蚌埠田家炳中学2020-2021学年高二6月月考化学试题
名校
6 . 六水合三氯化铬( )可用于制备催化剂、媒染剂和聚合胶黏剂。实验室用铬酸钠(
)可用于制备催化剂、媒染剂和聚合胶黏剂。实验室用铬酸钠( )为原料制备六水合三氯化铬的实验方案和装置如下:
)为原料制备六水合三氯化铬的实验方案和装置如下:
②六水合三氯化铬易溶于水、可溶于乙醇、不溶于乙醚。
③ 的性质与
的性质与 类似。
类似。
(1)仪器a的名称为___________ ;步骤I中使用该仪器的作用是___________ 。
(2)步骤I反应生成 的同时有
的同时有 气体逸出,反应的化学方程式为
气体逸出,反应的化学方程式为___________ 。
(3)步骤Ⅱ中调节溶液pH不能加入过量NaOH的原因是___________ (用离子方程式解释)。
(4)步骤Ⅳ中洗涤 固体的方法是
固体的方法是___________ 。
(5)步骤VI中“一系列操作”包括加热浓缩、冷却结晶、过滤、用少量___________ 洗涤、低温烘干。
(6)用碘量法测定产品纯度。称取6.0g产品,在强碱性条件下,加入过量 溶液,小火加热使
溶液,小火加热使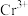 完全转化为
完全转化为 ,再继续加热煮沸一段时间。冷却至室温后,滴入适量稀硫酸使
,再继续加热煮沸一段时间。冷却至室温后,滴入适量稀硫酸使 转化为
转化为 ,再加入蒸馏水将溶液稀释至250mL。取25.00mL溶液,加入过量KI溶液,滴加2-3滴淀粉溶液,用0.3000
,再加入蒸馏水将溶液稀释至250mL。取25.00mL溶液,加入过量KI溶液,滴加2-3滴淀粉溶液,用0.3000
 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: ,三次平行实验测得消耗
,三次平行实验测得消耗 标准溶液体积的数据如下:
标准溶液体积的数据如下:
①“继续加热煮沸一段时间”的目的是___________ 。
②滴定终点的现象为___________ 。
③该产品的纯度为___________ %(结果保留1位小数)。
 )可用于制备催化剂、媒染剂和聚合胶黏剂。实验室用铬酸钠(
)可用于制备催化剂、媒染剂和聚合胶黏剂。实验室用铬酸钠( )为原料制备六水合三氯化铬的实验方案和装置如下:
)为原料制备六水合三氯化铬的实验方案和装置如下: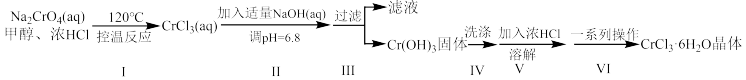
②六水合三氯化铬易溶于水、可溶于乙醇、不溶于乙醚。
③
 的性质与
的性质与 类似。
类似。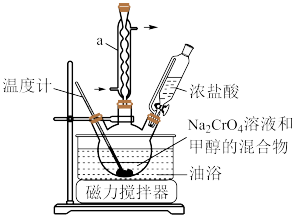
(1)仪器a的名称为
(2)步骤I反应生成
 的同时有
的同时有 气体逸出,反应的化学方程式为
气体逸出,反应的化学方程式为(3)步骤Ⅱ中调节溶液pH不能加入过量NaOH的原因是
(4)步骤Ⅳ中洗涤
 固体的方法是
固体的方法是(5)步骤VI中“一系列操作”包括加热浓缩、冷却结晶、过滤、用少量
(6)用碘量法测定产品纯度。称取6.0g产品,在强碱性条件下,加入过量
 溶液,小火加热使
溶液,小火加热使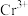 完全转化为
完全转化为 ,再继续加热煮沸一段时间。冷却至室温后,滴入适量稀硫酸使
,再继续加热煮沸一段时间。冷却至室温后,滴入适量稀硫酸使 转化为
转化为 ,再加入蒸馏水将溶液稀释至250mL。取25.00mL溶液,加入过量KI溶液,滴加2-3滴淀粉溶液,用0.3000
,再加入蒸馏水将溶液稀释至250mL。取25.00mL溶液,加入过量KI溶液,滴加2-3滴淀粉溶液,用0.3000
 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: ,三次平行实验测得消耗
,三次平行实验测得消耗 标准溶液体积的数据如下:
标准溶液体积的数据如下:| 第1次 | 第2次 | 第3次 |
| 20.05mL | 20.30mL | 19.95mL |
②滴定终点的现象为
③该产品的纯度为
您最近一年使用:0次
2024-04-11更新
|
282次组卷
|
3卷引用:安徽省皖江名校联盟2024届高三下学期二模化学试题
名校
7 . 二氧化硫是一把“双刃剑”,既是重要的化工原料,又是大气污染物。某化学小组用如图装置制备 ,并验证
,并验证 的部分性质(夹持及加热仪器已省略)。
的部分性质(夹持及加热仪器已省略)。
I.检查气密性后,加入药品,开始实验,关闭 ,打开
,打开 和仪器a活塞,至B处固体变蓝。
和仪器a活塞,至B处固体变蓝。
II.关闭 ,打开
,打开 。
。
回答下列问题:
(1)仪器a的名称为___________ ,装置D的作用是___________ 。
(2)实验过程中观察到C处蘸有酸性 溶液的棉花褪色,写出C处发生反应的离子方程式:
溶液的棉花褪色,写出C处发生反应的离子方程式:___________ (已知 转化为
转化为 )。
)。
(3)装置A___________ (填“需要”或“不需要”)加热,装置A中发生的化学反应方程式为___________ 。
(4)若试剂X是品红溶液,则可验证 的
的___________ 性。
(5)若试剂X是 溶液,反应一段时间,可观察到现象为
溶液,反应一段时间,可观察到现象为___________ ,该反应中 表现
表现___________ 性。
(6)若试剂X是 的
的 溶液,装置E中得到了大量白色沉淀;而用
溶液,装置E中得到了大量白色沉淀;而用 的
的 溶液,装置E中无白色沉淀生成。
溶液,装置E中无白色沉淀生成。
①前者生成的白色沉淀为 ,生成该沉淀的原因是
,生成该沉淀的原因是___________ (由语言描述)。
②后者无白色沉淀生成,可说明酸性:
___________ (填“>”或“<”)HCl。
 ,并验证
,并验证 的部分性质(夹持及加热仪器已省略)。
的部分性质(夹持及加热仪器已省略)。
I.检查气密性后,加入药品,开始实验,关闭
 ,打开
,打开 和仪器a活塞,至B处固体变蓝。
和仪器a活塞,至B处固体变蓝。II.关闭
 ,打开
,打开 。
。回答下列问题:
(1)仪器a的名称为
(2)实验过程中观察到C处蘸有酸性
 溶液的棉花褪色,写出C处发生反应的离子方程式:
溶液的棉花褪色,写出C处发生反应的离子方程式: 转化为
转化为 )。
)。(3)装置A
(4)若试剂X是品红溶液,则可验证
 的
的(5)若试剂X是
 溶液,反应一段时间,可观察到现象为
溶液,反应一段时间,可观察到现象为 表现
表现(6)若试剂X是
 的
的 溶液,装置E中得到了大量白色沉淀;而用
溶液,装置E中得到了大量白色沉淀;而用 的
的 溶液,装置E中无白色沉淀生成。
溶液,装置E中无白色沉淀生成。①前者生成的白色沉淀为
 ,生成该沉淀的原因是
,生成该沉淀的原因是②后者无白色沉淀生成,可说明酸性:

您最近一年使用:0次
名校
8 . 碳酸亚铁( )是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备
)是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备 ,并探究
,并探究 的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
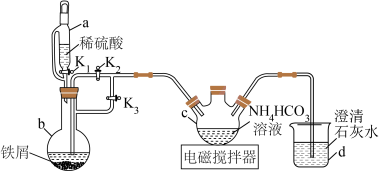
(1)仪器 的名称为
的名称为______ 。
(2)实验开始时,先打开______ (填“ 、
、 或
或 ”,下同)、关闭
”,下同)、关闭______ ;一段时间后,______ , 中反应获得
中反应获得 。
。
(3)已知 中澄清石灰水变浑浊,写出
中澄清石灰水变浑浊,写出 中反应的离子方程式:
中反应的离子方程式:______ 。
(4)反应结束后,将 中的混合液过滤,洗涤。简述证明
中的混合液过滤,洗涤。简述证明 已洗涤干净的操作:
已洗涤干净的操作:____________ 。
Ⅱ.定性定量探究碳酸亚铁有还原性
【查阅资料】氧化亚铁是一种黑色粉末,不稳定,在空气中加热,迅速被氧化成四氧化三铁。
(5)定性探究碳酸亚铁和氧气反应的固体成分:
【提出设想】
假设1固体成分是氧化铁;
假设2固体成分是四氧化三铁;
假设3______ 。
【实验验证】所用装置如下图所示,装药品,打开止水夹 ,通入
,通入 ,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入
,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入 至玻璃管冷却。
至玻璃管冷却。
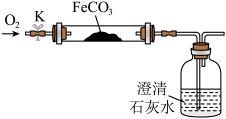
取少量玻璃管里固体于试管中,滴加稀硫酸,微热,固体完全溶解。将溶液分成甲、乙两份,进行后续实验。
【实验评价】上述实验(填“ⅰ”或“ⅱ”)不能确定固体成分。
【实验结论】由上述实验结果分析可知,碳酸亚铁在氧气中高温灼烧得到的产物是______ ,证明 具有还原性。
具有还原性。
(6)定量探究:取______ g纯净固体碳酸亚铁,在空气中高温灼烧至恒重,称得固体质量净减少7.2g,通过计算确定固体成分是 。
。
 )是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备
)是制备“速力菲”(主要成分:琥珀酸亚铁,一种常见的补铁药物)的重要物质。某学习小组同学设计实验制备 ,并探究
,并探究 的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
的还原性。回答下列问题:Ⅰ.碳酸亚铁的制备。实验装置(夹持仪器已省略)如图所示。
(1)仪器
 的名称为
的名称为(2)实验开始时,先打开
 、
、 或
或 ”,下同)、关闭
”,下同)、关闭 中反应获得
中反应获得 。
。(3)已知
 中澄清石灰水变浑浊,写出
中澄清石灰水变浑浊,写出 中反应的离子方程式:
中反应的离子方程式:(4)反应结束后,将
 中的混合液过滤,洗涤。简述证明
中的混合液过滤,洗涤。简述证明 已洗涤干净的操作:
已洗涤干净的操作:Ⅱ.定性定量探究碳酸亚铁有还原性
【查阅资料】氧化亚铁是一种黑色粉末,不稳定,在空气中加热,迅速被氧化成四氧化三铁。
(5)定性探究碳酸亚铁和氧气反应的固体成分:
【提出设想】
假设1固体成分是氧化铁;
假设2固体成分是四氧化三铁;
假设3
【实验验证】所用装置如下图所示,装药品,打开止水夹
 ,通入
,通入 ,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入
,加热玻璃管。澄清石灰水不产生沉淀时,停止加热,继续通入 至玻璃管冷却。
至玻璃管冷却。
取少量玻璃管里固体于试管中,滴加稀硫酸,微热,固体完全溶解。将溶液分成甲、乙两份,进行后续实验。
实验编号 | 实验步骤 | 实验现象 |
ⅰ | 滴加 | 溶液变红色 |
ⅱ | 向乙溶液中滴加酸性高锰酸钾溶液 | 溶液不褪色 |
【实验结论】由上述实验结果分析可知,碳酸亚铁在氧气中高温灼烧得到的产物是
 具有还原性。
具有还原性。(6)定量探究:取
 。
。
您最近一年使用:0次
名校
解题方法
9 . 金属铋在工业上常用于制造低熔点合金,用于消防装置、自动喷水器、锅炉等的安全塞,一旦发生火灾,·些水管的活塞会“自动”熔化,喷出水来。由一种铋矿[主要成分为 (不溶于水),含强氧化性杂质
(不溶于水),含强氧化性杂质 等]制备金属铋的简单工艺如图:
等]制备金属铋的简单工艺如图:
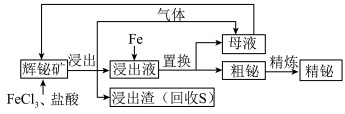
已知:酸性条件下的氧化性: 。
。
(1)“浸出”过程中,溶液中放出的气体是_________ ;放出该气体的离子方程式是________ 。
(2)加入 溶液的目的是
溶液的目的是___________ ,该反应的离子方程式是___________ 。
(3)检验母液中所含有的主要金属阳离子的方法是___________ 。
(4)铋的+5价盐类( 盐)具有强氧化性。欲探究
盐)具有强氧化性。欲探究 盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的
盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的 溶液,向其中依次加入下列试剂,对应的现象如下表所示:
溶液,向其中依次加入下列试剂,对应的现象如下表所示:
据图回答下面的问题:
①上述试剂的氧化性强弱顺序为:___________ 。
②写出 和
和 反应的离子方程式,并用双线桥法标注电子转移方向
反应的离子方程式,并用双线桥法标注电子转移方向_________ ,已知 不溶于水。)
不溶于水。)
 (不溶于水),含强氧化性杂质
(不溶于水),含强氧化性杂质 等]制备金属铋的简单工艺如图:
等]制备金属铋的简单工艺如图:
已知:酸性条件下的氧化性:
 。
。(1)“浸出”过程中,溶液中放出的气体是
(2)加入
 溶液的目的是
溶液的目的是(3)检验母液中所含有的主要金属阳离子的方法是
(4)铋的+5价盐类(
 盐)具有强氧化性。欲探究
盐)具有强氧化性。欲探究 盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的
盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的 溶液,向其中依次加入下列试剂,对应的现象如下表所示:
溶液,向其中依次加入下列试剂,对应的现象如下表所示:| 加入溶液 | ①适量铋酸钠固体 | ②过量的双氧水 | ③加入淀粉 溶液 溶液 |
| 实验现象 | 溶液呈现紫红色 | 紫红色消失,产生气泡 | 溶液变为蓝色 |
①上述试剂的氧化性强弱顺序为:
②写出
 和
和 反应的离子方程式,并用双线桥法标注电子转移方向
反应的离子方程式,并用双线桥法标注电子转移方向 不溶于水。)
不溶于水。)
您最近一年使用:0次
名校
解题方法
10 . 氯化钛( )可用于制造烟幕、织物媒染剂、人造珍珠等。常温下为无色液体,沸点为136℃,与水剧烈反应产生白烟。实验室利用反应
)可用于制造烟幕、织物媒染剂、人造珍珠等。常温下为无色液体,沸点为136℃,与水剧烈反应产生白烟。实验室利用反应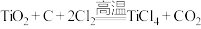 制备
制备 的装置如图所示。
的装置如图所示。

在制备 时,对原料及装置的干燥程度要求很高。回答下列问题:
时,对原料及装置的干燥程度要求很高。回答下列问题:
(1)若分别用 与
与 作氧化剂与盐酸反应制备
作氧化剂与盐酸反应制备 ,当获得等量的
,当获得等量的 时消耗的氧化剂物质的量之比为
时消耗的氧化剂物质的量之比为___________ 。
(2)B中试剂的作用为___________ 。
(3)干燥管D中的试剂可以是___________ ,装置E中棉花球的作用为___________ 。
(4) 与水剧烈反应产生的白烟为
与水剧烈反应产生的白烟为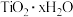 ,写出反应的化学方程式
,写出反应的化学方程式___________ 。
(5)实验中发现F中有少量白烟产生,为避免此现象,改进措施是___________ 。
(6)实验结束后,取下A装置后应进行的操作为___________ ;G中发生反应的离子方程式为:___________ 。
 )可用于制造烟幕、织物媒染剂、人造珍珠等。常温下为无色液体,沸点为136℃,与水剧烈反应产生白烟。实验室利用反应
)可用于制造烟幕、织物媒染剂、人造珍珠等。常温下为无色液体,沸点为136℃,与水剧烈反应产生白烟。实验室利用反应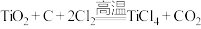 制备
制备 的装置如图所示。
的装置如图所示。
在制备
 时,对原料及装置的干燥程度要求很高。回答下列问题:
时,对原料及装置的干燥程度要求很高。回答下列问题:(1)若分别用
 与
与 作氧化剂与盐酸反应制备
作氧化剂与盐酸反应制备 ,当获得等量的
,当获得等量的 时消耗的氧化剂物质的量之比为
时消耗的氧化剂物质的量之比为(2)B中试剂的作用为
(3)干燥管D中的试剂可以是
(4)
 与水剧烈反应产生的白烟为
与水剧烈反应产生的白烟为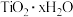 ,写出反应的化学方程式
,写出反应的化学方程式(5)实验中发现F中有少量白烟产生,为避免此现象,改进措施是
(6)实验结束后,取下A装置后应进行的操作为
您最近一年使用:0次



