名校
解题方法
1 . 有机物 是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究
是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究 的组成与结构,进行如下实验:
的组成与结构,进行如下实验:
(1)将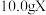 在足量
在足量 中充分燃烧,并将其产物依次通过足量的无水
中充分燃烧,并将其产物依次通过足量的无水 和
和 浓溶液,发现无水
浓溶液,发现无水 增重
增重 ,
, 浓溶液增重
浓溶液增重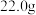 。该有机物
。该有机物 的实验式为
的实验式为_______ 。
(2)有机物 的质谱图如图所示,该有机物
的质谱图如图所示,该有机物 的相对分子质量为
的相对分子质量为_______ 。 的分子式为
的分子式为_______ 。
(4)经红外光谱测定,有机物 中含有醛基;有机物
中含有醛基;有机物 的核磁共振氢谱图上有2组吸收峰,峰面积之比为
的核磁共振氢谱图上有2组吸收峰,峰面积之比为 。该有机物
。该有机物 的结构简式为
的结构简式为_______ 。
 是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究
是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究 的组成与结构,进行如下实验:
的组成与结构,进行如下实验:(1)将
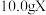 在足量
在足量 中充分燃烧,并将其产物依次通过足量的无水
中充分燃烧,并将其产物依次通过足量的无水 和
和 浓溶液,发现无水
浓溶液,发现无水 增重
增重 ,
, 浓溶液增重
浓溶液增重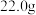 。该有机物
。该有机物 的实验式为
的实验式为(2)有机物
 的质谱图如图所示,该有机物
的质谱图如图所示,该有机物 的相对分子质量为
的相对分子质量为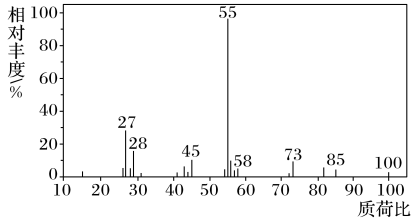
 的分子式为
的分子式为(4)经红外光谱测定,有机物
 中含有醛基;有机物
中含有醛基;有机物 的核磁共振氢谱图上有2组吸收峰,峰面积之比为
的核磁共振氢谱图上有2组吸收峰,峰面积之比为 。该有机物
。该有机物 的结构简式为
的结构简式为
您最近一年使用:0次
名校
解题方法
2 . 芳香族化合物 常用于药物及香料的合成,A有如图转化关系:
常用于药物及香料的合成,A有如图转化关系:
①A是芳香族化合物且苯环侧链上有两种处于不同环境下的氢原子;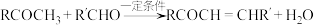 。
。
回答下列问题:
(1)B的分子式为_______ ,F具有的官能团名称是_______ 。
(2)由D生成E的反应类型为_______ ,由E生成F所需试剂及反应条件为_______ 。
(3)K分子中含有两个六元环,则K的结构简式为_______ 。
(4)由H生成I的化学方程式为_______ 。
(5)化合物F的同分异构体中能同时满足以下三个条件的有_______ 种(不考虑立体异构)。
①能与 溶液发生显色反应;②能发生银镜反应;③苯环上有两个取代基。
溶液发生显色反应;②能发生银镜反应;③苯环上有两个取代基。
其中核磁共振氢谱有6组峰,峰面积比为 的化合物的结构简式为
的化合物的结构简式为_______ 。
 常用于药物及香料的合成,A有如图转化关系:
常用于药物及香料的合成,A有如图转化关系:
①A是芳香族化合物且苯环侧链上有两种处于不同环境下的氢原子;
②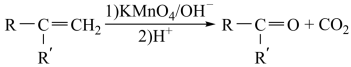 ;
;
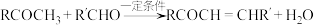 。
。回答下列问题:
(1)B的分子式为
(2)由D生成E的反应类型为
(3)K分子中含有两个六元环,则K的结构简式为
(4)由H生成I的化学方程式为
(5)化合物F的同分异构体中能同时满足以下三个条件的有
①能与
 溶液发生显色反应;②能发生银镜反应;③苯环上有两个取代基。
溶液发生显色反应;②能发生银镜反应;③苯环上有两个取代基。其中核磁共振氢谱有6组峰,峰面积比为
 的化合物的结构简式为
的化合物的结构简式为
您最近一年使用:0次
名校
3 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(MgxFe2-xSiO4)。回答下列问题:
(1)基态Fe原子在周期表的位置为___________ 。橄榄石中,各元素电负性由大到小顺序为___________ ,铁的化合价为___________ 。
(2)已知一些物质的熔点数据如下表:
①Na与Si均为第三周期元素,NaCl熔点明显高于SiCl4,原因是___________ 。
②分析同族元素的氯化物SiCl4、GeCl4、SnCl4熔点变化趋势及其原因___________ 。
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有___________ 个Mg。该物质化学式为___________ ,B—B最近距离为___________ 。
(1)基态Fe原子在周期表的位置为
(2)已知一些物质的熔点数据如下表:
| 物质 | 熔点/℃ |
| NaCl | 800.7 |
| SiCl4 | -68.8 |
| GeCl4 | -51.5 |
| SnCl4 | -34.1 |
②分析同族元素的氯化物SiCl4、GeCl4、SnCl4熔点变化趋势及其原因
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有

您最近一年使用:0次
名校
解题方法
4 . 下列有关说法不正确的是
A.S2Cl2 为极性分子 为极性分子 |
B.1个碳酸亚乙烯酯分子 中含8个σ键 中含8个σ键 |
C.每个P4S3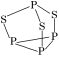 分子中含孤电子对的数目为10对 分子中含孤电子对的数目为10对 |
D. 表明1s轨道呈球形,有3条对称轴 表明1s轨道呈球形,有3条对称轴 |
您最近一年使用:0次
名校
5 . 冠醚是一种超分子,它是由多个二元醇分子之间脱水形成的环状化合物。18—冠—6可用作相转移催化其与 形成的螯合离子结构如图所示。下列说法正确的是
形成的螯合离子结构如图所示。下列说法正确的是
 形成的螯合离子结构如图所示。下列说法正确的是
形成的螯合离子结构如图所示。下列说法正确的是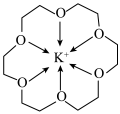
| A.该螯合离子形成的晶体类型为分子晶体 |
B.与二甲醚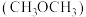 相比,该整合离子中“C-O-C”键角更大 相比,该整合离子中“C-O-C”键角更大 |
| C.该螯合离子中碳原子与氧原子杂化类型不同 |
| D.该螯合离子中所有非氢原子可以位于同一平面 |
您最近一年使用:0次
名校
6 . 一种抗癫痫药物的合成中间体的结构如图所示,下列关于该有机物的说法正确的是
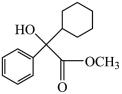
| A.属于芳香烃 | B.分子式为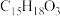 |
| C.苯环上的一氯代物有3种 | D.分子中含有2个手性碳原子 |
您最近一年使用:0次
名校
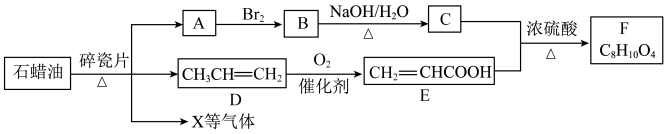
7 . A是米自石油的重要有机化工原料,其产量迫常用来衡量一个国家的石油化工发展水平,F是一种油状液体,转化关系如下图所示(部分反应条件、产物省略)。回答下列问题: RCH2OH
RCH2OH
(1)A的电子式为___________ 。
(2)A→B的化学反应方程式为___________ ,B的名称是___________ 。
(3)下列有关D的说法正确的是___________ (填字母)。
a.在水和四氯化碳中均易溶解 b能使酸性高锰酸钾溶液褪色
c.分子中最多有7个原子共平面 d.与HCl加成只生成一种产物
(4)根据上述已知信息,分析有机物C的结构简式是___________ 。
(5)E可用于制取聚丙烯酸树脂漆,聚丙烯酸的结构简式为___________ 。
 RCH2OH
RCH2OH(1)A的电子式为
(2)A→B的化学反应方程式为
(3)下列有关D的说法正确的是
a.在水和四氯化碳中均易溶解 b能使酸性高锰酸钾溶液褪色
c.分子中最多有7个原子共平面 d.与HCl加成只生成一种产物
(4)根据上述已知信息,分析有机物C的结构简式是
(5)E可用于制取聚丙烯酸树脂漆,聚丙烯酸的结构简式为
您最近一年使用:0次
8 . 下列关于物质结构的说法错误的是
| A.晶格能:NaF>NaCl>NaBr |
| B.基态碳原子核外有6种运动状态的电子 |
C.CH4和 都是正四面体结构,键角均为109°28′ 都是正四面体结构,键角均为109°28′ |
| D.甲醛(HCHO)的键角约为120°,分子之间存在氢键 |
您最近一年使用:0次
名校
9 . 硼、氮、铁、钴、镍等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
(2)硼酸( )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在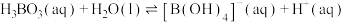 的平衡,回答下列问题。
的平衡,回答下列问题。__________ 。
②下列关于硼酸的说法正确的是__________ (填序号)。
a. 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
c.硼酸分子的稳定性与氢键有关 d.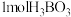 晶体中有
晶体中有 氢键
氢键
(3)叠氮化合物在化工上有重要应用, 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式__________ (写出一种即可),其立体构型为__________ 。
(4) 的结构如图所示,
的结构如图所示, 中
中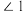 、
、 、
、 由大到小的顺序是
由大到小的顺序是____________________ 。 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于__________ 位置。
①从该晶胞中能分割出来的结构图有_______ (填标号)。 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有__________ 个,该距离为__________ pm(仅列式不计算)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
A.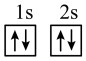 | B. |
C.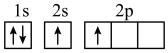 | D.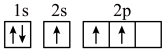 |
(2)硼酸(
 )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在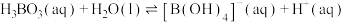 的平衡,回答下列问题。
的平衡,回答下列问题。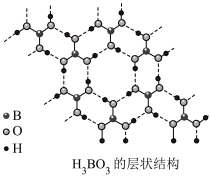
②下列关于硼酸的说法正确的是
a.
 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制c.硼酸分子的稳定性与氢键有关 d.
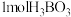 晶体中有
晶体中有 氢键
氢键(3)叠氮化合物在化工上有重要应用,
 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式(4)
 的结构如图所示,
的结构如图所示, 中
中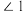 、
、 、
、 由大到小的顺序是
由大到小的顺序是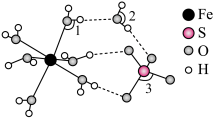
 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于
①从该晶胞中能分割出来的结构图有
a.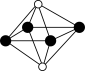 b.
b.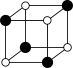 c.
c.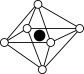 d.
d. e.
e.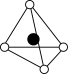
 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
您最近一年使用:0次
名校
解题方法
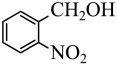
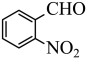
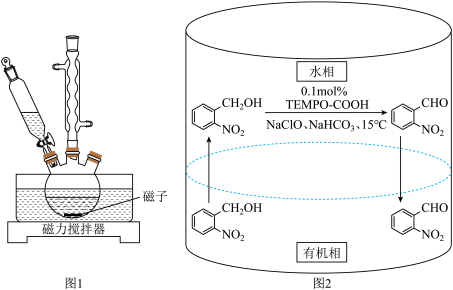
10 . 实验室以邻硝基苄醇为原料,通过图1装置(夹持仪器已略去)利用两相反应体系(图2)在TEMPO-COOH水溶液做催化剂下实现选择性氧化合成邻硝基苯甲醛。部分物质的性质如下表所示。
Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用10.0mL二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
Ⅲ.将粗品溶解在20.0mL二氯甲烷中,加入10.0mL饱和NaHSO3溶液,充分作用后,分离得到水层,水层在冰浴中用5%氢氧化钠溶液调节pH到10,浅黄色固体析出完全。抽滤、干燥至恒重,得1.30g产品。
(1)控制反应温度为15℃的方法是___________ ;滴加NaC1O溶液时,需要先将漏斗上端玻璃塞打开,目的是___________ 。
(2)合成产品的化学方程式为___________ 。
(3)配制饱和NaHCO3溶液时,必须使用的仪器是(填写仪器名称)___________ 。____________ ,该副产物主要成分是___________ 。
(5)步骤Ⅱ中除去并回收二氯甲烷的实验方法是___________ 。
(6)本实验产率为___________ (计算结果保留3位有效数字)。
| 物质 |
|
| TEMPO-COOH |
| 溶解性 | 微溶于水,易溶于CH2Cl2 | 难溶于水,易溶于CH2Cl2 | 易溶于水,难溶于CH2Cl2 |
| 熔点/℃ | 70 | 43 | —— |
| 沸点/℃ | 270 | 153 | —— |
已知: 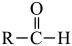 +NaHSO3
+NaHSO3
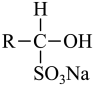 (易溶于水);
(易溶于水);
Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用10.0mL二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
Ⅲ.将粗品溶解在20.0mL二氯甲烷中,加入10.0mL饱和NaHSO3溶液,充分作用后,分离得到水层,水层在冰浴中用5%氢氧化钠溶液调节pH到10,浅黄色固体析出完全。抽滤、干燥至恒重,得1.30g产品。
(1)控制反应温度为15℃的方法是
(2)合成产品的化学方程式为
(3)配制饱和NaHCO3溶液时,必须使用的仪器是(填写仪器名称)
(5)步骤Ⅱ中除去并回收二氯甲烷的实验方法是
(6)本实验产率为
您最近一年使用:0次