名校
1 . 实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
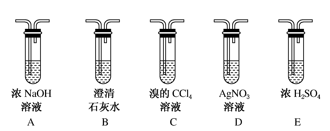
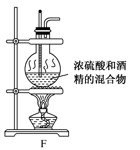
(1)写出制备乙烯反应的化学方程式___ 。加热F装置时必须使液体温度___ 。
(2)为实现上述实验目的,装置的连接顺序为F→___ →D。(各装置限用一次);其中B装置的作用___ 。
(3)当C中观察到___ 时,表明单质溴能与乙烯反应;当D中___ 时,表明C中发生的是取代反应;若D没有出现前面所描述的现象时,表明C中发生的是___ 反应。


(1)写出制备乙烯反应的化学方程式
(2)为实现上述实验目的,装置的连接顺序为F→
(3)当C中观察到
您最近一年使用:0次
2021-06-22更新
|
94次组卷
|
2卷引用:海南省华中师范大学琼中附属中学2020-2021学年高二下学期6月月考化学试题
名校
2 . 按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。
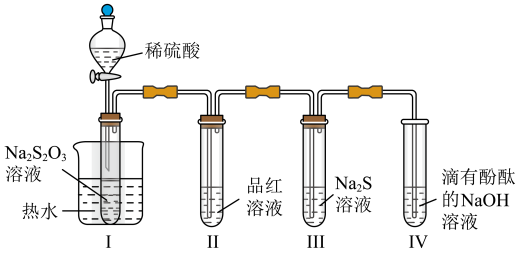
回答下列问题:
(1)盛放稀硫酸的仪器名称是___________ 。
(2)Ⅰ中试管内反应的离子方程式是___________ 。
(3)撤掉水浴,重做实验,Ⅱ中品红溶液褪色___________ (填“加快”“减慢”“无变化” “无法确定”)。
(4)试管Ⅳ中滴有酚酞的NaOH 溶液的作用是___________ 。
(5)试管Ⅲ的Na2S溶液若换为Na2S和Na2CO3混合溶液,先会变浑浊,后又变澄清(生成Na2S2O3溶液)。此浑浊物是___________ ,此过程总反应的化学方程式为:___________ 。
(6)实验已经验证SO2的部分化学性质,请设计实验验证SO2的其它化学性质___________ (包括实验目的、实验原理、操作现象)。

回答下列问题:
(1)盛放稀硫酸的仪器名称是
(2)Ⅰ中试管内反应的离子方程式是
(3)撤掉水浴,重做实验,Ⅱ中品红溶液褪色
(4)试管Ⅳ中滴有酚酞的NaOH 溶液的作用是
(5)试管Ⅲ的Na2S溶液若换为Na2S和Na2CO3混合溶液,先会变浑浊,后又变澄清(生成Na2S2O3溶液)。此浑浊物是
(6)实验已经验证SO2的部分化学性质,请设计实验验证SO2的其它化学性质
您最近一年使用:0次
3 . 下列实验设计能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 探究浓度对化学反应速率的影响 | 常温常压下,向一试管中加入10%的 溶液,另一试管中加入 溶液,另一试管中加入 固体和5%的 固体和5%的 溶液,观察现象 溶液,观察现象 |
| B | 制备并得到纯净的溴苯 | 向含溴的苯溶液中加入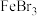 溶液,充分反应后,过滤洗涤 溶液,充分反应后,过滤洗涤 |
| C | 证明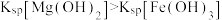 | 向  NaOH溶液中滴加2滴同浓度的 NaOH溶液中滴加2滴同浓度的 溶液后,再滴加2滴同浓度的 溶液后,再滴加2滴同浓度的 溶液,观察现象 溶液,观察现象 |
| D | 验证某溶液中一定含有钾元素 | 用洁净的铁丝蘸取该溶液在酒精灯外焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-16更新
|
137次组卷
|
2卷引用:海南省琼海市2023届高三联考二模化学试题
解题方法
4 . 某化学兴趣小组进行以下实验探究:
I.设计实验探究反应速率的测定和比较
实验步骤:
取一套装置(装置如图所示),加入40mL1mol•L-1的硫酸,测量收集10mLH2所需的时间。
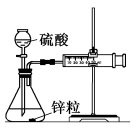
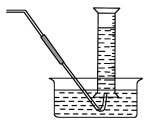
(1)取另一套装置,加入40mL4mol•L-1的硫酸,测量收集10mLH2所需的时间。
实验现象:锌跟硫酸反应产生气泡,收集10mL气体,(2)所用时间比(1)所用时间____ (填“长”或“短”)。
实验结论:4mol•L-1硫酸与锌反应比1mol•L-1硫酸与锌反应速率____ (填“大”或“小”)。
注意事项:①锌粒的颗粒(即表面积)大小_____ 。
②40mL的硫酸要迅速加入。
(2)II.探究用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素,所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K。
请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
I.设计实验探究反应速率的测定和比较
实验步骤:
取一套装置(装置如图所示),加入40mL1mol•L-1的硫酸,测量收集10mLH2所需的时间。


(1)取另一套装置,加入40mL4mol•L-1的硫酸,测量收集10mLH2所需的时间。
实验现象:锌跟硫酸反应产生气泡,收集10mL气体,(2)所用时间比(1)所用时间
实验结论:4mol•L-1硫酸与锌反应比1mol•L-1硫酸与锌反应速率
注意事项:①锌粒的颗粒(即表面积)大小
②40mL的硫酸要迅速加入。
(2)II.探究用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素,所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K。
请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T(K) | 大理石规格 | HNO3浓度(mol•L-1) | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (1)实验①和②探究HNO3浓度对该反应速率的影响 (2)实验①和 (3)实验①和 |
| ② | ||||
| ③ | 粗颗粒 | |||
| ④ |
您最近一年使用:0次
5 . 下列实验操作和现象正确并与预期实验目的或结论一致的是
| 选项 | 实验操作和现象 | 预期实验目的或结论 |
| A | 将过量稀硫酸加入碳酸钠溶液中,观察到有无色气泡产生 | 非金属性:S>C |
| B | 向品红溶液中通入足量Cl2,观察到品红溶液褪色 | Cl2具有漂白性 |
| C | 向0.1mol•L-1FeCl3溶液中滴加稀氨水,观察到溶液由黄色变为红褐色 | 制备Fe(OH)3胶体 |
| D | 将10~15滴溴乙烷和1mL5%NaOH溶液混合后加热,然后静置,待溶液分层后,取上层液体于另一支试管中,先加入足量稀硝酸酸化,再滴加AgNO3溶液,观察到有浅黄色沉淀生成 | 检验溴乙烷中的溴原子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-30更新
|
129次组卷
|
2卷引用:海南省昌江县部分学校2023届高三联合质检二模化学试题
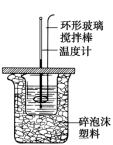
6 . (1)50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:____ 。
②大烧杯上如不盖硬纸板,求得的中和热数值____ (填“偏大”、“偏小”或“无影响”)。
③实验中改用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所放出的热量___ (填“相等”或“不相等”)。
④用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会____ (填“偏大””、“偏小””或“无影响”)。
(2)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
①催化剂能增大化学反应速率的原因是___ 。
②实验①和②的目的是探究___ 对反应速率的影响。实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是___ 。
③实验③④⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论:___ 环境能增大H2O2分解的速率;
b.___ 环境能减小H2O2分解的速率。
②大烧杯上如不盖硬纸板,求得的中和热数值
③实验中改用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
④用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
(2)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 分组实验 | 催化剂 | |
| ① | 10mL5%H2O2溶液 | 无 |
| ② | 10mL2%H2O2溶液 | 无 |
| ③ | 10mL5%H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5%H2O2溶液+少量稀盐酸 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5%H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
②实验①和②的目的是探究
③实验③④⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论:
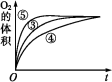
b.
您最近一年使用:0次
2021-05-24更新
|
176次组卷
|
2卷引用:海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题
7 . 利用下列有关实验装置进行的相应实验,能达到实验目的的是
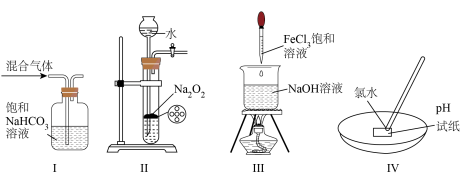

A.图Ⅰ除去 中含有的少量 中含有的少量 |
| B.实验室用图Ⅱ装置制备少量氧气 |
C.图Ⅲ制备 胶体 胶体 |
D.图Ⅳ测新制氯水的 值 值 |
您最近一年使用:0次
名校
8 .  是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是

 是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
A.用操作甲鉴别 溶液和 溶液和 溶液 溶液 |
B.用装置乙除去 气体中的 气体中的 |
C.用装置丙吸收多余的 |
D.用操作丁制备少量 固体 固体 |
您最近一年使用:0次
解题方法
9 . 下列实验装置可用于实验室制备少量无水 ,已知
,已知 遇水会强烈反应。
遇水会强烈反应。
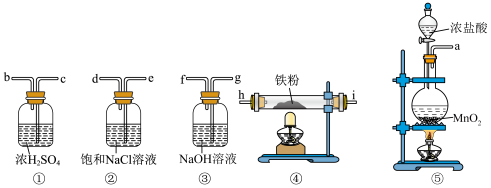
(1)装置⑤装有浓盐酸的仪器名称为_______ ,装有 的仪器名称为
的仪器名称为_______ 。
(2)为达到实验目的,各装置的正确连接顺序是:
__________ 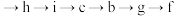 (填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。
(填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。
(3)请写出装置⑤中制备氯气的离子方程式_______ 。
(4)装置②的作用_______ 。
(5)请写出④制备 的化学方程式
的化学方程式_______ 。
(6)用离子方程式表示③的作用_______ 。
(7)本实验装置④⑤两处均有酒精灯,实验开始前应先点燃_______ (填装置序号)处酒精灯,后点燃_______ (填装置序号)处酒精灯。
(8)①装置前后两次使用,第1次使用时①装置的作用为_______ ,第2次使用时①装置的作用为_______ 。
 ,已知
,已知 遇水会强烈反应。
遇水会强烈反应。
(1)装置⑤装有浓盐酸的仪器名称为
 的仪器名称为
的仪器名称为(2)为达到实验目的,各装置的正确连接顺序是:

 (填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。
(填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。(3)请写出装置⑤中制备氯气的离子方程式
(4)装置②的作用
(5)请写出④制备
 的化学方程式
的化学方程式(6)用离子方程式表示③的作用
(7)本实验装置④⑤两处均有酒精灯,实验开始前应先点燃
(8)①装置前后两次使用,第1次使用时①装置的作用为
您最近一年使用:0次
名校
10 . 实验是化学研究的重要手段,下列有关实验装置能达到实验目的的是
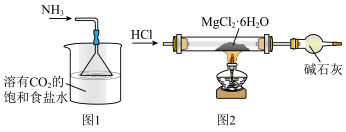
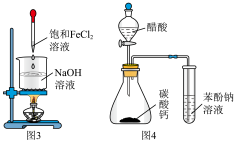


A.图1装置制备大量 | B.图2装置制备无水 |
C.图3装置制备 胶体 胶体 | D.图4装置可比较醋酸、碳酸、苯酚酸性强弱 |
您最近一年使用:0次
2023-05-04更新
|
427次组卷
|
3卷引用:海南省海口市海南中学,文昌中学,海口一中,嘉积中学2023届高三第一次模拟考试化学试题



