1 . NOx是汽车尾气和化工生产中的常见大气污染物,其综合治理是当前重要的研究课题。工业上可以用不同的方法处理NOx。
I.碘蒸气存在能大幅度提高N2O的分解速率,反应方程式为 ,反应历程可表示为:
,反应历程可表示为:
第一步(快反应) I2(g) 2I(g)
2I(g)
第二步(慢反应)
第三步(快反应) 2IO(g)+2N2O(g)→2N2(g)+2O2(g)+I2(g)
(1)写出第二步反应___________ 。
(2)下列表述正确的是___________。
II.汽车尾气中含有较多的氮氧化合物和不完全燃烧的CO,汽车三元催化器可以将其转化成两种无污染的气体,从而降低氮氧化合物的排放量。
例如:2CO(g) +2NO(g)N2(g)+2CO2(g)
(3)已知:N2(g)+O2(g) 2NO(g)
2NO(g)  H2=+181.0kJ·mol−1,CO的燃烧热
H2=+181.0kJ·mol−1,CO的燃烧热 H3=-283.5kJ·mol−l,则
H3=-283.5kJ·mol−l,则 H1=
H1=___________ kJ·mol−1。
(4)在绝热,恒容的密闭容器中,充入1molCO和1molNO,下列选项中不能说明该反应已经达到平衡状态的是___________。
(5)为探究温度和催化剂对反应的影响,分别在不同温度、不同催化剂下,保持其他条件不变,在相同时间内测得NO转化率与温度的关系如图所示。M点是否为平衡点___________ (填“是”或“不是”),M点以后,乙催化剂条件下,NO转化率降低,其原因是___________ 。___________ (填“>”或“<”)k逆增大的倍数;该温度下,Kp=___________ kPa-1。(保留小数点后2位)
注:Kp为用气体分压计算的平衡常数,气体分压等于气体总压×物质的量分数。
I.碘蒸气存在能大幅度提高N2O的分解速率,反应方程式为
 ,反应历程可表示为:
,反应历程可表示为:第一步(快反应) I2(g)
 2I(g)
2I(g)第二步(慢反应)

第三步(快反应) 2IO(g)+2N2O(g)→2N2(g)+2O2(g)+I2(g)
(1)写出第二步反应
(2)下列表述正确的是___________。
| A.增大I2的浓度能提高N2O的平衡转化率 | B.第二步活化能比第三步大 |
| C.第三步对总反应速率起决定作用 | D.IO为反应的催化剂 |
II.汽车尾气中含有较多的氮氧化合物和不完全燃烧的CO,汽车三元催化器可以将其转化成两种无污染的气体,从而降低氮氧化合物的排放量。
例如:2CO(g) +2NO(g)N2(g)+2CO2(g)

(3)已知:N2(g)+O2(g)
 2NO(g)
2NO(g)  H2=+181.0kJ·mol−1,CO的燃烧热
H2=+181.0kJ·mol−1,CO的燃烧热 H3=-283.5kJ·mol−l,则
H3=-283.5kJ·mol−l,则 H1=
H1=(4)在绝热,恒容的密闭容器中,充入1molCO和1molNO,下列选项中不能说明该反应已经达到平衡状态的是___________。
| A.CO和NO的物质的量之比不变 | B.混合气体的密度保持不变 |
| C.平衡常数K保持不变 | D.2ʋ(N2)正=ʋ(CO)逆 |
(5)为探究温度和催化剂对反应的影响,分别在不同温度、不同催化剂下,保持其他条件不变,在相同时间内测得NO转化率与温度的关系如图所示。M点是否为平衡点
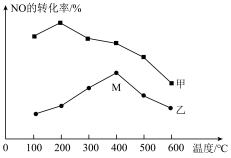
注:Kp为用气体分压计算的平衡常数,气体分压等于气体总压×物质的量分数。
您最近一年使用:0次
2 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知25℃时部分弱电解质的电离平衡常数如表所示,回答下列有关问题:
(1)25℃时,Na2S的水溶液呈_______ (填“酸性”、“中性”或“碱性”),原因是_______ (用离子方程式表示)。
(2)已知硼酸在水中可产生B(OH) ,则H3BO3在水中的电离方程式为
,则H3BO3在水中的电离方程式为_______ 。
(3)25℃时,浓度均为0.1mol/L的NaClO溶液和NaF溶液,c(Na+)-c(ClO-)_______ c(Na+)-c(F-) (填“>”、“=”或“<”)。
(4)已知某一元弱酸HA的电离常数K=2.5×10-10,则向Na2S溶液中加入过量的HA溶液,发生反应的离子方程式为_______ 。
(5)25℃时,将amol/L的氨水与0.05mol/L的稀硫酸等体积混合,若溶液中c(NH )=2c(SO
)=2c(SO ),此时溶液pH=
),此时溶液pH=_______ ,一水合氨的电离平衡常数为_______ (用含a的表达式来表示)。
Ⅱ.室温时,几种重金属离子的硫化物的溶度积常数如下表:
(6)向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是_______ (填离子符号);反应Cu2+(aq)+PbS(s) Pb2+(aq)+CuS(s)的平衡常数K=
Pb2+(aq)+CuS(s)的平衡常数K=_______ 。
(7)我国规定,工业废水中含Cr(VI)量的排放标准为0.1mg/L。已知:Ksp(BaCrO4)=1.2×10-10。若用Ba2+除去废水中的 ,达到废水排放标准时,废水中Ba2+浓度最低为
,达到废水排放标准时,废水中Ba2+浓度最低为_______ mol/L。
Ⅰ.已知25℃时部分弱电解质的电离平衡常数如表所示,回答下列有关问题:
| 物质 | H2S | H3BO3 | HF | HClO |
| 电离常数(K) | K1=1.1×10-7 K2=1.3×10-13 | 5.8×10-10 | 6.3×10-4 | 4.0×10-8 |
(2)已知硼酸在水中可产生B(OH)
 ,则H3BO3在水中的电离方程式为
,则H3BO3在水中的电离方程式为(3)25℃时,浓度均为0.1mol/L的NaClO溶液和NaF溶液,c(Na+)-c(ClO-)
(4)已知某一元弱酸HA的电离常数K=2.5×10-10,则向Na2S溶液中加入过量的HA溶液,发生反应的离子方程式为
(5)25℃时,将amol/L的氨水与0.05mol/L的稀硫酸等体积混合,若溶液中c(NH
 )=2c(SO
)=2c(SO ),此时溶液pH=
),此时溶液pH=Ⅱ.室温时,几种重金属离子的硫化物的溶度积常数如下表:
| 金属硫化物 | FeS | PbS | CuS | HgS |
| Ksp | 6.3×10-18 | 1.0×10-28 | 6.3×10-36 | 1.5×10-52 |
 Pb2+(aq)+CuS(s)的平衡常数K=
Pb2+(aq)+CuS(s)的平衡常数K=(7)我国规定,工业废水中含Cr(VI)量的排放标准为0.1mg/L。已知:Ksp(BaCrO4)=1.2×10-10。若用Ba2+除去废水中的
 ,达到废水排放标准时,废水中Ba2+浓度最低为
,达到废水排放标准时,废水中Ba2+浓度最低为
您最近一年使用:0次
3 . 温室气体二氧化碳的处理和再利用一直以来都是社会关注的热点问题。
(1)二氧化碳加氢制甲烷过程中的主要反应为:
Ⅰ.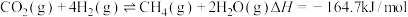
Ⅱ.
根据上述反应,请写出 与
与 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:_______ 。
(2) 时,在
时,在 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,起始时体系的压强为
,起始时体系的压强为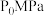 ,假设体系中只发生上述Ⅰ和Ⅱ两个反应,
,假设体系中只发生上述Ⅰ和Ⅱ两个反应, 时体系达到平衡状态,测得
时体系达到平衡状态,测得 的浓度为
的浓度为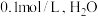 的浓度为
的浓度为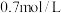 。
。
① ,用
,用 表示反应I的平均反应速率为
表示反应I的平均反应速率为_______ 。
②下列叙述能说明该体系已经达到平衡状态的是_______ (填标号)。
A.气体的密度不随时间变化 B. 的百分含量不再改变
的百分含量不再改变
C.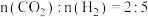 D.气体平均摩尔质量不随时间变化
D.气体平均摩尔质量不随时间变化
③该温度下反应I的平衡常数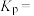
_______ 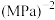 (用含
(用含 的代数式表示,
的代数式表示,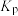 为以分压。表示的平衡常数,分压=总压
为以分压。表示的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
(3)二氧化碳催化加氢可制备甲醇: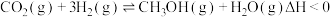 ,在起始物
,在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为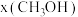 ,在
,在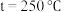 时,
时,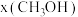 随压强
随压强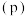 的变化以及在
的变化以及在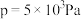 时
时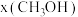 随温度(t)的变化,如图1所示。
随温度(t)的变化,如图1所示。_______ (填“a”或“b”),判断的理由是_______ 。
(4)电化学法还原二氧化碳可以制得乙烯( ),在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图2所示。则电解时阴极电极反应式为
),在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图2所示。则电解时阴极电极反应式为_______ ,在左侧电极每生成 乙烯,理论上在右侧生成气体的体积为
乙烯,理论上在右侧生成气体的体积为_______ L(标准状况下)
(1)二氧化碳加氢制甲烷过程中的主要反应为:
Ⅰ.
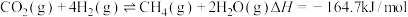
Ⅱ.

根据上述反应,请写出
 与
与 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:(2)
 时,在
时,在 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,起始时体系的压强为
,起始时体系的压强为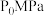 ,假设体系中只发生上述Ⅰ和Ⅱ两个反应,
,假设体系中只发生上述Ⅰ和Ⅱ两个反应, 时体系达到平衡状态,测得
时体系达到平衡状态,测得 的浓度为
的浓度为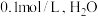 的浓度为
的浓度为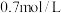 。
。①
 ,用
,用 表示反应I的平均反应速率为
表示反应I的平均反应速率为②下列叙述能说明该体系已经达到平衡状态的是
A.气体的密度不随时间变化 B.
 的百分含量不再改变
的百分含量不再改变C.
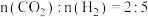 D.气体平均摩尔质量不随时间变化
D.气体平均摩尔质量不随时间变化③该温度下反应I的平衡常数
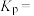
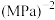 (用含
(用含 的代数式表示,
的代数式表示,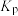 为以分压。表示的平衡常数,分压=总压
为以分压。表示的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。(3)二氧化碳催化加氢可制备甲醇:
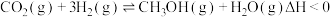 ,在起始物
,在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为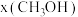 ,在
,在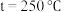 时,
时,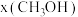 随压强
随压强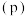 的变化以及在
的变化以及在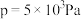 时
时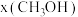 随温度(t)的变化,如图1所示。
随温度(t)的变化,如图1所示。
(4)电化学法还原二氧化碳可以制得乙烯(
 ),在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图2所示。则电解时阴极电极反应式为
),在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图2所示。则电解时阴极电极反应式为 乙烯,理论上在右侧生成气体的体积为
乙烯,理论上在右侧生成气体的体积为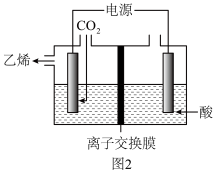
您最近一年使用:0次
4 . 很多过渡元素在生产和生活中都有比较广泛的应用。
Ⅰ.重铬酸钾可与酒精反应,可用于检测饮酒人员血液中的酒精含量,为了探究外界条件对重铬酸钾与酒精反应速率的影响,某学习小组进行了如下实验:
(1)上表中实验①和②可探究_______ 对化学反应速率的影响,则
_______ ;若利用实验①和③探究温度对化学反应速率的影响;则
_______ 。
(2)该实验可以通过测定_______ 来比较化学反应速率的大小。
II.有机螯合锰是一种稳定性比较好的锰的有机化合物,作为锰添加剂的来源,应用于营养强化剂、饲料添加剂和水溶肥料中。为测定某有机螯合锰中锰元素的含量(其余物质不参与反应),现进行如下操作:
(3)称取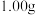 样品,置于
样品,置于 锥形瓶中,加
锥形瓶中,加 浓硫酸,瓶口盖小漏斗于电炉上加热消解,至有晶体析出时,稍冷,加
浓硫酸,瓶口盖小漏斗于电炉上加热消解,至有晶体析出时,稍冷,加 过氧化氢,继续加热
过氧化氢,继续加热 ,冷却,加
,冷却,加 水溶解,加
水溶解,加 焦磷酸钠饱和溶液,加
焦磷酸钠饱和溶液,加 过硫酸钾
过硫酸钾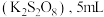 硝酸银溶液。此操作的目的在于将锰元素从有机物中转化为
硝酸银溶液。此操作的目的在于将锰元素从有机物中转化为 ,并在
,并在 催化下用
催化下用 将
将 氧化为
氧化为 。该操作中
。该操作中 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
(4)煮沸 去除过量的过硫酸钾,冷却,加入
去除过量的过硫酸钾,冷却,加入 氯化钠溶液,移入
氯化钠溶液,移入 容量瓶中定容静置
容量瓶中定容静置 后置于
后置于 滴定管中备用。此处滴定管应选用
滴定管中备用。此处滴定管应选用_______ (填“酸式”或“碱式”)滴定管中。
(5)取 上述溶液注入锥形瓶,加入
上述溶液注入锥形瓶,加入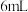 稀硫酸酸化,再用
稀硫酸酸化,再用 草酸钠溶液进行滴定(已知:
草酸钠溶液进行滴定(已知: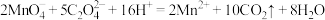 ),达到滴定终点的现象为
),达到滴定终点的现象为_______ 。
(6)重复上述操作,记录下草酸钠溶液滴定数据如下,则有机螯合锰中锰元素的质量分数为_______ 。
(7)若滴定前滴定管尖嘴部分有气泡,滴定后气泡消失,则测定出锰元素的质量分数_______ (填“偏高”、“偏低”或“无影响”)。
Ⅰ.重铬酸钾可与酒精反应,可用于检测饮酒人员血液中的酒精含量,为了探究外界条件对重铬酸钾与酒精反应速率的影响,某学习小组进行了如下实验:
| 实验序号 | 反应温度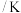 |  溶液 溶液 | 乙醇 | 稀硫酸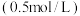 |  | |
 |  |  |  |  | ||
| ① | 298 | 5.0 | 0.2 | 5.0 | 2.0 | 0 |
| ② | 298 |  | 0.2 | 5.0 | 2.0 | 2.0 |
| ③ | 313 |  | 0.2 | 5.0 | 2.0 | 0 |


(2)该实验可以通过测定
II.有机螯合锰是一种稳定性比较好的锰的有机化合物,作为锰添加剂的来源,应用于营养强化剂、饲料添加剂和水溶肥料中。为测定某有机螯合锰中锰元素的含量(其余物质不参与反应),现进行如下操作:
(3)称取
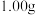 样品,置于
样品,置于 锥形瓶中,加
锥形瓶中,加 浓硫酸,瓶口盖小漏斗于电炉上加热消解,至有晶体析出时,稍冷,加
浓硫酸,瓶口盖小漏斗于电炉上加热消解,至有晶体析出时,稍冷,加 过氧化氢,继续加热
过氧化氢,继续加热 ,冷却,加
,冷却,加 水溶解,加
水溶解,加 焦磷酸钠饱和溶液,加
焦磷酸钠饱和溶液,加 过硫酸钾
过硫酸钾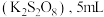 硝酸银溶液。此操作的目的在于将锰元素从有机物中转化为
硝酸银溶液。此操作的目的在于将锰元素从有机物中转化为 ,并在
,并在 催化下用
催化下用 将
将 氧化为
氧化为 。该操作中
。该操作中 转化为
转化为 的离子方程式为
的离子方程式为(4)煮沸
 去除过量的过硫酸钾,冷却,加入
去除过量的过硫酸钾,冷却,加入 氯化钠溶液,移入
氯化钠溶液,移入 容量瓶中定容静置
容量瓶中定容静置 后置于
后置于 滴定管中备用。此处滴定管应选用
滴定管中备用。此处滴定管应选用(5)取
 上述溶液注入锥形瓶,加入
上述溶液注入锥形瓶,加入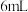 稀硫酸酸化,再用
稀硫酸酸化,再用 草酸钠溶液进行滴定(已知:
草酸钠溶液进行滴定(已知: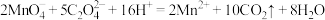 ),达到滴定终点的现象为
),达到滴定终点的现象为(6)重复上述操作,记录下草酸钠溶液滴定数据如下,则有机螯合锰中锰元素的质量分数为
| 滴定次数 | 滴定前/ | 滴定后/ |
| 第一次 | 0.05 | 15.08 |
| 第二次 | 1.23 | 17.22 |
| 第三次 | 0.22 | 15.19 |
您最近一年使用:0次
名校
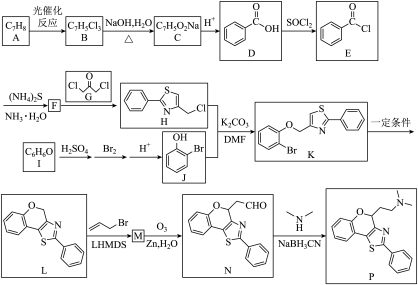
5 . 噻唑衍生物是重要的药物中间体,一种噻唑衍生物P的合成路线如下:
(1)A的结构简式为___________ ,G中官能团的名称是___________ ,J的名称是___________ 。
(2)H与J反应生成K的反应类型为___________ 。
(3)写出N和银氨溶液反应的化学方程式___________ 。
(4)B生成C的化学方程式为___________ 。
(5)已知L生成M是取代反应,则M的结构简式为___________ 。 在一定条件下能与以下哪些物质发生反应
在一定条件下能与以下哪些物质发生反应___________ 。
a.水 b.HCl c.氢氧化钠溶液
(6)Q是D与乙醇酯化后的产物,同时满足下列条件的Q的同分异构体的结构简式为___________ (任写2种)。
①与 溶液显色;
溶液显色;
②核磁共振氢谱显示有5组峰;
③只含两个环状结构且其中一个为苯环,两环不共边。
已知:①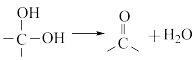 ;
;
②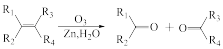 。
。
(1)A的结构简式为
(2)H与J反应生成K的反应类型为
(3)写出N和银氨溶液反应的化学方程式
(4)B生成C的化学方程式为
(5)已知L生成M是取代反应,则M的结构简式为
 在一定条件下能与以下哪些物质发生反应
在一定条件下能与以下哪些物质发生反应a.水 b.HCl c.氢氧化钠溶液
(6)Q是D与乙醇酯化后的产物,同时满足下列条件的Q的同分异构体的结构简式为
①与
 溶液显色;
溶液显色;②核磁共振氢谱显示有5组峰;
③只含两个环状结构且其中一个为苯环,两环不共边。
您最近一年使用:0次
名校
6 . 下列叙述正确的是
| A.少量苯酚与饱和溴水反应产生白色沉淀 | B.Fe与 反应生成碱 反应生成碱 |
| C.淀粉能与银氨溶液反应产生银镜 | D.Mg与 反应生成盐 反应生成盐 |
您最近一年使用:0次
7 . 可利用多种方法研究有机物的结构,如元素定量分析、质谱法、红外光谱分析和核磁共振氢谱分析等。下列有关说法正确的是
| A.利用质谱法可以鉴别乙醇和二甲醚 |
| B.利用红外光谱法可以鉴别甲苯和溴苯 |
C. 在核磁共振氢谱中有两组吸收峰 在核磁共振氢谱中有两组吸收峰 |
D.由某有机物完全燃烧的产物 可推测其实验式为 可推测其实验式为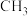 |
您最近一年使用:0次
8 . 储氢材料是当今研究的重点课题之一、X、Y是两种金属元素,都可制得储氢材料,X元素的基态原子价层电子排布式为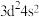 ,由它制得的储氢材料为
,由它制得的储氢材料为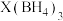 ;Y是短周期主族元素,其部分电离能(单位:
;Y是短周期主族元素,其部分电离能(单位: )数据如下表所示:
)数据如下表所示:
(1)X、Y两元素的元素符号分别是_______ 、_______ 。
(2)Y元素在周期表中的位置是_______ 。
(3)元素Y的基态原子具有_______ 种空间运动状态不同的电子。
(4)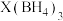 中所含化学键类型为
中所含化学键类型为_______ ,基态B原子的轨道表示式为_______ 。
(5)LiH与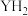 一样,都是具有良好发展前景的储氢材料。
一样,都是具有良好发展前景的储氢材料。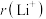
_______  (填“>”或“<”);
(填“>”或“<”);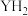 的电子式为
的电子式为_______ 。
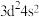 ,由它制得的储氢材料为
,由它制得的储氢材料为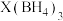 ;Y是短周期主族元素,其部分电离能(单位:
;Y是短周期主族元素,其部分电离能(单位: )数据如下表所示:
)数据如下表所示:
|
|
|
|
|
738 | 1451 | 7733 | 10540 | 13630 |
(2)Y元素在周期表中的位置是
(3)元素Y的基态原子具有
(4)
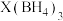 中所含化学键类型为
中所含化学键类型为(5)LiH与
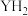 一样,都是具有良好发展前景的储氢材料。
一样,都是具有良好发展前景的储氢材料。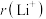
 (填“>”或“<”);
(填“>”或“<”);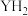 的电子式为
的电子式为
您最近一年使用:0次
2024-08-27更新
|
30次组卷
|
2卷引用:重庆市2023-2024学年高二上学期1月期末化学试题
解题方法
9 . 硫代硫酸钠( )主要用于照相业作定影剂,其次作鞣革时重铬酸盐的还原剂。实验室制备
)主要用于照相业作定影剂,其次作鞣革时重铬酸盐的还原剂。实验室制备 的装置如下图所示:
的装置如下图所示:_______ 。
(2)B装置的作用为_______ ,D装置中的试剂是_______ 。
(3) 溶液呈碱性的主要原因是
溶液呈碱性的主要原因是_______ (用离子方程式表示);常温下,pH=10的 溶液中,水电离出的
溶液中,水电离出的
_______ ; 溶液中,离子浓度由大到小的顺序是
溶液中,离子浓度由大到小的顺序是_______ (填离子符号)。
(4)取20mL上述制备的 溶液于锥形瓶中,将其调整呈弱酸性,滴入2滴淀粉溶液(溶液无色),用
溶液于锥形瓶中,将其调整呈弱酸性,滴入2滴淀粉溶液(溶液无色),用 的标准
的标准 溶液滴定,消耗标准
溶液滴定,消耗标准 溶液VmL。(已知:
溶液VmL。(已知: )。
)。
①盛装标准 溶液的滴定管是
溶液的滴定管是_______ 滴定管(填“酸式”或“碱式”)。
②滴定达到终点时的现象是_______ 。
③ 溶液的浓度为
溶液的浓度为_______  。
。
 )主要用于照相业作定影剂,其次作鞣革时重铬酸盐的还原剂。实验室制备
)主要用于照相业作定影剂,其次作鞣革时重铬酸盐的还原剂。实验室制备 的装置如下图所示:
的装置如下图所示: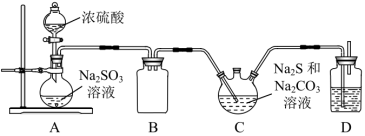
(2)B装置的作用为
(3)
 溶液呈碱性的主要原因是
溶液呈碱性的主要原因是 溶液中,水电离出的
溶液中,水电离出的
 溶液中,离子浓度由大到小的顺序是
溶液中,离子浓度由大到小的顺序是(4)取20mL上述制备的
 溶液于锥形瓶中,将其调整呈弱酸性,滴入2滴淀粉溶液(溶液无色),用
溶液于锥形瓶中,将其调整呈弱酸性,滴入2滴淀粉溶液(溶液无色),用 的标准
的标准 溶液滴定,消耗标准
溶液滴定,消耗标准 溶液VmL。(已知:
溶液VmL。(已知: )。
)。①盛装标准
 溶液的滴定管是
溶液的滴定管是②滴定达到终点时的现象是
③
 溶液的浓度为
溶液的浓度为 。
。
您最近一年使用:0次
2024-08-27更新
|
34次组卷
|
2卷引用:重庆市2023-2024学年高二上学期1月期末化学试题
10 . 下列说法正确的是
| A.活化分子之间的碰撞叫做有效碰撞 |
| B.生铁中含碳,生铁抗腐蚀能力比纯铁弱 |
| C.工业上合成氨压强越大越好 |
D.蒸干 和 和 溶液,所得固体成分相同 溶液,所得固体成分相同 |
您最近一年使用:0次
2024-08-27更新
|
19次组卷
|
2卷引用:重庆市2023-2024学年高二上学期1月期末化学试题







