9-10高一下·河北·期中
名校
解题方法
1 . 下列反应既是氧化还原反应,又是吸热反应的是
| A.铝片与稀硫酸反应 | B.Ba(OH)2·8H2O与NH4Cl反应 |
| C.灼热的炭与CO2反应 | D.甲烷在O2中的燃烧反应 |
您最近一年使用:0次
2023-12-09更新
|
350次组卷
|
247卷引用:甘肃省甘南藏族自治州合作第一中学2019-2020学年高二上学期期中考试理科化学试题
甘肃省甘南藏族自治州合作第一中学2019-2020学年高二上学期期中考试理科化学试题甘肃省甘南藏族自治州合作第一中学2019-2020学年高二上学期9月月考化学试题(已下线)2009-2010学年乐亭一中高一第二学期期中化学试题(已下线)09—10学年辽中第一私立高一下学期期末考试化学试题(已下线)2010年春季武汉睿升学校高一期中考试化学卷(已下线)09-10学年辽宁本溪一中高一下学期3月月考化学卷(已下线)09~10年黄冈中学高二下学期期末考试化学卷(已下线)2010年山西省汾阳中学高二上学期第二次月考(化学)(已下线)2010—2011学年广东省龙川一中高二3月月考(理科)化学部分(已下线)2010-2011学年广东省深圳高级中学高二下学期期中考试化学试卷(已下线)2010~2011学年辽宁省瓦房店市高级中学高一下学期期末考试(已下线)2011-2012学年云南大理云龙一中高二上学期期末考试化学试卷(已下线)2011-2012学年云南蒙自高中高二上学期期中考试化学试卷(已下线)2011-2012学年江苏省上冈高级中学高二下学期期中考试化学试卷(已下线)2011-2012学年太原五中高一下学期期中考试化学试卷(已下线)2011-2012学年四川省金堂中学高一下学期期中考试化学试卷(已下线)2011-2012学年江苏省盐城中学高一下学期期中考试化学试卷(已下线)2011-2012年湖南衡阳七校高二上学期期末质量检测化学试卷(已下线)2012-2013学年昆明三中、滇池中学高一下期中考试化学卷(滇中)(已下线)2013届河北省石家庄市第二实验中学高二上学期期中考试理科化学试卷(已下线)2012-2013学年江西省白鹭洲中学高一下学期期中考试化学试卷(已下线)2012-2013学年甘肃省兰州一中高一下学期期末考试化学试卷(已下线)2012-2013学年贵州省黔西一中高一第二学期期末检测化学试卷(已下线)2012-2013学年山东省临沂市高二上学期期中考试化学试卷(已下线)2013-2014学年陕西省岐山县高二上学期期中质量检测理科化学试卷(已下线)2013-2014学年江苏省南师附中江宁分校高二上学期选修期末化学试卷(已下线)2013-2014学年江西省新余市高二上学期期末考试化学试卷(已下线)2013-2014云南省玉溪一中高一下学期期末考试化学试卷(已下线)2013-2014宁夏大学附属中学高一下学期期中考试化学试卷2014-2015河北邢台一中高一3月月考化学试卷2014-2015学年四川省德阳市第五中学高一下学期期中考试化学试卷2014—2015学年福建省厦门市高一下期末质量检测化学试卷2014-2015学年四川眉山市高一第二学期期末教学质量检测化学试卷2015-2016学年河北省容城中学高二上学期第一次月考化学试卷2015-2016学年河北省定兴第三中学高二上学期第一次月考化学试卷2015-2016学年河北省行唐启明中学高二上学期第一次月考化学试卷2015-2016学年山东省淄博市淄川一中高二上学期期中测试化学试卷2015-2016学年湖南省株洲十八中高二上学期期中(理)化学试卷2015-2016学年广东省宝安第一外国语学校高二上期中考试化学试卷2015-2016学年河北省保定一中高二上学期第一次段考化学试卷2015-2016学年内蒙古巴彦淖尔一中高一上期末化学试卷22015-2016学年宁夏银川二中高一下3月月考化学试卷2015-2016学年湖南省岳阳市岳阳一中高一下3月月考化学试卷2015-2016学年贵州省习水一中高一下学期期中考试化学试卷2015-2016学年天津市耀华中学高一下期中化学试卷2015-2016学年广东实验中学高一下期中化学试卷2015-2016学年甘肃省会宁四中高一下学期期中考试化学试卷2015-2016学年广西南宁市八中高二下学期期中段考化学试卷2015-2016学年甘肃省会宁二中高一下学期期中化学试卷2015-2016学年浙江省绍兴一中高一下期中化学试卷2015-2016学年四川省雅安市天全中学高一下学期期中考试化学试卷2015-2016学年山西省右玉一中高一下学期期中考试化学试卷2015-2016学年新疆石河子二中高一下学期第二次月考化学试卷2015-2016学年辽宁省实验中学分校高一下期中化学试卷2015-2016学年河南省洛阳八中高一下学期5月月考化学试卷2015-2016学年湖北省枣阳二中高二下学期期中考试化学试卷2015-2016学年江西省南昌市八一、洪都等五校高一下期末化学试卷2015-2016学年新疆农业大学附中高一下学期期中化学试卷2015-2016学年宁夏中卫市海原一中高一下第二次月考化学试卷2015-2016学年陕西省宝鸡市岐山县高一下期末质检化学试卷2017届吉林省吉林二中高三上学期9月月考化学试卷2016-2017学年福建省三明一中高二上第一次月考化学卷2016-2017学年宁夏育才中学高二上学期期中化学卷2016-2017学年河北省秦皇岛北戴河中学高二上月考化学试卷2016-2017学年江苏省清江中学高二上期中选修化学卷2016-2017学年湖北省孝感市七校教学联盟高一下学期期中考试化学试卷2016-2017学年河南省洛阳市高一下学期期中考试化学试卷黑龙江省伊春市第二中学2016-2017学年高一下学期期中考试(理)化学试题黑龙江省伊春市第二中学2016-2017学年高一下学期期中考试(文)化学试题山西省怀仁县第一中学2016-2017学年高一下学期第三次(5月)月考化学试题云南省曲靖市第一中学2016-2017学年高一下学期期中考试化学试题贵州省遵义航天高级中学2016-2017学年高一下学期第三次月考理科综合化学试题贵州省遵义航天中学2016-2017学年高一下学期第三次月考化学试题山西省汾阳中学2016-2017学年高一下学期期中考试(理)化学试题湖北省孝感市七校教学联盟2016-2017学年高一下学期期末考试化学试题广西宾阳县宾阳中学2016-2017学年高一下学期7月期末考试(文)化学试题新疆呼图壁县一中2016-2017学年高一下学期期末考试化学试题黑龙江省伊春市第二中学2016-2017学年高一下学期期末考试(理)化学试题黑龙江省鹤岗市第一中学2016-2017学年高一下学期期末考试化学试题1黑龙江省鹤岗市第一中学2016-2017学年高一下学期期末考试化学试题2甘肃省武威市第六中学2017-2018学年高二上学期第一次学段考试化学试题云南省姚安县第一中学2017-2018学年高二10月月考化学试题新疆昌吉市2017-2018学年高二上学期期末考试化学试题《课时同步君》2017-2018学年高一化学人教必修2-2.1 化学能与热能甘肃省嘉峪关市一中2017-2018学年高二上学期期末考试化学(理)试题(已下线)《周末培优君》2017-2018学年高一下学期化学-第05周 化学能与热能【全国市级联考】江苏省宿迁市2017-2018学年高一下学期期中考试化学试题海南省热科院两院中学2017-2018高一下学期期中考试化学试题【全国百强校】贵州省铜仁市第一中学2017-2018学年高一下学期期中考试化学试题【全国百强校】新疆生产建设兵团第二中学2017-2018学年高一下学期期中考试化学试题四川省威远中学2017-2018学年高一下学期期中考试化学试题【全国校级联考】河南省商丘市九校2017-2018学年高一下学期期末联考化学试题【全国百强校】黑龙江省双鸭山市第一中学2017-2018学年高一下学期期末考试化学试题安徽师范大学附属中学2017-2018学年高一下学期期末模拟化学试题山西省忻州二中2017-2018学年高一下学期期中考试化学试题甘肃省岷县二中2018-2019学年高二上学期第一次月考化学试题安徽省滁州市定远县育才学校2018-2019学年高二(实验班)上学期第一次月考化学试题河南省鹤壁市淇滨高级中学2018-2019学年高二上学期第一次月考化学试题陕西省西安市远东第一中学2018-2019学年高二上学期10月月考化学试题河南省安阳市第三十六中学2018-2019学年高二上学期第一次月考化学试题四川省成都外国语学校2018-2019学年高二上学期半期考试化学试题【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期期中考试化学试题【全国百强校】山东省济南第一中学2018-2019学年高二上学期期中考试化学试题甘肃省白银市靖远县第四中学2018-2019学年高二上学期期中考试化学试题江苏省泰州市第二中学2017-2018学年高二上学期期中考试化学试题江西省铅山县第一中学2018-2019学年高二上学期期中考试化学试题浙江省余姚中学2018-2019学年高二上学期10月月考化学试题江西省分宜中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】广东省佛山市第一中学2018-2019学年高二(文)下学期期中考试化学试题吉林省乾安县第七中学2018-2019学年高一下学期第二次质量检测化学试题甘肃省兰州市第一中学2018-2019学年高一下学期期末考试化学试题黑龙江省双鸭山市第一中学2018-2019学年高一下学期期末考试化学试题山西省应县第一中学校2018-2019学年高一下学期期中考试化学试题云南省峨山彝族自治县第一中学2018-2019学年高一下学期期中考试化学试题新疆兵团八师一四三团一中2018-2019学年高一下学期期中考试化学试题山西省大同市铁路第一中学2018-2019学年高一下学期第三次月考化学试题河北省鸡泽县第一中学2019-2020学年高二10月月考化学试题河北省唐山一中2019-2020学年高二上学期10月月考化学试题浙江省台州市五校2020届高三10月联考化学试题贵州省思南中学2019-2020学年高二9月月考化学试题福建省漳平市第一中学2019-2020学年高二上学期第一次月考化学试题吉林省辽源市田家炳高级中学2019-2020学年高二上学期期中考试化学试题福建省泉州市永春华侨中学2019-2020学年高二上学期期中考试化学试题内蒙古呼和浩特开来中学2019-2020学年高二上学期期中考试化学试题新疆阿瓦提县第四中学2019-2020学年高二上学期期中考试化学试卷湖南省怀化市第三中学2018-2019学年高一下学期3月月考化学试题湖北省宜昌市长阳县第一高级中学2019-2020学年高二上学期期中考试化学试题湖北省宜昌市第二中学(人文艺术高级中学)2019-2020学年高二上学期10月月考化学试题广西北海市北海中学2019-2020学年高二上学期期中考试化学试题吉林省普通高中联合体2018-2019学年高二下学期期末联考化学试题云南省屏边县民族中学2019-2020学年高二上学期12月月考化学试题宁夏吴忠市盐池高级中学2019-2020学年高二上学期期末检测化学试题2019秋人教版高中化学必修2第二章 《化学反应与能量》同步训练题陕西省汉中市龙岗学校2019-2020学年高二上学期期末考试化学试题(文)2020届高考化学知识点必练——氧化还原反应的本质及相关概念辽宁省抚顺市六校协作体2019-2020学年高二上学期期末考试化学试题福建省莆田市仙游县枫亭中学2019-2020学年高二上学期期中考试(选考)化学试题6.1.1 化学反应与热能——2020年春高一新人教版第二册化学一课一练河北省正定中学2019-2020学年高一3月月考化学试题课时1 化学反应与热能——A学习区 夯实基础(人教版(2019)第二册)课时1 化学反应中能量变化的本质及转化形式——A学习区 夯实基础(鲁科版(2019)第二册)课时2 化学键与化学反应中的能量变化——A学习区 夯实基础(鲁科版必修2)湖北省武汉市第三十九中学2019-2020学年高一下学期线上期中考试化学试题2020年春高一化学新人教版第二册课后同步:6.1.1 化学反应与热能吉林省延边市长白山第一高级中学2019-2020学年高一下学期验收考试化学试题山西省晋中市和诚中学2019-2020学年高一4月月考化学试题湖北省武汉市2019-2020学年高一下学期期中联考化学试卷广东省湛江市第二十一中学2019-2020学年高二下学期开学考试化学试题山西省运城市高中联合体2019-2020学年高一下学期第一次摸底考试化学试题贵州省铜仁市思南中学2019-2020学年高一下学期5月月考化学试题广西壮族自治区田阳高中2019-2020学年高一5月月考化学试题宁夏吴忠中学2019-2020学年高一下学期期中考试化学试题辽宁省大连市普兰店区第一中学2019-2020学年高一下学期5月线上教学质量检测化学试题河北省石家庄市元氏县第四中学2019-2020学年高一下学期摸底考试化学试题宁夏银川市宁夏大学附属中学2019-2020学年高一下学期期中考试化学试题黑龙江省海林市朝鲜族中学2019-2020学年高一下学期期末考试化学试题吉林省辽源市田家炳高级中学等友好学校2019-2020学年高一下学期期末考试化学试题河北省衡水市深州市中学2019-2020学年高二下学期期中考试化学试题(已下线)1.1.1 化学反应的反应热 内能变化 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1黑龙江省哈尔滨师范大学青冈实验中学校2019-2020学年高二上学期开学考试(8月)化学试题黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高二上学期开学考试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第1节 化学反应的热效应四川省广安市北京师范大学广安实验学校2020-2021学年高二上学期9月月考化学试题必修第二册RJ第6章第一节 化学反应与能量变化 课时1宁夏回族自治区青铜峡市高级中学2020-2021学年高二上学期第一次月考化学试题山东省新泰市第一中学北校2020-2021学年高二上学期第一次月考化学试题山东省临沂市费县地区化学2020-2021学年高二上学期9月月考化学试题山西省运城市新绛县第二中学2019-2020学年高一下学期3月月考化学试题广东省东莞市第四高级中学2020-2021学年高二上学期期中考试化学试题安徽省蚌埠第三中学2019-2020学年高一下学期5月月考化学试题宁夏长庆高级中学2020-2021学年高二上学期期中考试化学试题浙江省杭州市富阳区第二中学2020-2021学年高二上学期期中考试化学试题浙江省“七彩阳光”新高考研究联盟2020-2021学年高二上学期期中联考化学试题吉林省榆树市第一高级中学2021届高三上学期第三次模拟考试化学试题(已下线)【浙江新东方】绍兴qw126黑龙江嫩江市高级中学2020-2021学年高二上学期期末考试化学试题吉林省白山市抚松县第五中学2020-2021学年高二上学期期中考试化学试题高中化学苏教2019版必修第二册-专题6 第二单元 第1课时 放热反应与吸热反应山东省滨州市阳信县第二高级中学2020-2021学年高二上学期期中考试化学试题甘肃省武威市民勤县第四中学2021届高三上学期期末考试(实验班)化学试题宁夏银川一中2020-2021学年高二上学期期末考试化学试题山西省沁县中学2020-2021学年高二上学期第一次月考化学试题湖南省长沙宁乡市第十高级中学2020-2021学年高二上学期10月月考化学试题吉林省长春市第二十中学2019-2020学年高一下学期期末考试化学试题甘肃省天水市田家炳中学2019-2020学年高一下学期期中考试化学试题浙江省湖州市2020-2021学年高二上学期期末调研测试化学试题浙江省杭州市萧山三中2020-2021学年高一下学期四校4月阶段联考化学试题河北省衡水市安平中学2020-2021学年高一下学期第一次月考化学试题甘肃省酒泉市青海油田第一中学2020-2021学年高一下学期期中考试化学试题(已下线)【浙江新东方】在线化学87高一下江苏省苏州外国语中学2020-2021学年高二下学期3月月考化学试题甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(文)试题辽宁省阜新市第二高级中学2020-2021学年高一下学期期中考试化学试题青海省海南州贵德高级中学2020-2021学年高二下学期期中化学试题(已下线)【镇江新东方】高一下第一次月考一中镇中联考江西省赣州市信丰中学2020-2021学年高二上学期入学考试化学试题宁夏长庆高级中学2020-2021学年高一下学期期末考试化学试题吉林省通化县综合高级中学2020-2021学年高一下学期期末考试化学试题甘肃省天水市田家炳中学2020-2021学年高一下学期期末考试化学试题浙江省磐安县第二中学2019-2020学年高二10月竞赛化学试题新疆乌苏市第一中学2021-2022学年高二上学期10月月考化学试题浙江省温州市瑞安市上海新纪元高级中学2021-2022学年高一9月份月考(1-4班)化学试题青海省西宁市海湖中学2021-2022学年高二上学期第一次月考化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高一下学期期中考试化学试题浙江省宁波市咸祥中学2021-2022学年高二上学期期中考试化学试题湖南省常德市外国语学校2021-2022学年高二上学期期中考试化学试题上海市徐汇中学2021-2022学年高二上学期期中考试化学(等级考)试题河南省驻马店市第一高级中学2021-2022学年高二上学期期中考试化学试题 重庆市朝阳中学2021-2022学年高二上学期期中考试化学试题安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题(已下线)第03讲 放热反应与吸热反应-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)(已下线)章末培优 第6章 化学反应与能量-2021-2022学年高一化学课后培优练(人教版2019必修第二册)江苏省盐城市伍佑中学2021-2022学年高一下学期学情调研(一)化学试题新疆乌鲁木齐市第三十一中学2021-2022学年高二上学期期中考试化学试题浙江省杭州市西湖高级中学2021-2022学年高一下学期期中考试化学试题宁夏灵武市第一中学2021-2022学年高一下学期期中考试化学试题福建省漳州市正兴学校等三校2021-2022学年高一下学期期中联考化学试题(已下线)第05练 化学能与热能-2022年【暑假分层作业】高一化学(人教版2019必修第二册)(已下线)1.1.1 系统的内能和反应热-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.1.1 系统的内能和反应热-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第24练 反应热-2023年高考化学一轮复习小题多维练(全国通用)安徽省阜阳市临泉县第一中学2021-2022学年高二下学期开学考试化学试题浙江省湖州市三贤联盟2021-2022学年高二上学期期中考试化学试题天津市河东区三校2020-2021学年高一下学期期中联考化学试题(已下线)1.1.1 反应热(一)-同步学习必备知识湖南省邵阳市洞口县第二中学2021-2022学年高一下学期第一次月考化学试题重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题湖北省黄冈市麻城市第二中学2021-2022学年高一下学期3月月考化学试题 浙江省舟山市南海实验高中2021-2022学年高一下学期4月月考化学试题甘肃省白银市第九中学2020-2021学年高一下学期期中考试化学试题河南省濮阳市南乐县第一高级中学2022-2023学年高二上学期第一次月考化学试题浙江省玉环市玉城中学2022-2023学年高二上学期第一次月考化学试题 甘肃省靖远县第二中学2021-2022学年高二上学期期中考试(二)化学(理)试题陕西省安康市汉滨区五里高级中学2021-2022学年高二上学期期中考试化学试题陕西省西安市周至县第四中学2021-2022学年高二上学期期中考试化学(理科)试题甘肃省徽县第一中学2021-2022学年高二上学期11月月考化学试题山东省菏泽市成武县第二中学2021-2022学年高一下学期第一次月考化学试题湖北省黄冈市麻城第二中学2021-2022学年高一下学期4月月考化学试题广东省汕头市澄海中学2020-2021学年高一下学期期中考试合格考化学试题黑龙江省鸡西市鸡冠区2022-2023学年高二上学期10月月考化学试题青海省海南藏族自治州高级中学2022-2023学年高二下学期期末考试化学试题贵州省铜仁市松桃民族中学2023-2024学年高二上学期9月月考化学试题海南省海口市长流中学2022-2023学年高一下学期第1次月考化学试题A卷海南省农垦中学2023-2024学年高二上学期期末考试化学试题(A卷)(已下线)FHgkyldyjhx11甘肃省兰州市教育局第四片区2023-2024学年高一下学期期中考试化学试卷名校期末好题汇编-化学反应与能量(选择题)
9-10高二下·浙江温州·期末
名校
解题方法
2 . 在25 ℃、101 kPa下,碳、氢气、甲烷和葡萄糖的摩尔燃烧焓依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2 800 kJ/mol,则下列热化学方程式正确的是
A.C(s)+ O2(g)=CO(g) ΔH=-393.5 kJ/mol O2(g)=CO(g) ΔH=-393.5 kJ/mol |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol |
| C.2H2(g)+O2(g)=2H2O(l) ΔH=+571.6 kJ/mol |
D. C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) ΔH=-1 400 kJ/mol C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) ΔH=-1 400 kJ/mol |
您最近一年使用:0次
2023-08-26更新
|
1382次组卷
|
53卷引用:甘肃省舟曲县第一中学2021-2022学年高二上学期第一次月考化学试题
甘肃省舟曲县第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)09-10年温州市高二下学期期末四校联考化学卷(已下线)2010年河北省邯郸市高二上学期期末考试化学试卷(已下线)2010—2011学年湖北省长阳一中高二上学期期末考试化学试卷(已下线)2011-2012学年陕西省西安市第一中学高二上学期期中考试化学试卷(已下线)2011-2012学年海南省洋浦中学高二下学期期末考试化学试卷(已下线)2011-2012学年江西上饶中学高一零点、实验班下期末化学试卷(已下线)2013届陕西省宝鸡市高三第三次模拟理综化学试卷(已下线)2013-2014学年海南省三亚市一中高二上学期期中考试理科化学试卷(已下线)2013-2014学年海南三亚一中高二上学期期中考试理科化学试卷(B)(已下线)2014届高考化学二轮复习提分训练 专题5化学反应与能量练习卷(已下线)2014-2015学年山西省太原第五中学高二10月月考化学试卷2014-2015四川省邛崃市高埂中学高二下学期第一次月考化学试卷2015-2016学年贵州省思南中学高二上第一半月考化学试卷2016届贵州省遵义航天高级中学高三第五次模拟理科综合试卷2016届海南省华侨中学高三考前模拟理综化学试卷2016-2017学年河北省涿鹿中学高二上学期第一次月考化学试卷2016-2017学年吉林省汪清六中高二上第一次月考化学试卷2016-2017学年广西柳州铁路一中高二上段考理化学卷辽宁省鞍山市第一中学2016-2017学年高一下学期期中考试化学试题宁夏银川市六盘山高级中学2017-2018学年高二上学期第一次月考化学试题山东省临沂市蒙阴县实验中学2017-2018学年高二上学期期中考试化学试题1山东省临沂市蒙阴县实验中学2017-2018学年高二上学期期中考试化学试题2山西省忻州二中2018-2019学年高二上学期期中考试化学试题(已下线)2019年9月1日《每日一题》人教选修4—— 每周一测河南省周口中英文学校2019-2020学年高二上学期第一次月考化学试题四川省广安市岳池县顾县中学2019—2020学年第一学期高二上学期期中测试化学(选修四)试题山西省运城市景胜中学2019-2020学年高二上学期期中考试化学试题江西省上饶市“山江湖”协作体2019-2020学年高二上学期期中联考(自主班)化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题(已下线)1.2 燃烧热 能源(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)内蒙古自治区通辽市科左后旗甘旗卡第二高级中学2020-2021学年高二上学期期中考试化学试题河南省豫北名校2020-2021学年高二上学期11月质量检测化学试题华中师范大学海南附属中学2019-2020学年高二上学期第三次月考化学试题江苏省南菁高级中学2020-2021学年度高二上学期第一次阶段性考试化学(强化班)试题江苏省江阴长泾中学2020~2021学年下学期期中考试化学试题青海省海东市第二中学2020-2021学年高二4月月考化学试题吉林省长春外国语学校2020-2021学年高一下学期期末考试化学试题(已下线)第二节 燃烧热 能源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)1.1.2 热化学方程式 燃烧热-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题18 化学反应与能量(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练江西省吉安市(吉安县三中、泰和二中、安福二中、井大附中 )2021-2022学年高二上学期期中考试化学试题山西省运城市康杰中学2021-2022学年高二上学期期中化学试题(已下线)1.1.2 热化学方程式 燃烧热(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)1.1.2 热化学方程式 燃烧热(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第02讲 热化学方程式与燃烧热(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)第一章 化学反应的热效应(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)云南省昆明市寻甸县第二中学2022-2023学年高二上学期10月月考 化学试卷(已下线)单项选择题第3课时 反应焓变的计算(已下线)专题01 反应热、焓变与热化学方程式【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
9-10高一下·河北衡水·期中
名校
解题方法
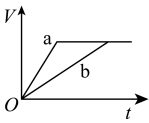
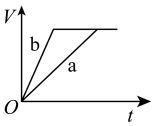
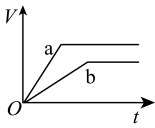
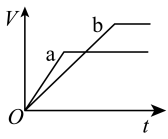
3 . 等质量且足量的两份锌a、b,分别加入等量的稀H2SO4,同时向a中加入少量的CuSO4溶液,下列各图表示产生H2的体积(V)与时间(t)的关系,其中正确的是
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-11更新
|
596次组卷
|
281卷引用:甘肃省甘南藏族自治州合作第一中学2018-2019学年高一下学期期中考试化学试题
甘肃省甘南藏族自治州合作第一中学2018-2019学年高一下学期期中考试化学试题(已下线)2009—2010学年河北冀州中学高一下学期期中考试化学卷(已下线)09~10学年三明市五校高一下学期期中联考化学卷(已下线)09-10年郑州智林学校高一下学期阶段测试2化学卷(已下线)2010年山西省忻州市高一下学期期末联考化学(A类)试题(已下线)2010年福建省福州市八县(市)协作校第一学期期中联考高二理科化学试卷(已下线)2011届福建省莆田一中高三上学期第三次月考化学试卷(已下线)2010-2011学年河南省许昌市高一下学期四校期中联考化学试卷(已下线)2010-2011学年黑龙江省鹤岗一中高一下学期期中考试化学试卷(已下线)2010-2011学年辽宁省师大附中高一下学期期中考试化学试卷(已下线)2010—2011学年山东省潍坊市三县高一下学期期末联考化学试卷(已下线)2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷(已下线)2011-2012年学福建省永安一中高二上学期期中考试化学试卷(已下线)2012届山东省淄博市第一中学高三上学期期中模块考试化学试卷(已下线)2011-2012学年福建省罗源县第一中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年甘肃省天水市一中高二上学期期末考试化学试卷(已下线)2011-2012学年浙江省开化县华埠中学高二下学期3月月考试卷(已下线)2011-2012学年湖南省望城一中高一下学期期中考试化学试卷(已下线)2011-2012学年重庆市南川三中高一下学期期中考试化学试卷(已下线)2011-2012学年甘肃省张掖二中高一下学期期中考试化学试卷 (已下线)2011-2012学年辽宁省开原高中高一下学期期中考试化学试卷(已下线)2011-2012学年陕西省宝鸡中学高二下学期期中考试化学试题(已下线)2011-2012学年甘肃白银市平川中恒学校高一下学期期末考试化学试卷(已下线)2011-2012学年陕西省长安一中高一下学期期末考试化学试卷(已下线)2011-2012学年河北省邯郸市高一下学期期末教学质量检测化学试卷(已下线)2011-2012学年浙江省余姚中学高二下学期期中考试实验班化学试卷(已下线)2011-2012学年广东省执信中学高一下学期期末考试化学试卷(已下线)2011-2012学年山东省泰安宁阳二中高二下学期期末考试化学试卷(已下线)2012年人教版高中化学选修4 2.2影响化学反应速率的因素练习卷(已下线)2012-2013学年海南省琼海市嘉积中学高二下学期第一次月考化学试卷(已下线)2012-2013学年新疆乌鲁木齐市一中高一(平行班)下学期期中考试化学试卷(已下线)2012-2013学年江苏省宿迁青华中学高二下学期期中考化学普通班试卷(已下线)2012-2013学年山东省临沭一中高二12月学情调查化学试卷(已下线)2012-2013学年广西毕节燕中高一下学期期末考试化学试卷(已下线)2012-2013学年四川省资阳市高一下学期期末检测化学试卷(已下线)2013-2014学年福建省福州八县一中高二上学期期中联考化学试卷(已下线)2014年高一下学期化学必修2 2-2-1 化学能转化为电能练习卷(已下线)2013-2014学年浙江省杭州及周边重点中学高一下学期期中考化学试卷(已下线)2013-2014福建安溪一中、惠安一中、养正中学下学期期中高二化学(已下线)2013-2014广西桂林中学高一下学期期中考试化学试卷(已下线)2013-2014湖南省五市十校高一下学期期中教学质量检测化学试卷(已下线)2013-2014山西省山大附中高一下学期期中化学试卷(已下线)2013届新疆乌鲁木齐市一中高一下学期平行班期中考试化学试卷(已下线)2014届云南省昆明滇池中学高一下学期期中考试化学试卷(已下线)2013-2014甘肃省嘉峪关市第二学期期末高一联合考试化学试卷(已下线)2013-2014宁夏银川一中下学期期中考试高二化学试卷(已下线)2013-2014吉林省长春市十一中高一下学期期末考试化学试卷(已下线)2015届江西省遂川中高三上学期第一次月考化学试卷(已下线)2015届安徽望江中学同步课时练(人教选修4)4.1原电池试卷(已下线)2013-2014学年福建省长乐第一中学高二上学期第二次月考化学试卷(已下线)2014-2015学年浙江台州中学高二上学期第一次统练化学试卷(已下线)2014-2015学年浙江省温州市十校联合体高二上学期期中联考化学试卷2014-2015学年福建省安溪八中高二上学期期中化学(理)试卷2014-2015河南省濮阳市一中高二上学期第三次质量检测化学试卷2015届福建省三明市一中高三上学期第二次月考化学试卷2014-2015河南省濮阳市一中高二上学期第三次月考化学试卷2014-2015湖南省五市十校高一下学期期中联考化学试卷2014-2015浙江省杭州地区七校高一下学期期中联考化学试卷2014-2015安徽省宣郞广三校高一下学期期中联考化学试卷2014-2015学年广东省深圳市明珠学校高二上学期期中化学试卷2014-2015学年安徽省涡阳四中高一下第二次质检化学试卷2014-2015学年河南省扶沟县高级中学高一5月月考化学试卷2014-2015学年湖北省宜昌市一般高中高一期末化学试卷2015-2016学年河南省扶沟县高级中学高二开学考试化学试卷2015-2016学年浙江余姚中学高二上学期期中考试化学试卷2015-2016学年河北衡水冀州中学高二上月考三化学试卷2015-2016学年山西忻州第一中学高二上期中考试化学试卷2015-2016学年湖南宁远一中、祁阳一中高二上第二次联考化学试卷2015-2016学年福建省师大附中高二上期末理化学试卷2015-2016学年山西省孝义市高二上学期期末考试化学试卷2015-2016学年广西河池市高中高一下第一次月考化学试卷2015-2016学年山西省怀仁一中高一下期中化学试卷2015-2016学年甘肃省会宁二中高一下学期期中化学试卷2015-2016学年河北省冀州中学高一下期中化学试卷2015-2016学年安徽六安一中高一下周末作业四化学试卷2015-2016学年天津市静海县六校高一下学期期中联考化学试卷2015-2016学年江苏省泰州中学高一创新班下期末化学试卷2015-2016学年山西省长治一中高一平行班下期中化学试卷2015-2016学年吉林东北师大附属实验高一下期末化学试卷2016-2017学年河北省望都中学高二8月月考化学试卷2016-2017学年辽宁省大连市第二十中学高二上9月月考化学试卷2016-2017学年山东省枣庄八中高二上10月月考化学卷2016-2017学年浙江省慈溪市高二上学期期中化学试卷2016-2017学年河北省张家口市第一中学高一(衔接班)3月月考(文)化学试卷吉林省实验中学2016-2017学年高一下学期期中考试化学试题福建省三明市第一中学2016-2017学年高一下学期半期考试化学试题安徽省黄山市屯溪第一中学2016-2017学年高一下学期期中考试化学试题山东省济南市第一中学2016-2017学年高一下学期期中考试化学试题浙江省金华市东阳中学2016-2017学年高一6月月考化学试题浙江省东阳中学2016-2017学年高一5月月考化学试题江西省南昌市第三中学2016-2017学年高一下学期5月月考化学试题山东省临沂市罗庄区2016-2017学年高一下学期期末考试化学试题河北省唐山市开滦第二中学2016-2017学年高二下学期期末考试化学试题内蒙古北京八中乌兰察布分校2016-2017学年高一下学期期末考试化学试题广东省仲元中学2016-2017学年高一下学期期末考试(理)化学试题山西省太原市黄陵中学高新部2017-2018学年高二上学期开学考化学试题贵州省思南中学2017-2018学年高二上学期第一次月考化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题A内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B河北省唐山市开滦第二中学2017-2018学年高二上学期期中考试化学试题福建省福州市八县(市)协作校2017-2018学年高二上学期期中联考化学(理)试题黑龙江省哈尔滨三中2017-2018学年高二上学期11月第一次验收考试化学试题北京市第161中学2017-2018学年高二上学期期中适应性训练化学试题陕西省黄陵中学2018届高三(重点班)上学期期中考试化学试题安徽省滁州市定远县西片三校2017-2018学年高二上学期期末考试化学试题湖南省衡阳县2017-2018学年高二上期期末考试化学试题安徽省定远重点中学2017-2018学年高一下学期第一次月考化学试题甘肃省武威第十八中学2017-2018学年高二下学期第一次月考化学试题【全国百强校】安徽省屯溪第一中学2017-2018学年高一下学期期中考试化学试题(已下线)解密09 电化学(教师版)——备战2018年高考化学之高频考点解密【全国百强校】黑龙江省双鸭山市第一中学2017-2018学年高一下学期第二次6月月考化学试题【全国市级联考】浙江省温州市共美联盟2017-2018学年高一下学期期末模拟化学试题贵州省毕节市威宁县黑石中学2017-2018学年高一下学期6月份考试化学试题江西省樟树中学2017-2018学年高一下学期第三次月考化学试题【全国校级联考】湖北省孝感市八校教学联盟2017-2018学年高一下学期期末联合考试化学试题吉林省榆树一中2017-2018学年高一下学期期末考试化学试题【全国百强校】西藏自治区拉萨中学2017-2018学年高一下学期期末考试化学试题贵州省钟山区水钢实验学校2017-2018学年高一下学期期末考试化学试题贵州省六盘水盘县四中2017-2018学年高一下学期期末考试化学试题河北省蠡县中学2018-2019学年高二上学期第一次(8月)月考化学试题山西省长治市第二中学2017-2018学年高一下学期期末考试化学试题河北省保定市蠡县中学2018-2019学年高二上学期9月月考化学试题吉林省辽源市田家炳高级中学2018-2019学年高二9月月考化学试题吉林省白城市第一中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】河南省信阳市高级中学2018-2019学年高二上学期10月月考化学试题2【校级联考】福建省闽侯二中五校教学联合体2017-2018学年高二上学期期中考试化学试题安徽省天长市天长二中2018-2019学年高二第一学期12月月考化学试题陕西省白水中学2018-2019学年高二上学期第二次月考化学试题山东省泰安市宁阳一中2018-2019学年高二上学期阶段性考试三(12月)化学试题(已下线)考点09 原电池原理及其应用——备战2019年浙江新高考化学考点【全国百强校】吉林省延边第二中学2018-2019学年高一下学期期中考试化学试题【全国百强校】内蒙古北方重工业集团有限公司第三中学2018-2019学年高一下学期期中考试化学试题吉林省白山市第七中学2018-2019学年高一下学期期中考试化学试题【校级联考】浙江省台州市联谊五校2018-2019学年高一下学期期中考试化学试题安徽省亳州市涡阳县第一中学2018-2019学年高一下学期第二次质量检测化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高一下学期期中考试化学试题(宾县用卷)云南省峨山彝族自治县第一中学2018-2019学年高一6月月考化学试题吉林省吉林市第三中学2018-2019学年高一5月阶段测试化学试题江西省南昌市八一中学、洪都中学、麻丘高中等七校2018-2019学年高一下学期期末考试化学试题云南省昆明市官渡区第一中学2018-2019学年高一下学期期中考试化学试题黑龙江省哈尔滨尚志中学2018-2019学年高一下学期期中考试化学试题黑龙江省鹤岗市第一中学2018-2019学年高一下学期期末化学试题甘肃省兰州市第一中学2018-2019学年高一下学期期末考试化学试题新疆自治区阿克苏地区沙雅县第二中学2018-2019学年高一下学期期中考试化学试题河南省洛阳市栾川县实验高中2019-2020学年高二9月月考化学试题江西省南昌市八一中学、洪都中学、十七中三校2019-2020学年高二10月联考化学试题江西省南昌市进贤县第一中学2019-2020学年高二上学期期中考试化学试题辽宁省沈阳市城郊市重点联合体2019-2020学年高一上学期第二次月考化学试题(已下线)【新东方】高中化学5029山西省朔州市怀仁一中2019-2020学年高二上学期第四次月考化学试题甘肃省天水市甘谷第一中学2020届高三上学期第四次检测考试化学试题浙江省丽水四校联考2019-2020学年高一11月月考化学试题人教版高中化学必修2第二章《化学反应与能量》测试卷3贵州省岑巩县第四中学2019-2020学年高二上学期期末考试化学试题(已下线)【新东方】2020-42020届高三化学知识点强化训练—化学影像速率的图象分析山西省忻州市第一中学2019-2020学年高一下学期(远程)目标检测(6)化学试题(已下线)【新东方】高中化学X006浙江省湖州中学2019-2020学年高一下学期3月月考(普通班)化学试题课时1 化学能转化为电能——A学习区 夯实基础(苏教版必修2)(已下线)【南昌新东方】2019 八一中学、洪都中学、麻丘高中等七校 高一下 期末(已下线)【南昌新东方】2019 进贤一中 高二上 第一次月考(已下线)【南昌新东方】2019 新建一中 高一下期中(已下线)【南昌新东方】2019 进贤一中 高二上 期中山东省烟台市第二中学2019-2020学年高一下学期4月月考化学试题湖南省邵东县第一中学2019-2020学年高二下学期第一次月考化学试题辽宁省庄河市高级中学2019-2020学年高一下学期5月网考化学试题山东省烟台市第三中学2019-2020学年高一下学期4月月考化学试题(已下线)专题6.2 原电池 化学电源(讲)——2020年高考化学一轮复习讲练测(已下线)【南昌新东方】2019-2020 南昌三中 高一下 第一次月考山西省朔州市怀仁县怀仁一中云东校区2019-2020学年高一下学期期中考试化学试题广西壮族自治区钦州市第一中学2019-2020学年高一下学期期中考试理科综合化学试题山西省朔州市应县第一中学校2019-2020学年高一下学期期中考试化学试题黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题黑龙江省伊春市伊美区第二中学2019-2020学年高二上学期开学考试化学试题天津市第一中学2018-2019学年高一下学期期中考试化学试题(已下线)1.2.1 原电池的工作原理 练习《新教材同步备课》(鲁科版选择性必修1)山东省临沂第一中学2019-2020学年高一下学期期中考试化学试题河北省秦皇岛市卢龙县中学2019-2020学年高一下学期第二次调研考试化学试题河北省衡水市阜城中学2020-2021学年高二上学期开学考试化学试题(已下线)2.2 影响化学反应速率的因素(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)高一必修第二册(人教2019版)第六章 化学反应与能量 素养检测鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 章末综合检测卷山东省新泰市第一中学北校2020-2021学年高二上学期第一次月考化学试题(已下线)【全国百强校】云南省曲靖市第一中学2018-2019学年高一5月月考化学试题(已下线)第20讲 原电池 化学电源(精讲)——2021年高考化学一轮复习讲练测黑龙江省大庆市东风中学2020-2021学年高二上学期10月月考化学试题福建省福州市八县(市)一中2020-2021学年高二上学期期中联考化学试题(已下线)第四章 化学反应与电能(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)(已下线)专题4.1 原电池-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)重庆市渝西中学2020-2021学年高二上学期第一次月考化学试题(已下线)【浙江新东方】绍兴qw105(已下线)练习13 原电池-2020-2021学年【补习教材·寒假作业】高二化学(人教版)(已下线)第四章 电化学基础(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)辽宁省大连市普兰店第二中学2020-2021学年高二上学期期中考试化学试题福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题陕西省宝鸡市金台区2020-2021学年高二上学期期末考试化学(理)试题(已下线)4.1 原电池(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)浙江省绍兴市2020-2021学年高一上学期期末调测化学试题人教版2019必修第二册 第六章 本章达标检测(人教版2019)必修第二册 第六章 化学反应与能量 第一节 化学反应与能量变化贵州省黔西南州兴义市第二高级中学2019-2020学年高一下学期期末考试化学试题(已下线)【绍兴新东方】绍兴高中化学00015浙江省精诚联盟2020-2021学年高一3月联考化学试题(已下线)【浙江新东方】双师159高一下甘肃省兰州市第二十七中学2020-2021学年高二上期末考试化学试题江苏省宿迁市沭阳县潼阳中学2020-2021学年高二下学期第一次月考化学试题(已下线)【浙江新东方】双师215高一下(已下线)【浙江新东方】双师177高一下内蒙古通辽市科尔沁区大林高中2020-2021学年高二4月月考化学试题新疆昌吉教育共同体2020-2021学年高一下学期期中考试化学试题山东省临沂市临沂第二十四中学2020-2021学年高一下学期期中考试化学试题贵州省铜仁市思南中学2020-2021学年高一下学期期中考试化学试题(已下线)【浙江新东方】高中化学20210513-027【2021】【高一下】四川省犍为外国语实验学校2020-2021学年高一下学期期中考试化学试题广东省珠海市第二中学2020-2021学年高一下学期期中考试化学试题湖北省汉川实验高中2020-2021学年高一下学期期中考试化学试题(已下线)【浙江新东方】在线化学100高一下南昌市新建一中2020-2021学年高一下学期期中考试化学试题浙江省义亭中学2017-2018学年高一下学期期中考试化学试题山东省德州市实验中学2020-2021学年高一下学期期中考试化学试题内蒙古包头市第六中学2020-2021学年高一下学期期中考试化学试题黑龙江省宾县第二中学2020-2021学年高一下学期第二次月考化学试题辽宁省恒仁满族自治县第二高级中学2020-2021学年高二上学期期末考试化学试题(已下线)专题06 化学反应速率和限度【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)云南省楚雄天人中学2020-2021学年高二上学期12月月考化学试题(苏教版2019)必修第二册专题6 化学反应与能量变化 第三单元 化学能与电能的转化 课时1 化学能转化为电能山西省吕梁市2020-2021学年高一下学期期末考试化学试题吉林省辽源市友好学校2020-2021学年高一下学期期末联考化学试题(已下线)专题2.1.2 影响化学反应速率的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)安徽省六安市新安中学2020-2021学年高一下学期期末考试化学试题内蒙古集宁新世纪中学2020-2021学年高一下学期期末考试化学试题(已下线)第14讲 原电池-2020-2021学年秋季班高一上学期化学教材知识点精讲练(沪科版)辽宁省庄河市高级中学2021-2022学年高二上学期开学考试化学试题河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷安徽省泗县第一中学2021-2022学年高二上学期第二次月考化学试题浙江省宁波市六校2020-2021学年高二上学期期中联考化学试题广东省广州市第八十九中学2021-2022学年高一上学期期中考试化学试题安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题(已下线)第13讲 化学反应速率(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)浙江省台州市书生中学2021-2022学年高一下学期阶段性测试(3月)化学试题江西省宜春市上高二中2021-2022学年高一下学期第六次月考试题(3月)化学试题黑龙江省绥化市第一中学2021-2022学年高二上学期期末考试化学试题河北省武安市第一中学2020-2021学年高一下学期第二次月考化学试卷题上海市南洋模范中学2021-2022学年高一下学期3月考化学试题上海市南洋模范中学2021-2022学年高一下学期3月月考化学试题河南省焦作市武陟县第一中学东校区2021-2022学年高一下学期4月月考化学试题 山东省烟台市第二中学2021-2022学年高一下学期4月月考化学试题(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)广东省潮州市潮安区宝山中学2021-2022学年高一下学期期中考试化学试题黑龙江省大庆实验中学2021-2022学年高一下学期期中考试化学试题河南省濮阳市范县第一中学2021-2022学年高一下学期期中检测化学试题广东珠海市斗门第一中学2021-2022学年高一下学期期中考试化学试题黑龙江省双鸭山市集贤县2021-2022学年高一下学期期中考试化学试题(已下线)【期末复习】必刷题(2)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)河南省安阳市中原名校2021-2022学年高一下学期第三次联考化学试题山东省泰安市第一中学2021-2022学年高一下学期期中考试(等级考)化学试题北京市顺义牛栏山第一中学2021-2022学年高一下学期居家学习成果展示化学测试题广东省汕头市潮阳林百欣中学2021-2022学年高一下学期 期中考试化学试题河北省新乐市第一中学2021-2022学年高一上学期第一次月考化学试题湖南省怀化市沅陵县第一中学2021-2022学年高一下学期第一次月考化学试题广西龙胜各族自治县龙胜中学2021-2022学年高一下学期期中考试化学试题山东省聊城市颐中外国语学校2021-2022学年高一下学期期中考试化学试题河北省邢台市隆尧县唐尧中学2021-2022学年高二上学期第三次月考化学试卷福建省平潭翰英中学2021-2022学年高二上学期期中考试化学试题(已下线)6.1.2 化学反应与电能——同步学习必备知识吉林省长春市实验中学2022-2023学年高二上学期期末考试化学试题广东省广州市天河区第八十九中学2022~2023学年高一下学期期中考试化学选考试题辽宁省六校协作体2022-2023学年高一下学期期中考试化学试题6.3.1化学能转化为电能(课后)-2019苏教版必修2课前课中课后河南省信阳市2022~2023学年高一下学期期中考试化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期5月期中考试化学试题吉林省延边第二中学2022-2023学年高一下学期5月期中考试化学试题江西省九江市彭泽县第二高级中学2022-2023学年高一下学期7月期末化学试题作业(四) 原电池的工作原理黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题陕西省商洛市洛南中学2022-2023学年高一下学期4月期中考试化学试题安徽省滁州市定远县育才学校2023-2024学年高二上学期期末化学模拟试卷福建省龙岩市连城县第一中学2023-2024学年高一下学期4月月考化学试题河北省唐山市开滦第二中学2023-2024学年高一下学期4月月考化学试题陕西省西安市5校联考2023-2024学年高二上学期1月期末化学试题
名校
解题方法
4 . 某无色溶液中,可大量共存的离子组是
A.Na+、HCO 、SO 、SO 、Br- 、Br- | B.Cu2+、NO 、Cl-、SO 、Cl-、SO |
C.H+、Cl-、K+、CO | D.K+、Mg2+、SO 、OH- 、OH- |
您最近一年使用:0次
2022-12-06更新
|
64次组卷
|
14卷引用:甘肃省甘南藏族自治州合作第一中学2021-2022学年高一上学期期末考试化学试题
甘肃省甘南藏族自治州合作第一中学2021-2022学年高一上学期期末考试化学试题云南省漾濞二中2019-2020学年高二上学期开学考试化学试题山东省济宁市鱼台县第一中学2019-2020学年高一上学期第一次月考(9月)化学试题山东省章丘市第一中学2020-2021学年高一10月月考化学试题吉林省汪清县第六中学2020-2021学年高一上学期期中考试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高一上学期第三次月考化学试题福建省长泰县第一中学2021届高三上学期11月考试化学试题云南省弥勒市第一中学黄冈校区2020-2021学年高一12月月考化学试题新疆维吾尔自治区呼图壁县第一中学2020-2021学年高一下学期期初考试化学试题西藏拉萨市第二高级中学2021-2022学年高一上学期期中考试化学试题陕西省安康市汉阴中学2021-2022学年高一上学期期中考试化学试题(已下线)陕西省西安市铁一中学2023-2024学年高一上学期第一次月考化学试题湖南省洞口县第九中学2023-2024学年高一上学期第一次月考化学试题广东省茂名市信宜市2023-2024学年高一上学期11月期中考试化学试题
10-11高一上·黑龙江大庆·期中
5 . 有一种气体的质量是14.2g,体积是4.48升(标准状况下),该气体的摩尔质量是
| A.28.4 | B. | C.71 | D.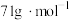 |
您最近一年使用:0次
2022-11-21更新
|
1155次组卷
|
100卷引用:甘肃省卓尼县柳林中学2018-2019学年高一上学期第一次月考化学试题
甘肃省卓尼县柳林中学2018-2019学年高一上学期第一次月考化学试题(已下线)2010年黑龙江大庆实验中学高一上学期期中考试化学试卷(已下线)2010—2011学年广东省梅州市曾宪梓中学高一上学期期末考试化学试卷(已下线)2011—2012学年河北省南宫中学高一期中考试化学试卷(已下线)2011-2012学年北京市重点中学高二上学期期中考试化学(文)试卷(已下线)2011-2012年湖南岳阳等四县一中高二第六次质检化学试卷(已下线)2012-2013学年福建晋江养正中学高一上学期期中考试化学试卷2015-2016学年内蒙古巴彦淖尔高一上10月月考化学试卷2015-2016学年重庆市杨家坪中学高一上学期第一次月考化学试卷2015-2016学年湖南衡阳第八中学高一上六科联赛化学卷2015-2016学年吉林省吉林五十五中高一上学期期中测试化学试卷2015-2016学年湖南省衡阳一中高一上学期期中测试化学试卷2016-2017学年宁夏吴忠中学高二上学期开学考试化学试卷2016-2017学年甘肃省武威二中高一上10月月考化学试卷2016-2017学年安徽马鞍山二中高一10月阶段测化学卷2016-2017学年贵州省遵义市第四中学高一上学期期中考试化学试卷2016-2017学年广东省普宁市华侨中学高一上月考二化学卷四川省邻水实验学校2017-2018学年高一上学期第一次月考化学试题甘肃省武威市第六中学2017-2018学年高一上学期第一次学段考试化学试题江西省崇义中学2017-2018学年高一上学期第一次月考化学试题河北省唐山市第一中学2017-2018学年高一上学期第一次月考(十月)化学试题河南省张家口市涿鹿中学2017-2018学年高一10月化学试题甘肃省武威第十八中学2017-2018学年高一上学期第一次月考化学试题江西省九江市2017-2018学年高一上学期第一次阶段联考化学试题广西河池市高级中学2017-2018学年高一上学期第一次月考化学试题吉黑两省九校2017-2018学年高一上学期期中考试化学试题辽宁省辽河油田第二高级中学2017-2018学年高一上学期第一次月考化学试题河北省辛集中学2017-2018学年高一10月月考化学试卷湖南省衡阳市26中2017-2018学年高一上期期中考试化学试题新疆维吾尔自治区阿克苏市农一师高级中学2017-2018学年高一第二次月考化学试卷内蒙古杭锦后旗奋斗中学2017-2018学年高一上学期第二次月考化学试题陕西省榆林市第二中学2017-2018学年高一上学期期中考试化学试题广西陆川县中学2017-2018学年高一12月月考化学试题青海省西宁二十一中2017-2018学年高一上学期12月月考化学试题黑龙江省大庆中学2017-2018学年高一上学期期末化学试题陕西省延安市实验中学大学区校际联盟2017-2018学年高一上学期期末考试(B)化学试题高中化学《气体的摩尔体积》专项训练题山西省朔州市应县第一中学2018-2019学年高一上学期第一次月考(9月)化学试题【全国百强校】四川省成都市双流区棠湖中学2018-2019学年高一上学期第一次月考化学试题陕西省铜川市煤炭建设公司第一中学2018-2019学年高一上学期10月月考化学试题【全国百强校】河北省辛集市辛集中学2018-2019学年高一上学期第一次月考化学试题2018-2019学年苏教版高中化学必修一 专题综合测评1安徽省合肥市第九中学2018-2019学年高一上学期第一次月考化学试题湖北省武汉市钢城四中2018-2019学年高一上学期10月月考化学试题新疆自治区北京大学附属中学新疆分校2018-2019学年高一上学期10月月考化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高一上学期10月月考化学试题河南省安阳市第三十六中学2018-2019学年高一上学期第一次月考化学试题西藏自治区日喀则市南木林高级中学2018-2019学年高一上学期期中考试化学试题江西省会昌中学2018-2019学年高一上学期第一次10月月考化学试题步步为赢 初高中衔接教材化学暑假作业:第20课时 理想气体状态方程和阿伏加德罗定律河北省大名县第一中学2019-2020学年高一10月月考化学试题河北省辛集中学2019-2020学年高一上学期第一次月考(理)化学试题甘肃省武威第十八中学2019-2020学年高一上学期第一次月考化学试题河北省邢台市第八中学2019-2020学年高一上学期期中考试化学试题宁夏回族自治区石嘴山市平罗中学2019-2020学年高一上学期期中考试化学试题宁夏青铜峡市高级中学2019-2020学年高一上学期期中考试化学试题四川省宜宾市第三中学校2019-2020学年高一上学期10月月考化学试题黑龙江省大庆市第十中学2019-2020学年高一上学期10月月考化学试题(已下线)【新东方】2019新中心五地087高中化学甘肃省兰州市联片办学2019-2020学年高一上学期期末考试化学试题甘肃省庆阳市宁县第二中学2019-2020学年高一上学期第一次月考化学试题甘肃省天水市2019-2020学年高一上学期期末考试化学试题吉林省长春市九台区第四中学2019-2020高一上学期期末测试化学试题(已下线)【南昌新东方】江西省九江市2017-2018学年高一上学期第一次阶段联考化学试题广东省江门市第二中学2019-2020学年高一上学期第二次考试(期中)化学试题苏教版(2020)高一必修第一册专题1第二单元 课时2 气体摩尔体积人教版(2019)高一必修第一册 第二章 第三节课时2 气体摩尔体积鲁科版(2019)高一必修第一册第1章 认识化学科学 第3节 物质的量 课时2 气体摩尔体积陕西省咸阳市永寿县中学2020-2021学年高二上学期第一次月考化学试题陕西省咸阳市永寿县中学2020-2021学年高一上学期第一次月考化学试题甘肃省庆阳市宁县第二中学2020-2021学年高一上学期第一次月考化学试题广东省东莞市粤华学校2019-2020学年高一上学期10月月考化学试题云南保山市第九中学2020-2021学年高一上学期第三次月考化学试题甘肃省武威第十八中学2020-2021学年高一上学期期中考试化学试题内蒙古乌兰察布市化德一中2020-2021学年高一上学期期中考试化学试题西藏昌都第四高级中学2020-2021学年高一上学期期中考试化学试题江西省贵溪市实验中学2020-2021学年高一上学期12月月考化学试题(已下线)【浙江新东方】绍兴qw73安徽省六安市舒城育才学校2020-2021学年高一12月月考化学试题河南省汤阴县五一中学2019-2020学年高一下学期期中考试化学试题辽宁省大连市普兰店区第一中学2020-2021学年高一上学期第二阶段考试化学试题宁夏银川唐徕回民中学2021-2022学年高一10月月考化学试题青海省西宁市北外附属新华联国际学校2021-2022学年高一上学期第一次月考化学试题青海省西宁市海湖中学2021-2022学年高一上学期第一次月考化学试题安徽省芜湖市2021-2022学年高一上学期期末教学质量监控化学试题(已下线)2.3.2 气体摩尔体积-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)山西省灵丘县第四中学校2021-2022学年高一上学期期中考试化学试题甘肃省庆阳市第六中学2021-2022学年高一上学期期中考试化学试题甘肃省定西市临洮县文峰中学2021-2022学年高一上学期期中考试化学试题江苏省高邮市第一中学2022-2023学年高一上学期期初考试化学试题陕西省渭南高级中学2021-2022学年高一上学期第一次月考化学试题山东省新泰市第一中学2022—2023学年高一上学期期中考试化学试题陕西省宜君县高级中学2021-2022学年高一上学期第一次月考化学试题山东省济南市天桥区黄河双语实验学校2021-2022学年高一上学期期中考试化学试题广西南宁市第五十六中学2021-2022学年高一上学期期中考试化学试题(已下线)第04讲 气体摩尔体积-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)河北省张家口市宣化第一中学2022-2023学年高一上学期12月月考化学试题(已下线)期中测试卷一【测试范围:第一、二章】-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)(已下线)【精品卷】2.3.2 气体摩尔体积课堂例题-人教版2023-2024学年必修第一册广西浦北中学2023-2024学年高一上学期10月月考化学试题
6 . 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS____ 0,该反应自发进行的条件是____ (填“低温”“高温”或“任意温度”)。
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为____ kJ。
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH____ ΔH3(填“>”“<”“=”)。
(4)根据盖斯定律计算反应②的ΔH2=____ kJ•mol-1,上述①②③反应中符合如图能量变化的是____ (填序号)。
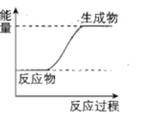
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH
(4)根据盖斯定律计算反应②的ΔH2=

您最近一年使用:0次
7 . 回答下列问题:
(1)在25℃、101kPa下,1gCH4燃烧生成CO2和液态水时放热56kJ。表示甲烷燃烧热的热化学方程式为____ 。
(2)在一定条件下N2与H2反应生成NH3,已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、945.7kJ,则N2与H2反应生成NH3的热化学方程式为:____ 。
(3)书写电离方程式:NaHCO3____ 。
H2O____ 。
NH3•H2O____ 。
(1)在25℃、101kPa下,1gCH4燃烧生成CO2和液态水时放热56kJ。表示甲烷燃烧热的热化学方程式为
(2)在一定条件下N2与H2反应生成NH3,已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、945.7kJ,则N2与H2反应生成NH3的热化学方程式为:
(3)书写电离方程式:NaHCO3
H2O
NH3•H2O
您最近一年使用:0次
解题方法
8 . 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验,请完成下列填空:
(1)配制100mL0.1000mol·L-1NaOH标准溶液,配制过程中选用的玻璃仪器主要有烧杯、玻璃棒、量筒、胶头滴管和____ 。
配制好标准液后进行滴定,滴定操作步骤:
①准备:检漏→洗涤→装液→排气泡→读数,其中洗涤先用水洗后____ 。
②滴定:用酸式滴定管取25.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用标准NaOH溶液进行滴定,重复上述滴定操作2-3次。
(2)从图中读出NaOH标准液终点滴定管的读数____ mL。
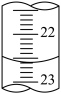
(3)滴定达到终点的标志是____ 。
(4)排去碱式滴定管中气泡的方法应采用操作____ ,然后挤压玻璃球使尖嘴部分充满碱液。
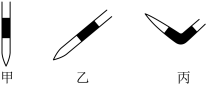
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有____ 。
(1)配制100mL0.1000mol·L-1NaOH标准溶液,配制过程中选用的玻璃仪器主要有烧杯、玻璃棒、量筒、胶头滴管和
配制好标准液后进行滴定,滴定操作步骤:
①准备:检漏→洗涤→装液→排气泡→读数,其中洗涤先用水洗后
②滴定:用酸式滴定管取25.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用标准NaOH溶液进行滴定,重复上述滴定操作2-3次。
(2)从图中读出NaOH标准液终点滴定管的读数

(3)滴定达到终点的标志是
(4)排去碱式滴定管中气泡的方法应采用操作

(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有
| A.碱式滴定管尖嘴部分有气泡,滴定后消失 |
| B.滴定终点读数时仰视读数 |
| C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗 |
| D.锥形瓶水洗后未干燥 |
您最近一年使用:0次
2022-09-21更新
|
108次组卷
|
2卷引用:甘肃省甘南藏族自治州舟曲县第一中学2021-2022学年高二上学期期中考试化学试题
解题方法
9 . I.高炉炼铁过程中发生的主要反应为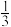 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如表:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如表:
请回答下列问题:
(1)该反应的平衡常数表达式K=_____ ,△H____ 0(填“>”、“<”或“=”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各1.0mol,反应经过10min后达到平衡。求该时间范围内CO的平衡转化率=____ 。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是____ 。
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
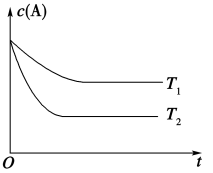
II.A(g) B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1。温度T1和T2下A的浓度与时间关系如图所示。
B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1。温度T1和T2下A的浓度与时间关系如图所示。
回答下列问题:
(4)温度:T1_____ T2(填“大于”“小于”或“等于”,下同),平衡常数:K(T1)_____ K(T2)。
(5)若温度为T2时,5min后反应达到平衡,A的转化率为50%,则:
①平衡时体系总的物质的量为____ 。
②该温度下,反应的平衡常数K=____ 。
③0~5min用A浓度的变化表示反应速率v(A)=_____ 。
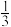 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如表:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如表:| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各1.0mol,反应经过10min后达到平衡。求该时间范围内CO的平衡转化率=
(3)欲提高(2)中CO的平衡转化率,可采取的措施是
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
II.A(g)
 B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1。温度T1和T2下A的浓度与时间关系如图所示。
B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1。温度T1和T2下A的浓度与时间关系如图所示。
回答下列问题:
(4)温度:T1
(5)若温度为T2时,5min后反应达到平衡,A的转化率为50%,则:
①平衡时体系总的物质的量为
②该温度下,反应的平衡常数K=
③0~5min用A浓度的变化表示反应速率v(A)=
您最近一年使用:0次
名校
解题方法
10 . 民以食为天,食品的种类越来越丰富,我国90%以上的食品中含有添加剂。
(1)下列做法会导致食品对人体有害的是_______。
①在沥青公路上翻晒粮食
②火腿中加过量亚硝酸钠可调味、增色和防腐
③用无烟煤直接烧烤鸡、鸭
④用“瘦肉精”(一种含激素的饲料)喂养生猪
⑤用小苏打作发酵粉制作面包
⑥用乙烯催熟水果
(2)卫生部印发首批非法食品添加剂名单。下列在食物中的添加剂(括号内物质)不属于非法食品添加剂的是_______。
(3)下列食品添加剂与其作用叙述错误的是_______。
(4)人的血液呈_______ (填“酸性”“弱酸性”“中性”“碱性”或“弱碱性”),我国居民形成了摄入蔬菜和水果偏少的饮食习惯,一般尿液偏_______ 性。
(1)下列做法会导致食品对人体有害的是_______。
①在沥青公路上翻晒粮食
②火腿中加过量亚硝酸钠可调味、增色和防腐
③用无烟煤直接烧烤鸡、鸭
④用“瘦肉精”(一种含激素的饲料)喂养生猪
⑤用小苏打作发酵粉制作面包
⑥用乙烯催熟水果
| A.①②③④ | B.①②③⑤⑥ | C.②③④⑤ | D.①②③④⑤ |
| A.海参(甲醛) | B.白酒(甲醇) | C.奶粉(三聚氰胺) | D.食盐(KIO3) |
| A.维生素C在食品中的作用是增加食物的营养及防止食物氧化变质 |
| B.在食品中适量增加胡萝卜素可以改善食品的外观 |
| C.在食品中加入亚硝酸钠可以代替食盐以调节食物的咸味 |
| D.在制作膨化食品时可以用洗衣粉作食品膨化剂 |
您最近一年使用:0次