1 . 某小组在实验室中模拟侯氏制碱法制备NaHCO3,并探究钠及其常见化合物的相关性质和应用,实验流程如图所示:
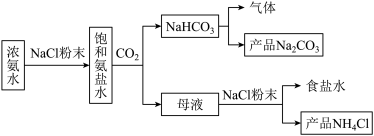
(1)写出由浓氨水生成NaHCO3的总反应的离子方程式:______ 。
(2)侯氏制碱法中NH3和CO2的通入顺序为先通入______ (填化学式,下同),后通入_____ 。
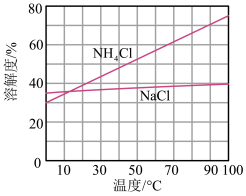
(3)向母液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程,为了充分析出并分离出NH4Cl,根据如图中物质溶解度曲线知,需采取的操作为_____ 、过滤、洗涤、干燥。
(4)NaHCO3长期放置在空气中会变质(部分转变为Na2CO3),现欲测定某NaHCO3样品中NaHCO3的质量分数,设计如下实验方案(假设产生的气体全部与Na2O2反应):
i.取一定质量的样品加水溶解后与如图所示的硫酸VmL恰好反应。
ii.将i中产生的气体用浓硫酸干燥后缓慢地通入足量的Na2O2粉末中充分反应,Na2O2粉末增重mg
①图中硫酸的物质的量浓度是______ 。
②标准状况下i中产生气体的体积为______ L(用含m的代数式表示)。样品中小苏打的物质的量是______ mol(用含m、V的代数式表示)。

(1)写出由浓氨水生成NaHCO3的总反应的离子方程式:
(2)侯氏制碱法中NH3和CO2的通入顺序为先通入
(3)向母液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程,为了充分析出并分离出NH4Cl,根据如图中物质溶解度曲线知,需采取的操作为

(4)NaHCO3长期放置在空气中会变质(部分转变为Na2CO3),现欲测定某NaHCO3样品中NaHCO3的质量分数,设计如下实验方案(假设产生的气体全部与Na2O2反应):
i.取一定质量的样品加水溶解后与如图所示的硫酸VmL恰好反应。
ii.将i中产生的气体用浓硫酸干燥后缓慢地通入足量的Na2O2粉末中充分反应,Na2O2粉末增重mg
| 名称:硫酸 分子式:H2SO4 密度:1.84 g·cm-3 质量分数:98% |
②标准状况下i中产生气体的体积为
您最近一年使用:0次
解题方法
2 . Ⅰ以下是实验室及生活中常见的一些物质:①液氯、②稀H2SO4、③CO2、④石灰水、⑤氯水、⑥氢氧化钠溶液、⑦CaO、⑧酒精、⑨Cu,请根据要求填空:
(1)属于酸性氧化物的是______ ;属于电解质的是________ 。(填序号)
(2)②在水中的电离方程式为_________ 。
(3)写出①与⑥溶液反应的离子方程式:______ 。
Ⅱ、过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验,请回答以下问题:
(4)纯净的Na2O2是________ 色固体,其中氧元素的化合价为_________ 价。
该实验小组为了粗略测定过氧化钠的质量分数,称取了20.0 g样品,并设计用如图装置通过排水法测定E中收集到的O2的体积,来测定过氧化钠的质量分数。
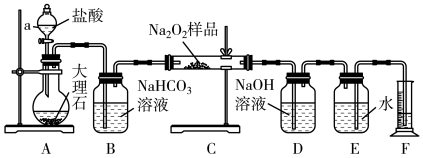
(5)将仪器连接好以后、加药品之前必须进行的一步操作_____ ,A中主要反应的离子方程式:_____ ;
(6)装置B的作用是除去二氧化碳气体中的______ 气体,写出相应的化学方程式_____ 。读出量筒内水的体积后,将其折算成标准状况下氧气的体积为2.24L,则样品中过氧化钠的质量分数为_____ 。
(1)属于酸性氧化物的是
(2)②在水中的电离方程式为
(3)写出①与⑥溶液反应的离子方程式:
Ⅱ、过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验,请回答以下问题:
(4)纯净的Na2O2是
该实验小组为了粗略测定过氧化钠的质量分数,称取了20.0 g样品,并设计用如图装置通过排水法测定E中收集到的O2的体积,来测定过氧化钠的质量分数。

(5)将仪器连接好以后、加药品之前必须进行的一步操作
(6)装置B的作用是除去二氧化碳气体中的
您最近一年使用:0次
解题方法
3 . 下列方案设计、现象和结论不正确 的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究样品中是否含有Na元素 | 用玻璃棒蘸取样品进行焰色试验 | 若火焰呈黄色,则该样品中含有Na元素 |
| B | 探究Fe2+、Br−的还原性强弱 | 向FeBr2溶液中加入少量氯水,再加CCl4萃取 | 若CCl4层无色,则Fe2+的还原性强于Br− |
| C | 检验铁粉是否变质 | 取少量铁粉溶于稀盐酸中,滴加KSCN溶液 | 若溶液未变红色,无法说明铁粉是否变质 |
| D | 确认二氯甲烷分子不存在同分异构体 | 先搭建甲烷分子球棍模型,后用2个氯原子取代任意2个氢原子,重复数次,观察所得球棍模型的结构 | 若所得球棍模型均代表相同物质,则确认二氯甲烷分子不存在同分异构体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-15更新
|
310次组卷
|
2卷引用: 浙江省丽水、湖州、衢州 2022 年 11 月三地市高三教学质量检测(一模)化学试题
4 . 下列实验方案中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 比较CH3COOH和HClO的酸性 | 用pH试纸测定同浓度的两溶液的pH值 |
| B | 检验Fe(NO3)2晶体是否变质 | 将样品溶于稀硫酸,滴入几滴KSCN溶液 |
| C | 除去乙酸乙酯中的少量乙酸 | 加入过量饱和Na2CO3溶液洗涤后分液 |
| D | 除去乙烯中少量的二氧化硫 | 将混合气体通过足量酸性KMnO4溶液洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验 溶液中 溶液中 是否被氧化 是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 | 若溶液呈红色,则说明有 被氧化 被氧化 |
| B | 探究干燥 是否具有漂白性 是否具有漂白性 | 将鲜花投入盛有干燥氯气的集气瓶中 | 鲜花褪色,说明干燥氯气具有漂白性 |
| C | 探究碳酸钠样品是否变质为 | 在稀盐酸中加入少量可能变质的碳酸钠样品 | 立即有气体产生,则说明 已经变质,有一部分转化为 已经变质,有一部分转化为 |
| D | 探究钠是否变质 | 将表面已经变质的钠投入水中 | 产生无色无味的气体,则说明钠已经变质,有一部分被氧化为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-12更新
|
425次组卷
|
2卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
名校
解题方法
6 . 下列方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 检验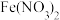 晶体是否已氧化变质 晶体是否已氧化变质 | 将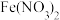 样品溶于稀硫酸后,滴加KSCN溶液, 样品溶于稀硫酸后,滴加KSCN溶液, | 溶液变红,说明已氧化变质 |
| B | 鉴定某涂改液中是否存在含氯化合物 | 取涂改液与KOH溶液混合充分反应,取上层清液,硝酸酸化,加入硝酸银溶液 | 出现白色沉淀,说明涂改液中存在含氯化合物 |
| C | 检验苯中的苯酚 | 取少量样品,加入适量的浓溴水 | 若未出现白色沉淀,说明苯中不存在苯酚 |
| D | 探究B、C、S三种元素的非金属性 | 分别向饱和 溶液和稀硫酸溶液中加入少量 溶液和稀硫酸溶液中加入少量 粉末 粉末 | 前者无气泡冒出,后者有气泡冒出,说明非金属性:S>C>B |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-16更新
|
261次组卷
|
3卷引用:山东省淄博市2022-2023学年高三上学期12月月考化学试题
名校
解题方法
7 . 下列实验操作、现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeCl3溶液中滴加淀粉KI溶液 | 溶液变成蓝色 | 氧化性:I2 > FeCl3 |
| B | 向硫酸铜溶液中加入小颗粒钠 | 产生红色固体 | 钠比铜活泼 |
| C | 向硫酸亚铁溶液中加入过氧化钠粉末 | 产生红褐色沉淀 | FeSO4已变质 |
| D | 向烧碱样品中滴加氯化钡溶液 | 产生白色沉淀 | 烧碱已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-05更新
|
92次组卷
|
2卷引用:内蒙古集宁一中2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 根据下列实验操作和实验现象,得出的实验结论正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 常温下,分别测定0.01mol/L的NaHSO3溶液和0.01mol/L的NaHCO3溶液的pH值 | NaHCO3的pH值大 | 非金属性:S>C |
| B | 向某钠盐中滴加稀盐酸,将产生的无色气体通入品红溶液 | 品红溶液褪色 | 该钠盐可能为Na2S2O3 |
| C | 将 样品溶于稀硫酸,滴加KSCN溶液 样品溶于稀硫酸,滴加KSCN溶液 | 溶液变红 |  样品已变质 样品已变质 |
| D | 向盛有过量AgNO3溶液的试管中滴加少量NaCl溶液,再向其中滴加Na2CrO4溶液 | 先观察到白色沉淀,后产生砖红色沉淀 | AgCl沉淀可转化为更难溶的沉淀Ag2CrO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-26更新
|
268次组卷
|
2卷引用:重庆南开中学2022-2023学年高二上学期线上教学质量诊断考试化学试题
名校
解题方法
9 . 铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)有“中华第一剑”之称的虢国玉柄铁剑是我国目前出土的最早冶炼铁,玉柄铁剑,剑断锈连,剑身表面的铁锈的主要成分是___ (填标号)。
(2)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是___ (用离子方程式表示)。
(3)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液 溶液I
溶液I 沉淀II
沉淀II Fe2O3
Fe2O3
①H2O2溶液的作用是___ 。
②“溶液I”的溶质为___ (填化学式),写出由“溶液I”到“沉淀II”反应的离子方程式:___ 。
③“操作III”的名称为___ 。
(4)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:__ (填标号);重复上述操作步骤,直至装置A恒重,记为m3g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=___ (列出计算式即可)。
(1)有“中华第一剑”之称的虢国玉柄铁剑是我国目前出土的最早冶炼铁,玉柄铁剑,剑断锈连,剑身表面的铁锈的主要成分是
| A.Fe | B.FeO | C.Fe3O4 | D.Fe2O3 |
(3)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液
 溶液I
溶液I 沉淀II
沉淀II Fe2O3
Fe2O3①H2O2溶液的作用是
②“溶液I”的溶质为
③“操作III”的名称为
(4)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=
您最近一年使用:0次
2021-12-17更新
|
564次组卷
|
4卷引用:第三章 铁 金属材料(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)河北省保定市唐县第一中学2022-2023学年高一上学期第三次考试化学试题河北省定州市第二中学2022-2023学年高一上学期12月月考化学试题河北省百所学校大联考2021-2022学年高一12月联考化学试题
解题方法
10 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验麦芽糖水解产物 | 在麦芽糖溶液中加入麦芽糖酶,反应一段时间后,再加入适量新制Cu(OH)2悬浊液加热 | 出现砖红色沉淀说明麦芽糖水解产物中含葡萄糖 |
| B | 检验脱氧剂中还原铁粉是否变质 | 取少量样品溶于盐酸,再滴加KSCN溶液 | 溶液未变红,说明铁粉未变质 |
| C | 检验石蜡油分解产物 | 将碎瓷片催化石蜡油分解产生的气体通入酸性高锌酸钾溶液中 | 酸性高锌酸钾溶液褪色证明石蜡油分解产生的气体是乙烯 |
| D | 比较AlO 、CO 、CO 得到质子的能力 得到质子的能力 | 将NaAlO2溶液与NaHCO3溶液混合 | 出现白色沉淀,证明AlO 得到质子的能力强于CO 得到质子的能力强于CO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



