解题方法
1 . A、B、C、D.E五种元素中,A、B、C、D为原子序数依次增大的短周期主族元素,A的电子层数等于其最外层电子数且在同周期中A的原子半径最小, B、C、D元素的常见单质均为气体,其中B、C的单质是空气的主要成分,D与其他元素不在同一周期,E为常见使用量最大的金属。在一定条件下,A的单质可以分别与C、D的单质化合生成甲、乙。各物质间有如图转化关系,回答下列问题:
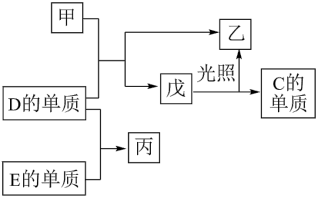
(1)D在元素周期表中的位置为_______ 。
(2)写出B的单质的电子式:_______ 。
(3)戊的分子中D元素的化合价为_______ 。写出戊在光照条件下发生反应的化学方程式:_______ 。
(4)A、B、C三种元素的原子半径从大到小的顺序为_______ (用元素符号表示)。
(5)钠在C的气体中燃烧可以生成淡黄色固体,该物质中阳离子与阴离子的个数比为_______

(1)D在元素周期表中的位置为
(2)写出B的单质的电子式:
(3)戊的分子中D元素的化合价为
(4)A、B、C三种元素的原子半径从大到小的顺序为
(5)钠在C的气体中燃烧可以生成淡黄色固体,该物质中阳离子与阴离子的个数比为
您最近一年使用:0次
2 . 短周期元素a、b、c、d在元素周期表中的相对位置如图所示,其中d在同周期中原子半径最小。回答下列问题:
(1)属于碱金属元素的有___ (填元素符号)。
(2)d在元素周期表中的位置是___ 。
(3)写出由a、b形成的既含极性键又含非极性键的化合物的电子式:___ 。
(4)如图表示某些物质之间的转化关系,其中化合物A是由c、d两种元素组成的二元化合物,L为b的一种单质;常温下M为深红棕色液体,Q可用来检验淀粉的存在。
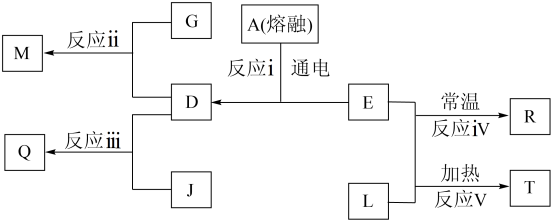
①化合物A在熔融时的电离方程式是___ 。
②反应ⅱ、反应ⅲ说明元素非金属性的强弱关系是___ (用元素符号表示)。
③写出T与水反应的离子方程式:___ 。
| a | |||||
| …… | b | ||||
| c | d | ||||
(2)d在元素周期表中的位置是
(3)写出由a、b形成的既含极性键又含非极性键的化合物的电子式:
(4)如图表示某些物质之间的转化关系,其中化合物A是由c、d两种元素组成的二元化合物,L为b的一种单质;常温下M为深红棕色液体,Q可用来检验淀粉的存在。

①化合物A在熔融时的电离方程式是
②反应ⅱ、反应ⅲ说明元素非金属性的强弱关系是
③写出T与水反应的离子方程式:
您最近一年使用:0次
名校
解题方法
3 . A、B、C、D、E是原子序数依次增大并分属四个周期的前20号主族元素。B、C相邻且C原子的最外层电子数是内层电子数的3倍,D、E能形成化合物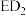 。
。
(1)B在元素周期表中的位置是___________ ,化合物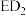 的电子式为
的电子式为___________ 。
(2)A与B、C形成的简单化合物的稳定性相对强弱为___________ (用化学式表示);化合物 中的化学键类型为
中的化学键类型为___________ 。
(3)科学研究发现化合物BC具有“扩张血管和增强免疫力、记忆力”的功能,故它成为当前生命科学研究中的“明星分子”。一定条件下该“明星分子”可转化为化合物B,C与另一种常见的红棕色气体,写出反应的化学方程式:___________ ,同温同体积条件下,该反应完全转化后,容器内反应前后的压强比为___________ 。
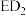 。
。(1)B在元素周期表中的位置是
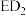 的电子式为
的电子式为(2)A与B、C形成的简单化合物的稳定性相对强弱为
 中的化学键类型为
中的化学键类型为(3)科学研究发现化合物BC具有“扩张血管和增强免疫力、记忆力”的功能,故它成为当前生命科学研究中的“明星分子”。一定条件下该“明星分子”可转化为化合物B,C与另一种常见的红棕色气体,写出反应的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 元素周期表的学习对我们学习化学具有重要的指导意义,如表是元素周期表的一部分,请根据要求回答问题:
(1)⑥表示的元素是 _______ (填元素符号);
(2)⑤元素在周期表中的位置是_______ ;②和⑤两种元素非金属性强弱关系:②___ ⑤(填“>”或“<”)
(3)写出④最高价氧化物水化物的化学式_______ ;
(4)③形成的简单离子符号是_______ ,请写出51号元素在元素周期表中的位置 _______ 。
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | C | ② | ③ | Ne | ||||
| 3 | ④ | Mg | ⑤ | ⑥ |
(2)⑤元素在周期表中的位置是
(3)写出④最高价氧化物水化物的化学式
(4)③形成的简单离子符号是
您最近一年使用:0次
21-22高一上·全国·课前预习
解题方法
5 . 门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下了空位。例如:他认为铝的下方有一个与铝类似的元素“类铝”,并预测了它的性质。1875年,法国化学家布瓦博德朗发现了这种元素,将它命名为“镓”,镓的性质与门捷列夫预测的一样。门捷列夫还预测在硅和锡之间存在一种元素“类硅”,15年后该元素被德国化学家文克勒发现,为了纪念他的祖国,将其命名为“锗”。
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据_____ ?元素周期表中元素的位置和性质之间存在着怎样的内在联系_____ ?
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据
您最近一年使用:0次
解题方法
6 . 下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题
(1)上述元素中,金属性最强的是_______ (填元素名称),最高价氧化物对应水化物酸性最强的是_______ (写出酸的化学式)。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:_______ 。(用离子符号表示)
(3)由元素①和④形成的18电子的结构式为_______ ;由元素①、③、⑨形成的离子化合物的电子式为_______ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程_______ 。
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为:_______
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系_______ 。
(6)可以比较⑤、⑥两元素金属性强弱的实验是_______。
(7)元素③、磷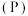 、砷
、砷 、锑
、锑 、铋
、铋 为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置_______ 。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | ⑩ | |||||||
(1)上述元素中,金属性最强的是
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:
(3)由元素①和④形成的18电子的结构式为
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为:
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系
(6)可以比较⑤、⑥两元素金属性强弱的实验是_______。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
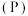 、砷
、砷 、锑
、锑 、铋
、铋 为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
您最近一年使用:0次
解题方法
7 . 元素周期表体现了元素位-构-性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
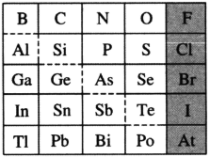
(1)元素Po在元素周期表中的位置为第_______ 周期_______ 族。
(2)Br的最高价氧化物对应水化物的化学式为_______ ,Ge的最高价氧化物为_______ 。
(3) 、
、 的酸性强弱:
的酸性强弱:
_______ 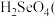 (填“>”“<”或“=”,下同)。氢化物的还原性:
(填“>”“<”或“=”,下同)。氢化物的还原性:
_______  。
。
(4)可在图中分界线(虚线部分)附近寻找_______(填字母)。
(5)某小组同学向浓硝酸中加入少量碳粉,无明显现象,缓慢加热,发现碳粉逐渐溶解,产生红棕色气体,试写出上述反应的化学方程式:_______ ,在该反应中硝酸体现的性质为_______ 。

(1)元素Po在元素周期表中的位置为第
(2)Br的最高价氧化物对应水化物的化学式为
(3)
 、
、 的酸性强弱:
的酸性强弱:
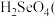 (填“>”“<”或“=”,下同)。氢化物的还原性:
(填“>”“<”或“=”,下同)。氢化物的还原性:
 。
。(4)可在图中分界线(虚线部分)附近寻找_______(填字母)。
| A.优良的催化剂 | B.半导体材料 | C.合金材料 | D.农药 |
您最近一年使用:0次
8 . 元素周期表的建立和元素周期律的发现,揭示了元素“位”“构”“性”之间的内在联系,可以根据“位”“构”的特点预测和解释元素的性质。下图是元素周期表的一部分,请回答下列问题:
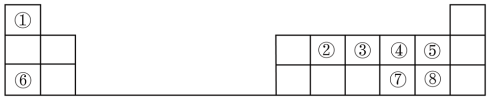
(1)元素⑦在周期表中的位置是
(2)元素③、④的原子半径大小关系正确的是
(3)元素④、⑦的非金属性强弱关系正确的是
(4)元素①、⑧形成化合物的电子式正确的是
(5)元素②有多种同位素,这些同位素具有相同的
(6)下列各组元素形成的化合物中只含有离子键的是

(1)元素⑦在周期表中的位置是
| A.第二周期、第ⅣA族 | B.第二周期、第ⅥA族 |
| C.第三周期、第ⅣA族 | D.第三周期、第ⅥA族 |
| A.③>④ | B.③<④ | C.③=④ | D.无法确定 |
| A.④>⑦ | B.④<⑦ | C.④=⑦ | D.无法确定 |
| A.HCl | B.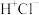 | C.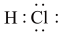 | D.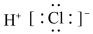 |
| A.质量数和电子数 | B.质子数和电子数 |
| C.质子数和中子数 | D.质量数和中子数 |
| A.①和④ | B.②和④ | C.①和⑤ | D.⑥和⑧ |
您最近一年使用:0次
9 . 元素周期表体现了元素的“位一构—性”的关系,揭示了元素间的内在联系。下表列出部分元素在周期表中的位置。请回答下列问题。
(1)元素①④⑨形成的化合物中含有的化学键有 ___________ 。
(2)元素②③最高价氧化物对应水化物的酸性较强的是___________ (填化学式, 下同)。
(3)元素⑤⑧氢化物的稳定性较大的是___________ 。
(4)元素⑥⑦最高价氧化物对应的水化物之间发生反应的离子方程式为___________ 。
(5)如果发现119号元素,它应该位于周期表的位置为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ |
(2)元素②③最高价氧化物对应水化物的酸性较强的是
(3)元素⑤⑧氢化物的稳定性较大的是
(4)元素⑥⑦最高价氧化物对应的水化物之间发生反应的离子方程式为
(5)如果发现119号元素,它应该位于周期表的位置为
您最近一年使用:0次
10 . 根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A是1~36号元素原子核外电子排布中未成对电子数最多的元素,A元素的名称是______ ,在元素周期表中的位置是_______ 。
(2)B元素基态原子的轨道表示式是下图中的________ (填序号),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合_______ (填序号)。
①
②
A.能量最低原则 B.泡利不相容原理 C.洪特规则
(3)下图表示8种短周期元素的原子序数(图中原子序数是连续的)和元素常见单质沸点的关系。其中第一电离能和电负性最大的元素分别是______ 、_______ (填序号);C、D、F元素的简单离子的半径由大到小的顺序是______ (用离子符号表示)。
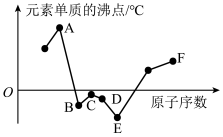
(1)A是1~36号元素原子核外电子排布中未成对电子数最多的元素,A元素的名称是
(2)B元素基态原子的轨道表示式是下图中的
①

②

A.能量最低原则 B.泡利不相容原理 C.洪特规则
(3)下图表示8种短周期元素的原子序数(图中原子序数是连续的)和元素常见单质沸点的关系。其中第一电离能和电负性最大的元素分别是

您最近一年使用:0次



