1 . 化合物A中含有三种元素,3.68gA在氧气中充分煅烧后生成1.28gB、1.60gC和气体D,物质A~H存在如图转化关系。
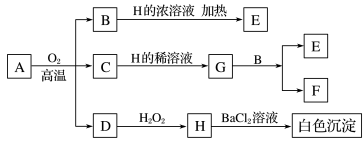
已知B是一种红色金属单质,C是金属氧化物,D是非金属氧化物,E、F、G是盐。请回答:
(1)化合物A中非金属元素在元素周期表中的位置为:___ ;
(2)检验气体D的实验方法:___ ;
(3)写出B与H的浓溶液反应的化学方程式:___ ;
(4)写出A在氧气中充分煅烧的化学方程式:___ 。

已知B是一种红色金属单质,C是金属氧化物,D是非金属氧化物,E、F、G是盐。请回答:
(1)化合物A中非金属元素在元素周期表中的位置为:
(2)检验气体D的实验方法:
(3)写出B与H的浓溶液反应的化学方程式:
(4)写出A在氧气中充分煅烧的化学方程式:
您最近一年使用:0次
2 . 下列说法正确的是( )
A.单质 氧化物 氧化物 酸或碱 酸或碱 盐,硅单质可以按上述关系进行转化 盐,硅单质可以按上述关系进行转化 |
B.若a、b、c分别为Si、SiO2、H2SiO3,则可以通过一步反应实现如图所示的转化 |
| C.太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 |
| D.单质硅常用于制造光导纤维 |
您最近一年使用:0次
2019-01-02更新
|
85次组卷
|
2卷引用:广东省佛山市萌茵实验学校2020-2021学年高一下学期第一次月考化学试题
解题方法
3 . 下表是元素周期表的一部分。
回答问题:
(1)门捷列夫科学地预言了“类铝”元素Ga, Ga在元素周期表中的位置是第_______ 周期、第_______ 族。
(2)第三周期主族元素中,金属性最强的元素原子结构示意图为_______ 。
(3)碳元素的一种放射性核素 C可用于文物年代的测定,
C可用于文物年代的测定, C 的原子核内中子数为
C 的原子核内中子数为_______ 。
(4)某研究小组探究氯与溴非金属性的强弱关系,过程如下:
[预测]非金属性: Cl>Br。
[设计与实验]如图所示,在点滴板的2个孔穴中分别滴入3滴新制氯水,然后向其中之一滴加3滴NaBr溶液。

[证据与分析]滴加NaBr溶液的孔穴中,溶液颜色变深,说明有Br2生成。
[结论]预测_______ (选项“正确”或“不正确”)。
[解释]从原子结构的角度解释为_______ 。
族 周期 | I A | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | C | ||||||
| 3 | Na | Mg | Al | Si | P | S | Cl |
| 4 | Ga | Br |
回答问题:
(1)门捷列夫科学地预言了“类铝”元素Ga, Ga在元素周期表中的位置是第
(2)第三周期主族元素中,金属性最强的元素原子结构示意图为
(3)碳元素的一种放射性核素
 C可用于文物年代的测定,
C可用于文物年代的测定, C 的原子核内中子数为
C 的原子核内中子数为(4)某研究小组探究氯与溴非金属性的强弱关系,过程如下:
[预测]非金属性: Cl>Br。
[设计与实验]如图所示,在点滴板的2个孔穴中分别滴入3滴新制氯水,然后向其中之一滴加3滴NaBr溶液。

[证据与分析]滴加NaBr溶液的孔穴中,溶液颜色变深,说明有Br2生成。
[结论]预测
[解释]从原子结构的角度解释为
您最近一年使用:0次
21-22高一上·全国·课前预习
解题方法
4 . 门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下了空位。例如:他认为铝的下方有一个与铝类似的元素“类铝”,并预测了它的性质。1875年,法国化学家布瓦博德朗发现了这种元素,将它命名为“镓”,镓的性质与门捷列夫预测的一样。门捷列夫还预测在硅和锡之间存在一种元素“类硅”,15年后该元素被德国化学家文克勒发现,为了纪念他的祖国,将其命名为“锗”。
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据_____ ?元素周期表中元素的位置和性质之间存在着怎样的内在联系_____ ?
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
5 . 元素的“位、构、性”是指元素在周期表中的位置、元素原子的核外电子排布与元素性质的关系。下列有关说法正确的是
| A.元素周期表中同一个“格”内只表示一种原子 |
| B.原子最外层电子数为1的元素的最高价氧化物对应的水化物为碱 |
| C.F、Cl、Br得电子能力和氢化物的稳定性均依次减弱 |
| D.非金属都集中在元素周期表的右上角 |
您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、Q、W、R是常见的短周期主族元素,其相关信息如下表:
(1)元素X在元素周期表中的位置是___________ 。
(2)上述六种元素中有2种元素能形成一种淡黄色的固体化合物,该化合物的电子式是___________ , 所含化学键的类型有___________ 。
(3)Y、Q、R三种元素的简单氢化物中,稳定性最强的化合物的结构式为___________ 。
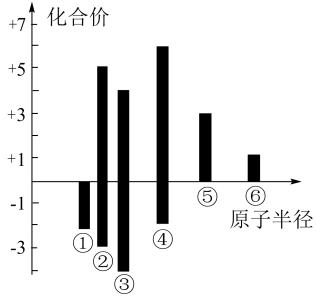
(4)上述六种元素原子半径与主要化合价的关系如图,其中④对应的元素为___________ (填名称)。
(5)将RQ2通入BaCl2溶液中,没有明显变化,再向其中加入Z的最高价氧化物的水化物,可观察到的现象是___________ ,发生反应的离子方程式是___________ 。
| 元素 | 相关信息 |
| X | 它的一种同位素被用作相对原子质量的标准 |
| Y | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Z | 是短周期中(除稀有气体外)原子半径最大的元素 |
| Q | 最外层电子数是次外层电子数的3倍 |
| W | 原子序数等于X、Y原子序数之和 |
| R | 与Q同族,且最高价氧化物的水化物的浓溶液常温下使W单质钝化 |
(2)上述六种元素中有2种元素能形成一种淡黄色的固体化合物,该化合物的电子式是
(3)Y、Q、R三种元素的简单氢化物中,稳定性最强的化合物的结构式为
(4)上述六种元素原子半径与主要化合价的关系如图,其中④对应的元素为

(5)将RQ2通入BaCl2溶液中,没有明显变化,再向其中加入Z的最高价氧化物的水化物,可观察到的现象是
您最近一年使用:0次
名校
7 . 元素周期表体现了元素“位—构—性”的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
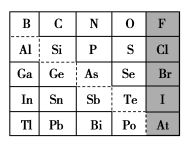
(1)元素Ga在元素周期表中的位置为:第___________ 周期第___________ 族;
(2)Sn的最高正价为___________ ,Bi的最高价氧化物为___________ ;
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是___________ 元素(填元素符号);
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___________ (填“>”“<”或“=”)H2SeO4;
③氢化物的还原性:H2O___________ (填“>”“<”或“=”)H2S;

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次
名校
8 . 元素周期表揭示了元素之间的内在联系,使元素构成了一个较为系统的体系.请回答下列问题:
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的_______ 。按照元素在周期表中的顺序给元素编号,得到原子序数。人们发现原子序数与元素的原子结构之间存在如下关系:原子序数=_______ =核外电子数
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。
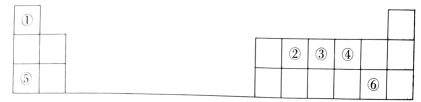
(1)②、③、④三种元素中,原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)①、④、⑤三种元素形成的化合物的电子式为_______ ,该化合物中化学键的类型有_______ 。
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:_______ 。根据元素周期律推测,下列性质中Q不可能具有的是_______ (填选项字母)。
A.最高正化合价为 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。

(1)②、③、④三种元素中,原子半径由大到小的顺序为
(2)①、④、⑤三种元素形成的化合物的电子式为
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:
A.最高正化合价为
 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
您最近一年使用:0次
2021-01-28更新
|
172次组卷
|
2卷引用:山西省2020-2021学年高一上学期期末考试化学试题
9 . Ⅰ. 元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。
(1)元素X在周期表中的位置是第_______ 周期,第_______ 族。
(2)五种元素中离子半径最小的是_______ 。
Ⅱ. 下图是部分短周期主族元素原子半径与原子序数的关系。

(3)X的元素符号:_______ 。
(4)Y与Z形成的是_______ 化合物。(填“离子”或“共价”)
(5)上述元素的最高价含氧酸中酸性最强的是_______ (填化学式)。
Ⅲ.(6)下列关于元素及其化合物性质的判断中,正确的是_______ (填序号)
A. 元素甲的氢氧化物只有碱性,而元素乙的氢氧化物具有两性,所以金属性:甲>乙
B. 元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
C. 金属元素 、
、 能分别形成+2、+3价离子,所以氧化性:
能分别形成+2、+3价离子,所以氧化性: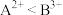
D. 因为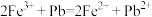 ,所以金属性:
,所以金属性:
E. 因为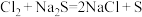 ,所以非金属性:
,所以非金属性:
F. 因为水溶液的酸性: ,所以非金属性:
,所以非金属性:
G. 是一元酸,而
是一元酸,而 是二元酸,所以酸性:
是二元酸,所以酸性: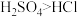
Ⅳ.(7)甲同学查阅资料知:氨气( )的分解温度在850℃以上,甲烷(
)的分解温度在850℃以上,甲烷( )的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
)的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):_______ 。
| X | Y | ||||
| Z | W | Q |
(2)五种元素中离子半径最小的是
Ⅱ. 下图是部分短周期主族元素原子半径与原子序数的关系。

(3)X的元素符号:
(4)Y与Z形成的是
(5)上述元素的最高价含氧酸中酸性最强的是
Ⅲ.(6)下列关于元素及其化合物性质的判断中,正确的是
A. 元素甲的氢氧化物只有碱性,而元素乙的氢氧化物具有两性,所以金属性:甲>乙
B. 元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
C. 金属元素
 、
、 能分别形成+2、+3价离子,所以氧化性:
能分别形成+2、+3价离子,所以氧化性: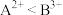
D. 因为
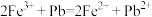 ,所以金属性:
,所以金属性:
E. 因为
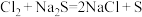 ,所以非金属性:
,所以非金属性:
F. 因为水溶液的酸性:
 ,所以非金属性:
,所以非金属性:
G.
 是一元酸,而
是一元酸,而 是二元酸,所以酸性:
是二元酸,所以酸性: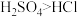
Ⅳ.(7)甲同学查阅资料知:氨气(
 )的分解温度在850℃以上,甲烷(
)的分解温度在850℃以上,甲烷( )的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
)的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
您最近一年使用:0次
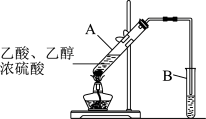
10 . 根据如图,已知有机物A,B,C,D,E,F有以下转化关系。A是分子量为28的气体烯烃,其产量是衡量一个国家石油化工生产水平的标志;D是食醋的主要成分,E是不溶于水且具有香味的无色液体,相对分子质量是C的2倍,F是一种高分子化合物。结合如图关系回答问题:

(1)B中官能团名称___ 、C的结构简式为___ 。
(2)①的化学方程式为___ ;该反应类型是___ 。F是常见的高分子材料,合成F的化学方程式是___ 。
(3)根据如图,实验室用该装置制备E,试管A中浓硫酸的作用是___ ;B中的试剂是___ ;B中导管的位置在液面上方,目的是:___ 。

(1)B中官能团名称
(2)①的化学方程式为
(3)根据如图,实验室用该装置制备E,试管A中浓硫酸的作用是

您最近一年使用:0次



