名校
解题方法
1 . 已知A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。甲、乙、丙三种化合物的分子中含有相同数目的电子;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,化合物丁与C的某种单质在常温下反应可生成红棕色气体;B、C、D三种元素的单质与甲、乙、丁三种化合物之间存在如图所示的转化关系(反应条件已略去):

(1)D在元素周期表中的位置为________________ 。
(2)B、C、D的原子半径的大小关系为________ (用元素符号表示)。
(3)丁与C的单质在常温下反应的化学方程式为______________ 。
(4)甲、乙、丙分子中的电子数均为________ ,实验室如何检验丙_______ 。
(5)C的单质+丙→乙+丁的化学方程式为_______________ 。

(1)D在元素周期表中的位置为
(2)B、C、D的原子半径的大小关系为
(3)丁与C的单质在常温下反应的化学方程式为
(4)甲、乙、丙分子中的电子数均为
(5)C的单质+丙→乙+丁的化学方程式为
您最近一年使用:0次
名校
解题方法
2 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
(1)A在元素周期表中的位置为___________ ,画出基态B原子的轨道表示式___________ 。
(2)B的简单气态氢化物的沸点___________ (填“高于”或“低于”)PH3,原因是___________ 。
(3)A、B、C三种元素的电负性由高到低的排列次序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 链状分子中所有的原子都满足8电子稳定结构,则其分子中
链状分子中所有的原子都满足8电子稳定结构,则其分子中 键与
键与 键数目之比为
键数目之比为___________ 。
(5)G元素可形成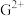 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(6)短周期元素 与元素
与元素 在周期表中的位置呈现对角线关系,已知元素
在周期表中的位置呈现对角线关系,已知元素 、
、 的电负性分别为1.5和3.0,预测它们形成的化合物是
的电负性分别为1.5和3.0,预测它们形成的化合物是___________ (填“离子”或“共价”)化合物。推测 的最高价氧化物对应的水化物
的最高价氧化物对应的水化物___________ (填“能”或“不能”)与 的最高价氧化物对应水化物发生反应。
的最高价氧化物对应水化物发生反应。
| A | 原子核外有6个电子 |
| B | 原子序数比 大1 大1 |
| C | 基态原子中 电子总数与p电子总数相等 电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子价层电子排布式为3s23p1 |
| F | 基态原子的最外层p 轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属,其高价氯化物的盐溶液常用于刻蚀铜制印刷电路板 |
(2)B的简单气态氢化物的沸点
(3)A、B、C三种元素的电负性由高到低的排列次序为
(4)已知元素A、B形成的
 链状分子中所有的原子都满足8电子稳定结构,则其分子中
链状分子中所有的原子都满足8电子稳定结构,则其分子中 键与
键与 键数目之比为
键数目之比为(5)G元素可形成
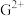 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(6)短周期元素
 与元素
与元素 在周期表中的位置呈现对角线关系,已知元素
在周期表中的位置呈现对角线关系,已知元素 、
、 的电负性分别为1.5和3.0,预测它们形成的化合物是
的电负性分别为1.5和3.0,预测它们形成的化合物是 的最高价氧化物对应的水化物
的最高价氧化物对应的水化物 的最高价氧化物对应水化物发生反应。
的最高价氧化物对应水化物发生反应。
您最近一年使用:0次
2022-07-25更新
|
981次组卷
|
3卷引用:宁夏石嘴山市第三中学2023-2024学年高二下学期3月月考化学试题
13-14高三下·重庆·阶段练习
名校
3 . 甲、乙、丙、丁为中学常见物质,其中甲、乙为单质,丙为氧化物,它们之间存在如图所示的转化关系:
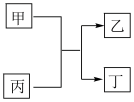
下列说法正确的是( )

下列说法正确的是( )
| A.若甲、乙元素是同主族元素,根据元素周期表推测,此时乙单质可能是Si |
| B.若甲、乙均为金属单质,则丁所属的物质类别一定是碱性氧化物 |
| C.若甲为金属单质,乙为非金属单质,则甲只能是Mg |
| D.若甲、乙元素是同周期元素,则该反应的化学方程式一定为:2F2 + 2H2O=4HF + O2 |
您最近一年使用:0次
2019-03-09更新
|
2262次组卷
|
8卷引用:宁夏石嘴山市第三中学2019-2020学年高二上学期期末考试化学试题
14-15高三上·广西桂林·阶段练习
解题方法
4 . 已知 +HCN→
+HCN→
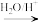
 ,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:
,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:

(1)A、E的结构简式分别为:_______ 、_______ ;
(2)B→C、E→F的反应类型分别为:_______ 、_______ ;
(3)写出下列转化的化学方程式:C→D_______ ;G+F→H_______ ;
(4)要检验B中的Br元素,可用的操作和现象为_______ 。
(5)写出符合下列要求的H的同分异构体①有一个支链②能使溴的四氯化碳溶液褪色③跟NaHCO3反应生成CO2_______ ,_______ 。(只要求写出2个)
 +HCN→
+HCN→
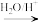
 ,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:
,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:
(1)A、E的结构简式分别为:
(2)B→C、E→F的反应类型分别为:
(3)写出下列转化的化学方程式:C→D
(4)要检验B中的Br元素,可用的操作和现象为
(5)写出符合下列要求的H的同分异构体①有一个支链②能使溴的四氯化碳溶液褪色③跟NaHCO3反应生成CO2
您最近一年使用:0次
名校
5 . 碳和氧元素及其化合物与人类的生产、生活密切相关。
I.氯的化合物合成、转化一直是科学研究的热点。
(1)一定条件下,氯气与氨气反应可以制备气态氯胺(NH2Cl),已知部分化学键的键能:
则上述反应的热化学方程式为:__________________ 。
(2)氯胺是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为_____________ 。
II.碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。
(3)在三个容积均为1L的密闭容器中以不同的氢碳比 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
请回答下列问题:
①反应的△H______ 0,氢碳比α____ β,Q点v(正)_____ v(逆)(填“>”或“<”、“=”)
②若起始时,CO2的浓度分别为0.5mol/L,则P点对应温度度的平衡常数的值为________ 。
(4)已知:碳酸 H2CO3: K1=4.3×10-7、K2=5.6×10-11;
草酸 H2C2O4: K1=6.0×10-2、K2=6.0×10-5
①下列微粒可以大量共存的是_______ (填字母)。
a.CO32-、HC2O4-b.H2CO3、C2O42-c. C2O42-、HCO3-d.H2C2O4、HCO3-
②若将等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子(除OH-外)浓度由大到小的顺序是_________ 。
I.氯的化合物合成、转化一直是科学研究的热点。
(1)一定条件下,氯气与氨气反应可以制备气态氯胺(NH2Cl),已知部分化学键的键能:
| 化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
| 键能/KJ•mol-1 | 391.3 | 243.0 | 191.2 | 431.8 |
则上述反应的热化学方程式为:
(2)氯胺是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为
II.碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。
(3)在三个容积均为1L的密闭容器中以不同的氢碳比
 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。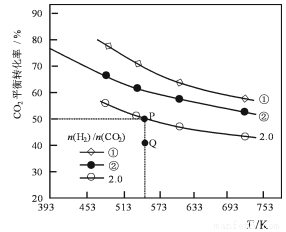
请回答下列问题:
①反应的△H
②若起始时,CO2的浓度分别为0.5mol/L,则P点对应温度度的平衡常数的值为
(4)已知:碳酸 H2CO3: K1=4.3×10-7、K2=5.6×10-11;
草酸 H2C2O4: K1=6.0×10-2、K2=6.0×10-5
①下列微粒可以大量共存的是
a.CO32-、HC2O4-b.H2CO3、C2O42-c. C2O42-、HCO3-d.H2C2O4、HCO3-
②若将等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子(除OH-外)浓度由大到小的顺序是
您最近一年使用:0次



