解题方法
1 . 电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成.下列装置是用燃烧法确定有机物分子式常用的装置.
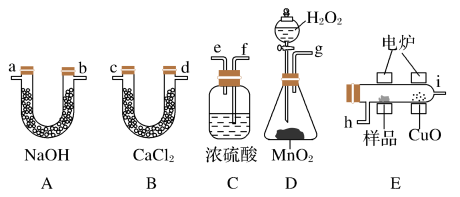
(1)产生的O2按从左到右的流向,所选各装置的正确连接顺序是
_________ →_______ →________ →_______ →________ .
(2)燃烧管中CuO的作用是_________ ,如果去掉CuO,则A管的质量会________ (填增大、减小或不变)
(3)请改进这套装置的一个不足之处____________________
(4)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为__________ .
(5)用质谱仪测定其相对分子质量,得如图1所示的质谱图,则该有机物的相对分子质量为________ .
(6)该物质的核磁共振氢谱如图2所示,则其结构简式为________ .



(1)产生的O2按从左到右的流向,所选各装置的正确连接顺序是
(2)燃烧管中CuO的作用是
(3)请改进这套装置的一个不足之处
(4)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为
(5)用质谱仪测定其相对分子质量,得如图1所示的质谱图,则该有机物的相对分子质量为
(6)该物质的核磁共振氢谱如图2所示,则其结构简式为


您最近一年使用:0次
2 . 化学反应原理在工业生产中具有十分重要的意义。
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:
(2)已知反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
①该反应的化学平衡常数K的表达式为____________ ,a________ 0(填“>”、“<”或“=”)。在500 ℃ 2 L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5 min后达到平衡时CO2的转化率为________ ,生成CO的平均速率v(CO)为_______________ 。
②700 ℃反应达到平衡后,要使反应速率增大且平衡向右移动, 可采取的措施有___________ 。
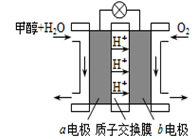
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式_____________________ ,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH=_________ (溶液电解前后体积的变化忽略不计)。
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为
(2)已知反应Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:| 温度(℃) | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
①该反应的化学平衡常数K的表达式为
②700 ℃反应达到平衡后,要使反应速率增大且平衡向右移动, 可采取的措施有
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式

您最近一年使用:0次
2016-12-09更新
|
683次组卷
|
4卷引用:2016届辽宁省大石桥市第二高级中学高三上期末化学试卷
名校
3 . 前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A 元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是__________ (填元素符号,下同),电负性最大的是_________ 。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式___________ ,1 mol AB-中含有π键的数目为__________ ,黄血盐晶体中各种微粒间的作用力不涉及__________ (填选项字母)。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为_____________ ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③ 、④HCHO。其中碳原子采取sp2杂化的分子有
、④HCHO。其中碳原子采取sp2杂化的分子有___________ (填物质序号),HCHO分子的立体结构为______________ 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)__________________ 。
(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为_____________ 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加德罗常数的值为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为______________ cm。

(1)六种元素中第一电离能最小的是
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为
 、④HCHO。其中碳原子采取sp2杂化的分子有
、④HCHO。其中碳原子采取sp2杂化的分子有(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为

您最近一年使用:0次
2016-12-09更新
|
690次组卷
|
9卷引用:2016届辽宁省大石桥市第二高级中学高三上期末化学试卷
11-12高一上·新疆乌鲁木齐·期末
名校
4 . 为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:
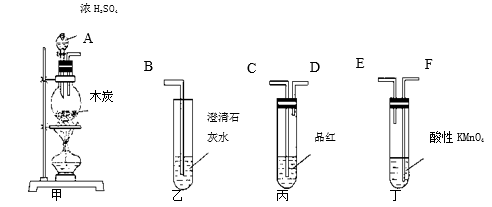
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):_____ 接________ ,_____ 接_____ ,____ 接____ ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中_______ ,丙中_______ ;
(3)丁中酸性KMnO4溶液的作用是_________ ;
(4)写出甲中反应的化学方程式________ 。

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中
(3)丁中酸性KMnO4溶液的作用是
(4)写出甲中反应的化学方程式
您最近一年使用:0次
2016-12-09更新
|
1433次组卷
|
20卷引用:辽宁省营口市第二高级中学2019-2020学年高一下学期期末考试化学(理)试题
辽宁省营口市第二高级中学2019-2020学年高一下学期期末考试化学(理)试题(已下线)2010—2011学年新疆乌鲁木齐市第八中学高一上学期期末考试化学试卷(已下线)2010—2011学年黑龙江七校高一期末联考化学试卷(已下线)2011-2012学年福建省五校高一上学期期末联考化学试卷(已下线)2013-2014广东省梅州市重点中学高一下学期期中化学试卷(已下线)2013-2014甘肃省肃南县第一中学高一下学期期末考试化学试卷(已下线)2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷2014-2015海南省海南中学高一上学期期末化学试卷2014-2015学年内蒙古霍林郭勒市第三中学高一下期中考试化学试卷2018年高一化学(人教版)必修1综合题型练习卷:非金属及其化合物(已下线)2018年12月11日 《每日一题》人教必修1-浓硫酸的特性吉林省辉南县第一中学2018-2019学年高一下学期第一次月考化学试题新疆石河子第二中学2018-2019学年高一上学期期末考试化学试题广东第二师范学院番禺附属中学2019-2020学年高二上学期中考试化学(学考)试题(已下线)2019年12月10日 《每日一题》化学人教版(必修1)——浓硫酸的特性辽宁省锦州市黑山县黑山中学2019-2020学年高一6月质量检测化学试题吉林省乾安县第七中学2020-2021学年高一下学期第五次质量检测化学试题(已下线)5.1.2 硫酸、含硫化合物的相互转化——同步学习必备知识吉林省舒兰市第十八中学校2021-2022学年高一下学期期末考试化学试题海南省琼海市嘉积中学2023-2024学年高一年级下学期第一次月考化学试题B卷



