名校
1 . 25 °C时,1L 0.1mol·L-1的某二元酸H2RO3溶液中各含R物种的pc-pOH关系如图所示。图中pc表示各含R物种的浓度负对数[pc=-lgc,pOH= -lgc(OH)]。下列说法正确的是
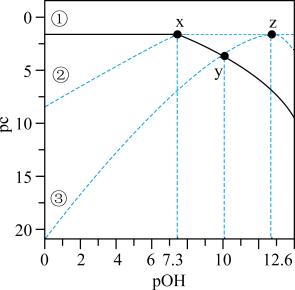

A.曲线③表示pc(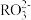 )随pOH的变化 )随pOH的变化 |
B.y点的溶液中:c(H2RO3)+2c(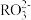 )=0.1mol·L-1 )=0.1mol·L-1 |
| C.H2RO3的Ka1=1.0×10-6.7 |
D.2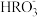  H2RO3+ H2RO3+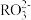 的平衡常数K=1.0×10-5.3 的平衡常数K=1.0×10-5.3 |
您最近一年使用:0次
2023-05-21更新
|
1035次组卷
|
4卷引用:辽宁省实验中学2023-2024学年高二上学期期中阶段测试化学试题
辽宁省实验中学2023-2024学年高二上学期期中阶段测试化学试题安徽省马鞍山市2023届高三下学期第三次教学质量监测理科综合化学试题(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)
名校
解题方法
2 . 如图所示,实验室中利用洁净的铜片(0.3 mol)和浓硫酸进行反应,实验中无气体生成,Y型管左侧得到Cu2S和白色固体a,倾斜Y型管使左侧的物质全部转移到右侧稀硝酸中,反应生成固体单质b、a的溶液和NO。下列说法错误的是
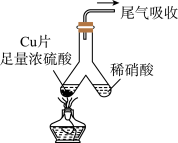

| A.白色固体为CuSO4 |
| B.NO为还原产物,b为氧化产物 |
| C.NO与b的物质的量之和可能为0.2 mol |
| D.参加反应的浓硫酸中,表现氧化性的占25% |
您最近一年使用:0次
2023-05-16更新
|
1272次组卷
|
3卷引用:辽宁省实验中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
3 . 溶液X中含有下表离子中的某5种,且其浓度均为 (不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是
(不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是
 (不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是
(不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是阳离子 | 阴离子 |
|
|
| A.X溶液中可能含3种阳离子、2种阴离子 | B.X溶液中不可能含有 或 或 |
C.生成的无色气体是 | D.根据电荷守恒,原溶液中一定含 |
您最近一年使用:0次
2023-04-20更新
|
1309次组卷
|
9卷引用:辽宁省沈阳市铁路实验中学2022-2023学年高一下学期第一次月考化学试题
辽宁省沈阳市铁路实验中学2022-2023学年高一下学期第一次月考化学试题辽宁省大连市金普新区省示范性高中2022届高三上学期第一次联合考试化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一下学期3月阶段反馈化学试题上海市育才中学2022-2023学年高三上学期10月月考化学试题黑龙江省鹤岗市绥滨县第一中学2021-2022学年高三上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题黑龙江省哈尔滨师范大学附属中学2024届高三上学期开学考试化学试题河北省秦皇岛市昌黎第一中学2023届高三第一次调研考试化学试题河北省石家庄市第二中学2023-2024高一上学期第一次诊断测评化学试题
名校
解题方法
4 . 把NaOH、 、
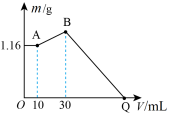
、 三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/L HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如下图所示。下列说法错误的是
三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/L HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如下图所示。下列说法错误的是
 、
、 三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/L HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如下图所示。下列说法错误的是
三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/L HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如下图所示。下列说法错误的是
| A.三种固体溶于足量水反应后有NaOH剩余 |
B.B点的沉淀物为 和 和 |
| C.原混合物中NaOH的质量是5.20g |
| D.Q点HCl溶液加入量是120mL |
您最近一年使用:0次
2023-01-04更新
|
1405次组卷
|
2卷引用:辽宁省沈阳市第一二0中学2022-2023学年高一上学期期末考试化学试题
5 . 已知图甲为金属钠的晶胞,晶胞边长为 ,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为
,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为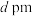 。下列关于ZnS晶胞的描述错误的是
。下列关于ZnS晶胞的描述错误的是
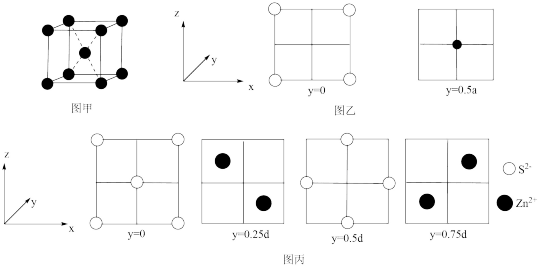
 ,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为
,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为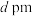 。下列关于ZnS晶胞的描述错误的是
。下列关于ZnS晶胞的描述错误的是
A.每个晶胞中含有的 数目为4 数目为4 |
B.与 距离最近且相等的 距离最近且相等的 有8个 有8个 |
C.该晶胞中两个距离最近的 和 和 的核间距的计算表达式为 的核间距的计算表达式为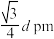 |
D.ZnS晶体的密度为 ( ( 表示阿伏加德罗常数) 表示阿伏加德罗常数) |
您最近一年使用:0次
2022-12-16更新
|
1134次组卷
|
3卷引用:辽宁省沈阳市五校协作体2022-2023学年高三上学期12月月考化学试题
6 . 回答下列问题
(1)硫化氢( )、二氧化硫(
)、二氧化硫( )是有害气体,可用多种方法进行脱除。(已知25℃时,
)是有害气体,可用多种方法进行脱除。(已知25℃时, 的
的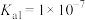 ,
, ,
, )
)
① 和
和 的VSEPR模型分别为
的VSEPR模型分别为______ 、______ 。
②室温下,若用足量的烧碱溶液吸收硫化氢气体,写出该反应的离子方程式______ ,计算25℃时,该反应的平衡常数为______ 。
③室温下,若在 硫酸铜溶液中通入过量
硫酸铜溶液中通入过量 气体,此时溶液中的PH是
气体,此时溶液中的PH是______ 。
(2)通过电化学循环法可将 转化为
转化为 和
和 (如图所示)。其中氧化过程发生如下两步反应:
(如图所示)。其中氧化过程发生如下两步反应: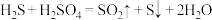 、
、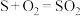

①电极a上发生反应的电极反应式为______ 。
②理论上1mol 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为______ 。
(3)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,下列说法中正确的是______。
,下列说法中正确的是______。

(1)硫化氢(
 )、二氧化硫(
)、二氧化硫( )是有害气体,可用多种方法进行脱除。(已知25℃时,
)是有害气体,可用多种方法进行脱除。(已知25℃时, 的
的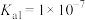 ,
, ,
, )
)①
 和
和 的VSEPR模型分别为
的VSEPR模型分别为②室温下,若用足量的烧碱溶液吸收硫化氢气体,写出该反应的离子方程式
③室温下,若在
 硫酸铜溶液中通入过量
硫酸铜溶液中通入过量 气体,此时溶液中的PH是
气体,此时溶液中的PH是(2)通过电化学循环法可将
 转化为
转化为 和
和 (如图所示)。其中氧化过程发生如下两步反应:
(如图所示)。其中氧化过程发生如下两步反应: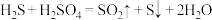 、
、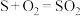

①电极a上发生反应的电极反应式为
②理论上1mol
 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为(3)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。已知该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,下列说法中正确的是______。
,下列说法中正确的是______。
A.该铁的氧化物化学式为 | B.距离 最近的 最近的 有6个 有6个 |
C.晶体中的 只能构成正四面体空隙 只能构成正四面体空隙 | D.晶胞的边长为 |
您最近一年使用:0次
名校
解题方法
7 . 已知:将Cl2通入适量NaOH溶液中,反应会放热,当温度升高后会发生如下反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O。则Cl2通入NaOH溶液的产物中可能有NaCl、NaClO、NaClO3中的两种或三种,且 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是| A.与碱的反应中,Cl2既是氧化剂又是还原剂 |
| B.参加反应的Cl2物质的量为0.5a mol |
C.若某温度下,反应后 =6,则溶液中 =6,则溶液中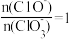 |
D.改变温度,反应中转移电子的物质的量可能为 mol mol |
您最近一年使用:0次
2022-10-24更新
|
2103次组卷
|
12卷引用:辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题
辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题 江苏省无锡市锡山高级中学2021-2022学年高一上学期期中考试化学试题山东省实验中学2022-2023学年高一上学期11月期中考试化学试题甘肃省酒泉市玉门油田第一中学2022-2023学年高一上学期期中考试化学(A卷)试题北京市第八中学2022-2023学年高一上学期12月月考化学试题陕西省榆林中学2022-2023学年高一上学期期末考试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试(选考)化学试题江苏省苏州中学2022-2023学年高一下学期开学考试化学试题陕西省安康市2022-2023学年高一下学期开学摸底考试化学试题山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题(已下线)专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
名校
解题方法
8 . 铜及其化合物在科学研究和工业生产中具有许多用途,请回答下列问题:
(1)写出基态Cu原子的价电子排布式_______ 。
(2)已知高温下 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因_______ 。
(3)配合物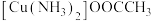 中碳原子的杂化类型是
中碳原子的杂化类型是_______ ,配体的空间构型为_______ 。配合物所含元素的电负性由大到小的顺序是_______ (用元素符号表示)。
(4)M原子的价电子排布式为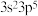 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
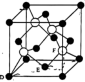
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为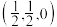 ,则F原子的坐标参数为
,则F原子的坐标参数为_______ 。
②已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为_______ pm(写出计算式)。
(1)写出基态Cu原子的价电子排布式
(2)已知高温下
 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因(3)配合物
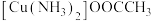 中碳原子的杂化类型是
中碳原子的杂化类型是(4)M原子的价电子排布式为
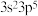 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为
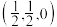 ,则F原子的坐标参数为
,则F原子的坐标参数为②已知该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为
您最近一年使用:0次
2022-10-12更新
|
459次组卷
|
4卷引用:辽宁省实验中学2023届高三上学期第一次阶段测试化学试题
名校
解题方法
9 . CoCl2可用于电镀,是一种性能优越的电池前驱材料,由含钴矿(Co元素主要以Co2O3、CoO的形式存在,还含有Fe、Si、Cu、Zn、Mn、Ni、Mg、Ca元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图:
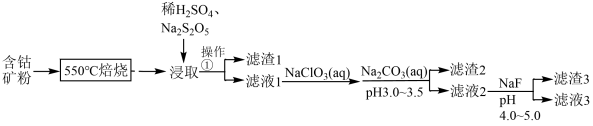
已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2难溶于水。
②CoCl2•6H2O的熔点为86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的pH见表:
回答下列问题:
(1)“550℃焙烧”的目的是____ 。
(2)“浸取”的过程中,用离子方程式表示Na2S2O5的作用是____ 。
(3)滤液1中加入NaClO3溶液的作用是____ 。
(4)加入Na2CO3溶液生成滤渣2的主要离子方程式为____ 。
滤液3经过多次萃取与反萃取制备CoCl2晶体:
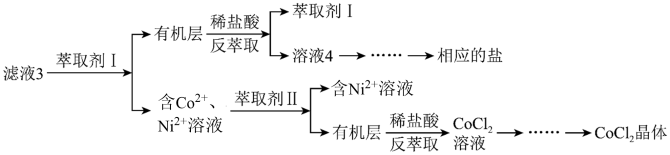
(5)滤液3中加入萃取剂I,然后用稀盐酸反萃取的目的是____ 。
(6)制备晶体CoCl2•6H2O,需在减压环境下烘干的原因是____ 。
(7)为测定制得的产品的纯度,现称取2.00gCoCl2•6H2O样品,将其用适当试剂转化为CoC2O4,再转化为草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用0.1000mol/L高锰酸钾溶液滴定,当达到滴定终点时,共用去高锰酸钾溶液24.00mL,该产品的纯度为____ 。

已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2难溶于水。
②CoCl2•6H2O的熔点为86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的pH见表:
| Co3+ | Fe3+ | Cu2+ | Co2+ | Fe2+ | Zn2+ | Mn2+ | Mg2+ | |
| 开始沉淀pH | 0.3 | 2.7 | 5.5 | 7.2 | 7.6 | 7.6 | 8.3 | 9.6 |
| 完全沉淀pH | 1.1 | 3.2 | 6.6 | 9.2 | 9.6 | 9.2 | 9.3 | 11.1 |
(1)“550℃焙烧”的目的是
(2)“浸取”的过程中,用离子方程式表示Na2S2O5的作用是
(3)滤液1中加入NaClO3溶液的作用是
(4)加入Na2CO3溶液生成滤渣2的主要离子方程式为
滤液3经过多次萃取与反萃取制备CoCl2晶体:

(5)滤液3中加入萃取剂I,然后用稀盐酸反萃取的目的是
(6)制备晶体CoCl2•6H2O,需在减压环境下烘干的原因是
(7)为测定制得的产品的纯度,现称取2.00gCoCl2•6H2O样品,将其用适当试剂转化为CoC2O4,再转化为草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用0.1000mol/L高锰酸钾溶液滴定,当达到滴定终点时,共用去高锰酸钾溶液24.00mL,该产品的纯度为
您最近一年使用:0次
名校
解题方法
10 . 我国提出2060年前实现碳中和,降低大气中CO2含量是当今世界重要科研课题之一,以CO2为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。回答下列问题:
(1)CO2在固体催化剂表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1=-156.9kJ·mol-l
CH4(g)+2H2O(g) ΔH1=-156.9kJ·mol-l
副反应:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.1kJ·mol-1
CO(g)+H2O(g) ΔH2=+41.1kJ·mol-1
①已知:2H2(g)+O2(g)=2H2O(g) ΔH3=-395.6kJ·mol-1,
则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=_______ 。
②500°C时,向1L恒容密闭容器中充入4mol CO2和12mol H2,初始压强为p,20min时主、3副反应都达到平衡状态,测得c(H2O)=5mol·L-1,体系压强为 p,则0~20min内v(CH4)=
p,则0~20min内v(CH4)=_______ ,平衡时CH4选择性=_______ (CH4选择性=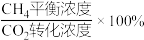 ,计算保留三位有效数字)。
,计算保留三位有效数字)。
(2)我国科研人员将CO2和H2在Na-Fe3O4/HZSM-5催化下转变为汽油(C5~C11的烃),反应过程如下图所示。
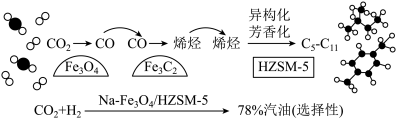
①若CO2在该条件下转化为戊烷(C5H12),则该反应的化学方程式为_______ 。
②催化剂中的Fe3O4可用电解法制备。电解时以Fe电极作电解池的_______ 极,电解质溶液为稀硫酸,铁电极的反应式为_______ 。
(3)甲醇催化制取乙烯的过程中发生如下反应:
反应1:3CH3OH(g) C3H6(g)+3H2O(g);
C3H6(g)+3H2O(g);
反应2:2CH3OH(g) C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)
反应1的Arthenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式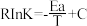 (Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=_______ kJ·mol-1.当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是_______ 。

(1)CO2在固体催化剂表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH1=-156.9kJ·mol-l
CH4(g)+2H2O(g) ΔH1=-156.9kJ·mol-l副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41.1kJ·mol-1
CO(g)+H2O(g) ΔH2=+41.1kJ·mol-1①已知:2H2(g)+O2(g)=2H2O(g) ΔH3=-395.6kJ·mol-1,
则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=
②500°C时,向1L恒容密闭容器中充入4mol CO2和12mol H2,初始压强为p,20min时主、3副反应都达到平衡状态,测得c(H2O)=5mol·L-1,体系压强为
 p,则0~20min内v(CH4)=
p,则0~20min内v(CH4)=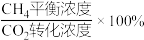 ,计算保留三位有效数字)。
,计算保留三位有效数字)。(2)我国科研人员将CO2和H2在Na-Fe3O4/HZSM-5催化下转变为汽油(C5~C11的烃),反应过程如下图所示。

①若CO2在该条件下转化为戊烷(C5H12),则该反应的化学方程式为
②催化剂中的Fe3O4可用电解法制备。电解时以Fe电极作电解池的
(3)甲醇催化制取乙烯的过程中发生如下反应:
反应1:3CH3OH(g)
 C3H6(g)+3H2O(g);
C3H6(g)+3H2O(g);反应2:2CH3OH(g)
 C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)反应1的Arthenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式
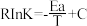 (Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=
您最近一年使用:0次
2022-08-20更新
|
919次组卷
|
3卷引用:辽宁省沈阳市法库县高级中学2022届高三下学期4月线上模拟考试化学试题

 、
、 、
、 、
、
 、
、 、
、 、
、


