名校
解题方法
1 . 下列化学用语或图示表达正确的是
A.乙烯分子中σ键的形成: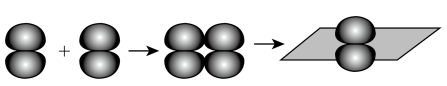 |
B.SO3的VSEPR模型: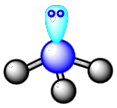 |
C.中子数为20的氯原子: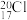 |
D.HClO的空间填充模型: |
您最近一年使用:0次
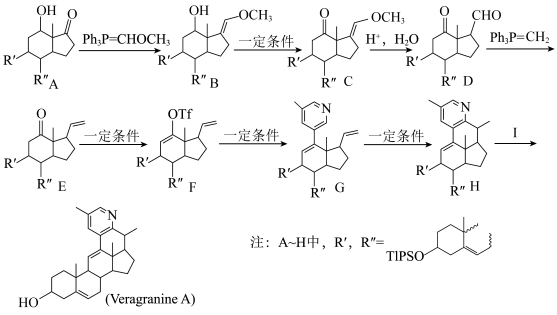
2 . Veragranine A是治疗骨关节疼痛的药物,一种合成路线如图(Ph为苯基,略去部分试剂和条件,忽略立体化学)。
(1)化合物B生成C的反应类型是_______ 。
(2)化合物C到D的反应中,另一产物的结构简式为_______ 。
(3)合成路线中化合物D发生反应的官能团名称为_______ 。可用于检验该官能团的试剂为_______ (填序号)。
①银氨溶液 ②氯化铁溶液 ③新制氢氧化铜溶液
(4)化合物G和H的质谱图中分子离子峰的质荷比数值相同,它们互为_______ 。
(5)化合物I是一种类似氯化铵的盐,分子式为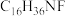 ,核磁共振氢谱有四组峰,峰面积比为
,核磁共振氢谱有四组峰,峰面积比为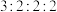 ,结构简式为
,结构简式为_______ 。
(6)Veragranine A中手性碳原子的个数为_______ 。
(7)结合上述合成路线和所学知识,设计以甲苯和 为原料合成
为原料合成 的路线
的路线_______ (无机试剂任选)。
(1)化合物B生成C的反应类型是
(2)化合物C到D的反应中,另一产物的结构简式为
(3)合成路线中化合物D发生反应的官能团名称为
①银氨溶液 ②氯化铁溶液 ③新制氢氧化铜溶液
(4)化合物G和H的质谱图中分子离子峰的质荷比数值相同,它们互为
(5)化合物I是一种类似氯化铵的盐,分子式为
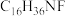 ,核磁共振氢谱有四组峰,峰面积比为
,核磁共振氢谱有四组峰,峰面积比为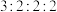 ,结构简式为
,结构简式为(6)Veragranine A中手性碳原子的个数为
(7)结合上述合成路线和所学知识,设计以甲苯和
 为原料合成
为原料合成 的路线
的路线
您最近一年使用:0次
3 . 下列有关氮、硫、氯的单质及其化合物的转化都能实现的是
A.工业制备漂白粉:饱和食盐水 Cl2 Cl2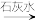 漂白粉 漂白粉 |
B.工业制备FeCl3:Fe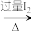 FeI2 FeI2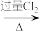 FeCl3 FeCl3 |
C.工业制备硫酸:FeS2 SO3 SO3 H2SO4 H2SO4 |
| D.实验室制备SO2:Na2SO3+2HNO3=2NaNO3+SO2↑+H2O |
您最近一年使用:0次
解题方法
4 . 我国研发的“无淡化海水原位直接电解制氢技术”装置如图所示,阴、阳极材料均为附着有 的
的 催化电极网,表面的
催化电极网,表面的 可选择性地紧密结合水电离出的
可选择性地紧密结合水电离出的 。下列说法不正确的是
。下列说法不正确的是
 的
的 催化电极网,表面的
催化电极网,表面的 可选择性地紧密结合水电离出的
可选择性地紧密结合水电离出的 。下列说法不正确的是
。下列说法不正确的是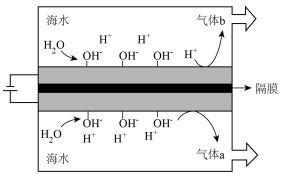
A.气体b为 |
B. 负电层可减少副产物 负电层可减少副产物 的生成 的生成 |
C. 等电极垢在阳极产生,应定期更换 等电极垢在阳极产生,应定期更换 |
| D.与海水淡化间接制氢相比,原位直接制氢成本低 |
您最近一年使用:0次
名校
5 . 碳酸钠是造纸、玻璃、纺织等行业的重要原料。工业碳酸钠(纯度约为98%)中含有少量 、
、 、
、 和
和 等杂质,提纯的工艺流程如下:
等杂质,提纯的工艺流程如下: 随温度变化的曲线如图所示。
随温度变化的曲线如图所示。
(1)设计实验方案,验证工业碳酸钠中含有杂质 ,写出该方案的操作和现象:
,写出该方案的操作和现象:_____ 。
(2)“滤渣”的主要成分为_______ (写化学式)。
(3)实验室进行“蒸发浓缩结晶”用到的主要仪器有蒸发皿、酒精灯、_______ 等。
(4)“趁热过滤”的目的是_______ 。
(5)若“母液”多次循环使用,可能导致的问题是_______ 。
(6)“加热脱水”属于_______ 变化(填“物理”或“化学”)。
(7)“检验”制备的试剂级碳酸钠纯度,设计如下实验方案:取 产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到
产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到 固体,则产品中
固体,则产品中 的质量分数为
的质量分数为_______ (用含 、
、 的式子表示)。
的式子表示)。
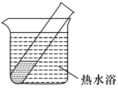
(8)实验室探究 和
和 的热稳定性,设计了如图装置。大试管中应盛放的固体是
的热稳定性,设计了如图装置。大试管中应盛放的固体是_______ ,理由是_______ 。
 、
、 、
、 和
和 等杂质,提纯的工艺流程如下:
等杂质,提纯的工艺流程如下:
 随温度变化的曲线如图所示。
随温度变化的曲线如图所示。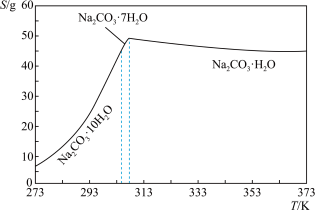
(1)设计实验方案,验证工业碳酸钠中含有杂质
 ,写出该方案的操作和现象:
,写出该方案的操作和现象:(2)“滤渣”的主要成分为
(3)实验室进行“蒸发浓缩结晶”用到的主要仪器有蒸发皿、酒精灯、
(4)“趁热过滤”的目的是
(5)若“母液”多次循环使用,可能导致的问题是
(6)“加热脱水”属于
(7)“检验”制备的试剂级碳酸钠纯度,设计如下实验方案:取
 产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到
产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到 固体,则产品中
固体,则产品中 的质量分数为
的质量分数为 、
、 的式子表示)。
的式子表示)。(8)实验室探究
 和
和 的热稳定性,设计了如图装置。大试管中应盛放的固体是
的热稳定性,设计了如图装置。大试管中应盛放的固体是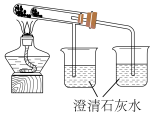
您最近一年使用:0次
解题方法
6 . 以废铁屑(主要成分为Fe及少量 ,还有油污、磷、硫等杂质)为原料制备硫酸亚铁铵晶体,生成
,还有油污、磷、硫等杂质)为原料制备硫酸亚铁铵晶体,生成 的反应为
的反应为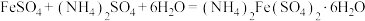 ,具体步骤如下:
,具体步骤如下:
Ⅰ.在废铁屑中加入 溶液,水浴加热。
溶液,水浴加热。
Ⅱ.洗涤废铁屑,加入过量稀 ,加热至充分反应(装置如图)。
,加热至充分反应(装置如图)。
Ⅳ.将饱和硫酸铵溶液加入上述滤液中,加热搅拌。
Ⅴ.将Ⅳ中所得溶液经一系列操作制得硫酸亚铁铵晶体。
回答下列问题:
(1)仪器a的名称为_______ 。
(2)步骤Ⅰ中 溶液的主要作用是
溶液的主要作用是_______ 。
(3)步骤Ⅱ中与Fe元素相关的反应,除 外,还有
外,还有_______ 、_______ (用离子方程式表示)。
(4)装置B的作用是_______ 。
(5)步骤Ⅴ中一系列操作指_______ 、_______ 、过滤、洗涤、干燥。
(6)图为硫酸亚铁铵晶体的局部结构示意图,所缺微粒Y的化学式为_______ 。 与
与 反应生成有色配合物来检验
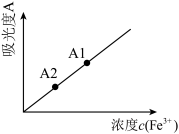
反应生成有色配合物来检验 含量,配合物溶液颜色越深,吸光度越大。将质量相同的两份产品S1和S2配成体积相同的溶液,吸光度分别为A1和A2(如图),则产品的纯度:S1
含量,配合物溶液颜色越深,吸光度越大。将质量相同的两份产品S1和S2配成体积相同的溶液,吸光度分别为A1和A2(如图),则产品的纯度:S1_______ S2(填“ ”或“
”或“ ”)。
”)。 的含量,其离子方程式如下:
的含量,其离子方程式如下: ,准确称取产品1.6000g,配成100.00mL溶液。移取该溶液25.00mL,用
,准确称取产品1.6000g,配成100.00mL溶液。移取该溶液25.00mL,用 酸性
酸性 溶液滴定,消耗
溶液滴定,消耗 溶液的体积为20.00mL,则产品中
溶液的体积为20.00mL,则产品中 的含量为
的含量为_______ %(已知: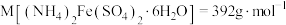 )。
)。
 ,还有油污、磷、硫等杂质)为原料制备硫酸亚铁铵晶体,生成
,还有油污、磷、硫等杂质)为原料制备硫酸亚铁铵晶体,生成 的反应为
的反应为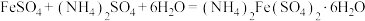 ,具体步骤如下:
,具体步骤如下:Ⅰ.在废铁屑中加入
 溶液,水浴加热。
溶液,水浴加热。Ⅱ.洗涤废铁屑,加入过量稀
 ,加热至充分反应(装置如图)。
,加热至充分反应(装置如图)。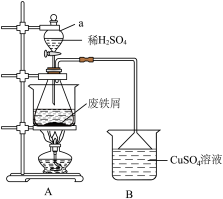
Ⅳ.将饱和硫酸铵溶液加入上述滤液中,加热搅拌。
Ⅴ.将Ⅳ中所得溶液经一系列操作制得硫酸亚铁铵晶体。
回答下列问题:
(1)仪器a的名称为
(2)步骤Ⅰ中
 溶液的主要作用是
溶液的主要作用是(3)步骤Ⅱ中与Fe元素相关的反应,除
 外,还有
外,还有(4)装置B的作用是
(5)步骤Ⅴ中一系列操作指
(6)图为硫酸亚铁铵晶体的局部结构示意图,所缺微粒Y的化学式为

 与
与 反应生成有色配合物来检验
反应生成有色配合物来检验 含量,配合物溶液颜色越深,吸光度越大。将质量相同的两份产品S1和S2配成体积相同的溶液,吸光度分别为A1和A2(如图),则产品的纯度:S1
含量,配合物溶液颜色越深,吸光度越大。将质量相同的两份产品S1和S2配成体积相同的溶液,吸光度分别为A1和A2(如图),则产品的纯度:S1 ”或“
”或“ ”)。
”)。
 的含量,其离子方程式如下:
的含量,其离子方程式如下: ,准确称取产品1.6000g,配成100.00mL溶液。移取该溶液25.00mL,用
,准确称取产品1.6000g,配成100.00mL溶液。移取该溶液25.00mL,用 酸性
酸性 溶液滴定,消耗
溶液滴定,消耗 溶液的体积为20.00mL,则产品中
溶液的体积为20.00mL,则产品中 的含量为
的含量为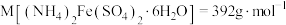 )。
)。
您最近一年使用:0次
名校
解题方法
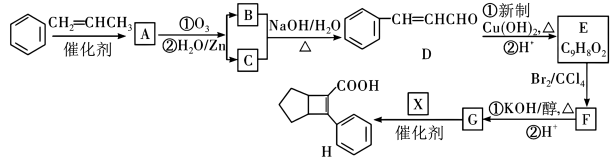
7 . 化合物H是一种有机材料中间体。实验室由苯制备H的一种合成路线如下:
(1)有机物H的分子式为_______ ,该分子中所含官能团的名称为_______ 。
(2)A的结构简式为_______ 。
(3)B+C→D经过两步反应,其反应类型依次分别为_______ 、_______ 。
(4)F→G的第①步反应的化学方程式为_______ 。
(5)E有多种同分异构体,符合下列条件的有_______ 种(不包括E),其中核磁共振氢谱为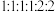 的结构简式为
的结构简式为_______ 。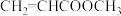 的合成路线
的合成路线_______ (其他试剂任选)。
已知:①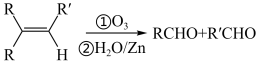
②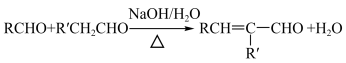
③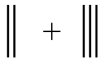


(1)有机物H的分子式为
(2)A的结构简式为
(3)B+C→D经过两步反应,其反应类型依次分别为
(4)F→G的第①步反应的化学方程式为
(5)E有多种同分异构体,符合下列条件的有
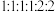 的结构简式为
的结构简式为①能使溴的四氯化碳溶液褪色,②含“ ”基团
”基团
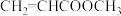 的合成路线
的合成路线
您最近一年使用:0次
名校
解题方法
8 .  可活化
可活化 放出
放出 ,其反应历程如下图所示:
,其反应历程如下图所示:
 可活化
可活化 放出
放出 ,其反应历程如下图所示:
,其反应历程如下图所示: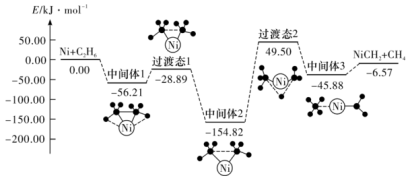
| A.该反应的决速步是:中间体2→中间体3 |
| B.只涉及极性键的断裂和生成 |
C. 是该反应的催化剂 是该反应的催化剂 |
D.该反应的热化学方程式为: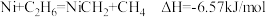 |
您最近一年使用:0次
名校
9 . 某化学小组查阅资料发现强碱条件下,加热银氨溶液也可以析出银镜,并做了以下两组实验进行分析证明。已知: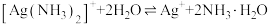 。
。
下列说法正确的是
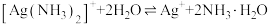 。
。| 装置 | 实验序号 | 试管中的药品 | 现象 |
| 实验I |  银氨溶液和数滴较浓 银氨溶液和数滴较浓 溶液 溶液 | 有气泡产生,一段时间后,溶液逐渐变黑,试管壁附着银镜 |
| 实验Ⅱ |  银氨溶液和数滴浓氨水 银氨溶液和数滴浓氨水 | 有气泡产生,一段时间后,溶液无明显变化 |
| A.两组实验中产生的气体成分完全相同 |
B.实验I的黑色固体中有 |
C.清洗实验后的银镜时,用 溶液清洗的效果优于 溶液清洗的效果优于 溶液 溶液 |
| D.实验I产生银镜的原因是银氨溶液在碱性条件下被空气中的氧气氧化所致 |
您最近一年使用:0次
名校
解题方法
10 . 已知 时,
时, 和
和 的饱和溶液中,a、b分别表示
的饱和溶液中,a、b分别表示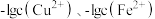 与溶液
与溶液 的变化关系。下列说法中正确的是
的变化关系。下列说法中正确的是
 时,
时, 和
和 的饱和溶液中,a、b分别表示
的饱和溶液中,a、b分别表示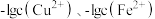 与溶液
与溶液 的变化关系。下列说法中正确的是
的变化关系。下列说法中正确的是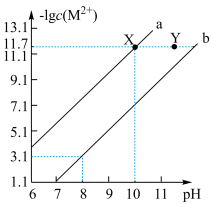
A.该温度下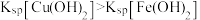 |
B.当 和 和 沉淀共存时,溶液中 沉淀共存时,溶液中 |
C.除去 溶液中少量的 溶液中少量的 ,可加入适量 ,可加入适量 或 或 |
D.向X点对应的饱和溶液中加入少量 ,可转化为Y点对应的溶液 ,可转化为Y点对应的溶液 |
您最近一年使用:0次